金属铝在生产生活中有广泛用途。
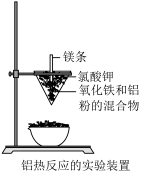
(1)写出工业通过电解法生产铝的化学方程式___________
(2)写出该铝热反应的化学方程式___________ ;利用铝热反应在工业上可冶炼___________ 金属(填编号)。
A.强还原性 B.难熔性 C.易导电 D.活泼
(3)反应结束后,从沙中取出生成的固体物质,该固体可能是铁铝合金,请同学设计实验证明。______
(4)某溶液中含有 0.15mol 的AlCl3,向其中加入 1mol/L 的NaOH溶液,得到沉淀7.8g,加入NaOH溶液的体积为___________ 。

(1)写出工业通过电解法生产铝的化学方程式
(2)写出该铝热反应的化学方程式
A.强还原性 B.难熔性 C.易导电 D.活泼
(3)反应结束后,从沙中取出生成的固体物质,该固体可能是铁铝合金,请同学设计实验证明。
(4)某溶液中含有 0.15mol 的AlCl3,向其中加入 1mol/L 的NaOH溶液,得到沉淀7.8g,加入NaOH溶液的体积为
更新时间:2023-05-28 15:03:53
|
相似题推荐
【推荐1】铝及其化合物在生活、生产中有广泛应用。
(1)饮用水可用明矾、铁明矾[Al2Fe(SO4)4·xH2O]净化,用____ (填方法名称)检验它们在水中形成了胶体。
(2)CuAlO2是重要的化工产品,通常用氢氧化铝和氢氧化铜按一定比例混合在高温下反应制备。配平化学方程式: Cu(OH)2+ Al(OH)3 CuAlO2+ + H2O。
CuAlO2+ + H2O。___________
(3)冰晶石(Na3AlF6)是工业冶炼铝的助熔剂。工业上将碳酸钠、氢氧化铝与氢氟酸按一定比例混合在高温下反应制备冰晶石。在该反应中理想的Na2CO3、HF投料的物质的量之比为______ 。
(4)工业上,用真空碳热还原-氯化法制备金属铝,其中间产物有Al4C3。Al4C3与盐酸反应生成一种含氢质量分数最高的烃,写出该反应的离子方程式_____________ 。
(5)镁铝合金(Mg17Al12)是一种潜在的贮氢材料。一般在氩气环境中将一定量的镁、铝单质在一定温度下熔炼获得。该合金在一定条件下可完全吸收氢得到混合物Y(含MgH2和Al),Y在一定条件下可释放出氢气。
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是___________ 。
②写出镁铝合金在一定条件下完全吸氢的化学方程式________________ 。
③在6 mol·L-1盐酸中,混合物Y能完全释放出H2。a mol镁铝合金完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出H2的物质的量为______ mol。
(1)饮用水可用明矾、铁明矾[Al2Fe(SO4)4·xH2O]净化,用
(2)CuAlO2是重要的化工产品,通常用氢氧化铝和氢氧化铜按一定比例混合在高温下反应制备。配平化学方程式: Cu(OH)2+ Al(OH)3
 CuAlO2+ + H2O。
CuAlO2+ + H2O。(3)冰晶石(Na3AlF6)是工业冶炼铝的助熔剂。工业上将碳酸钠、氢氧化铝与氢氟酸按一定比例混合在高温下反应制备冰晶石。在该反应中理想的Na2CO3、HF投料的物质的量之比为
(4)工业上,用真空碳热还原-氯化法制备金属铝,其中间产物有Al4C3。Al4C3与盐酸反应生成一种含氢质量分数最高的烃,写出该反应的离子方程式
(5)镁铝合金(Mg17Al12)是一种潜在的贮氢材料。一般在氩气环境中将一定量的镁、铝单质在一定温度下熔炼获得。该合金在一定条件下可完全吸收氢得到混合物Y(含MgH2和Al),Y在一定条件下可释放出氢气。
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是
②写出镁铝合金在一定条件下完全吸氢的化学方程式
③在6 mol·L-1盐酸中,混合物Y能完全释放出H2。a mol镁铝合金完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出H2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示,则B点时铬的氧化物化学式为___________ 。


您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求进行计算,直接写出结果。
(1)标准状况下,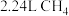 所含氢原子的物质的量为
所含氢原子的物质的量为_______ mol。
(2)含 氧原子的
氧原子的 的质量是
的质量是_______ g。
(3)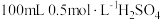 溶液中,
溶液中, 的物质的量浓度为
的物质的量浓度为_______  。
。
(4) 碳在一定量氧气中反应,生成气体的质量为
碳在一定量氧气中反应,生成气体的质量为 。所得气体的物质的量为
。所得气体的物质的量为_______  。
。
(5)向 某浓度的
某浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 ,充分反应后,得到
,充分反应后,得到 和
和 的混合溶液。向上述所得溶液中,逐滴滴加
的混合溶液。向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
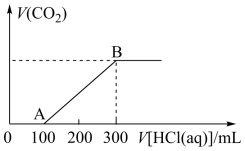
①OA段发生反应的离子方程式为_______ 。
②B点时,反应所得溶液中溶质的物质的量浓度是_______  。
。
(1)标准状况下,
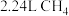 所含氢原子的物质的量为
所含氢原子的物质的量为(2)含
 氧原子的
氧原子的 的质量是
的质量是(3)
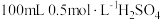 溶液中,
溶液中, 的物质的量浓度为
的物质的量浓度为 。
。(4)
 碳在一定量氧气中反应,生成气体的质量为
碳在一定量氧气中反应,生成气体的质量为 。所得气体的物质的量为
。所得气体的物质的量为 。
。(5)向
 某浓度的
某浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 ,充分反应后,得到
,充分反应后,得到 和
和 的混合溶液。向上述所得溶液中,逐滴滴加
的混合溶液。向上述所得溶液中,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
①OA段发生反应的离子方程式为
②B点时,反应所得溶液中溶质的物质的量浓度是
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知高温条件下2Al+Fe2O3=2Fe+Al2O3放出大量的热,据说可用于定向爆破和焊接铁轨。请回答下列问题:
①该反应中氧化剂是_____________ ,______________ 元素被氧化。
②标出该反应的电子转移方向和数目__________________________________ 。
③欲除去产物中的Al2O3,请写出所加试剂的离子反应方程式___________________ 。
①该反应中氧化剂是
②标出该反应的电子转移方向和数目
③欲除去产物中的Al2O3,请写出所加试剂的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现行教材中给我们介绍的“铝热反应”是用铝粉和氧化铁混合物,在镁条燃烧产生的高温下发生反应的。
(1)该反应的化学方程式为:__________________________________________________ ;
该反应是________ (填“吸热”或“放热”)反应;以上叙述中除镁条外,还缺少一种药品,它是__________ ,在该反应中的作用是____________________________________________ 。
(2)工业冶金常用以下四法:①焦炭法;②水煤气法;③活泼金属置换法;④电解法。
用“铝热反应”原理冶炼金属锰属于_____________________________________________ 。
(1)该反应的化学方程式为:
该反应是
(2)工业冶金常用以下四法:①焦炭法;②水煤气法;③活泼金属置换法;④电解法。
用“铝热反应”原理冶炼金属锰属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铝是一种重要的金属。
(1)铝在元素周期表中的位置是_______________________________ 。
(2)生产中曾用铝热反应焊接钢轨,铝与氧化铁发生反应的化学方程式为____________ 。铝热反应也可以用于金属的冶炼,有同学认为将氧化镁和铝分放一起在高温下可用于镁的冶炼,你认为此说法________ (填对或不对),认为不对的请说出原因____________________________ 并写出镁的冶炼的化学方程式 ________________________________________ (认为对的此项可不作答)。
(3)铝与NaOH溶液反应的离子方程式为_____________________ ;
(4)以AlCl3溶液为原料制取无水AlCl3,先制得AlCl3·6H2O晶体,主要操作包括①________ ,②冷却结晶,③过滤。在第①步操作中应注意的事项是__________________ 。
(5).加热AlCl3·6H2O晶体,能进一步制取无水AlCl3,此操作应注意在___________ ,其原因是(结合化学方程式简要说明)______________ 。
(1)铝在元素周期表中的位置是
(2)生产中曾用铝热反应焊接钢轨,铝与氧化铁发生反应的化学方程式为
(3)铝与NaOH溶液反应的离子方程式为
(4)以AlCl3溶液为原料制取无水AlCl3,先制得AlCl3·6H2O晶体,主要操作包括①
(5).加热AlCl3·6H2O晶体,能进一步制取无水AlCl3,此操作应注意在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知有关物质的熔、沸点数据如下表:
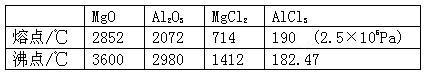
请参考上述数据回答下列问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁;也不用电解AlCl3的方法生产铝?
答___________ 。
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。

请参考上述数据回答下列问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁;也不用电解AlCl3的方法生产铝?
答___________ 。
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是___ 。
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___ ,氧化性最弱的简单阳离子是___ 。
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是___ ;制铝时,电解Al2O3而不电解AlCl3的原因是___ 。
(4)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗)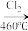 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)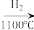 Si(纯)
Si(纯)
写出SiCl4的电子式:___ ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:____ 。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是____ 。
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:____ 。
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是
(4)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗)
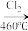 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)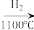 Si(纯)
Si(纯)写出SiCl4的电子式:
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】除了金、铂等极少数金属外,绝大多数金属元素以化合物的形式存在于自然界。利用金属活泼性的不同,可以采用不同的冶炼方法获取金属。
(1)“ 霍尔一埃鲁铝电解法” 是以氧化铝为原料、冰晶石为熔剂通过电解的方法制得铝,该反应的化学方程式是____________ 。
(2)获得金属锰一般用“ 铝热法”,即在高温下用铝与二氧化锰反应,该反应的化学方程式是________ ,其中的还原剂是______________ 。
(3)“ 皮江法” 冶炼镁的工业流程如下所示:
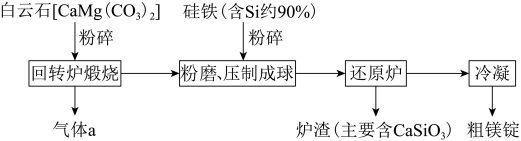
①气体a是_____________ ;
②粉碎、粉磨的目的是______________ 和________________ ;
③还原炉中将空气抽出,使炉内近似真空的原因是________________ 。
(1)“ 霍尔一埃鲁铝电解法” 是以氧化铝为原料、冰晶石为熔剂通过电解的方法制得铝,该反应的化学方程式是
(2)获得金属锰一般用“ 铝热法”,即在高温下用铝与二氧化锰反应,该反应的化学方程式是
(3)“ 皮江法” 冶炼镁的工业流程如下所示:

①气体a是
②粉碎、粉磨的目的是
③还原炉中将空气抽出,使炉内近似真空的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】小强同学准备制取乙烯并探究乙烯与溴的反应(提示:在制乙烯时易生成SO2)。在I至IV的仪器中盛放的药品顺序为:无水乙醇、浓硫酸;溴水;氢氧化钠溶液;品红溶液。准备的仪器如图。
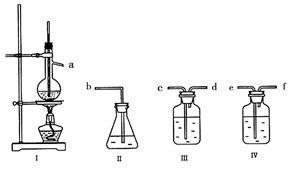
(1)仪器各接口顺序为_______ 。
(2)I中无水乙醇与浓硫酸的体积比为_______ 反应方程式为_______ 。
(3)II中的化学方程式是_______ 。
(4)III IV的作用为_______ 。
若没有这两个装置,则易发生反应的离子方程式为_______ 。

(1)仪器各接口顺序为
(2)I中无水乙醇与浓硫酸的体积比为
(3)II中的化学方程式是
(4)III IV的作用为
若没有这两个装置,则易发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】胶体是一种重要的分散系。
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈________ 色,即可制得Fe(OH)3胶体。
(2)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到_______ 烧杯(填甲”或“乙”)中的液体产生丁达尔效应。
(3)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中逐渐滴加稀盐酸至过量,在此过程中可以观察到的现象是______________________________________________________________ 。
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至溶液呈
(2)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
(3)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中逐渐滴加稀盐酸至过量,在此过程中可以观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某实验小组同学模拟工业制碘的方法,探究 和I-的反应规律。实验操作及现象如表:
和I-的反应规律。实验操作及现象如表:
(1)取实验2后的溶液,进行如图实验:
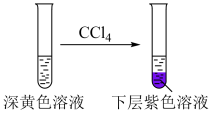
①检验 的还原产物。取上层清液,
的还原产物。取上层清液,___________ (填操作和现象),说明 被还原为Cl﹣。
被还原为Cl﹣。
②写出加入0.20mLNaClO3后,溶液中 和Cl﹣发生反应的离子方程式:
和Cl﹣发生反应的离子方程式:___________ 。
(2)查阅资料:定条件下,I-和I2都可以被氧化成 。
。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2.进行实验:
①取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有 。
。
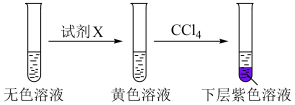
其中试剂X可以是___________ (填字母序号)。
a.碘水b.KMnO4溶液c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,发现湿润的淀粉试纸没有明显变化。进行以上对比实验的目的是___________ ,进一步佐证实验4中生成了Cl2。
获得结论:NaClO3溶液用量增加导致溶液褪色的原因是___________ (用离子方程式表示)。
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
对比实验4和5,可以获得的结论是___________ 。
 和I-的反应规律。实验操作及现象如表:
和I-的反应规律。实验操作及现象如表:| 实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
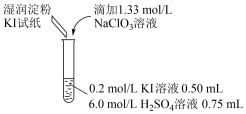 | 1 | 0.05mL | 浅黄色 | 无色 |
| 2 | 0.20mL | 深黄色 | 无色 | |
| 3 | 0.25mL | 浅黄色 | 蓝色 | |
| 4 | 0.30mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如图实验:

①检验
 的还原产物。取上层清液,
的还原产物。取上层清液, 被还原为Cl﹣。
被还原为Cl﹣。②写出加入0.20mLNaClO3后,溶液中
 和Cl﹣发生反应的离子方程式:
和Cl﹣发生反应的离子方程式:(2)查阅资料:定条件下,I-和I2都可以被氧化成
 。
。作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2.进行实验:
①取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有
 。
。
其中试剂X可以是
a.碘水b.KMnO4溶液c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,发现湿润的淀粉试纸没有明显变化。进行以上对比实验的目的是
获得结论:NaClO3溶液用量增加导致溶液褪色的原因是
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
| 编号 | 6.0mol•L-1H2SO4溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
| 5 | 0.25mL | 浅黄色 | 无色 |
对比实验4和5,可以获得的结论是
您最近一年使用:0次



