化学反应中常伴随着能量变化,请按要求回答问题:
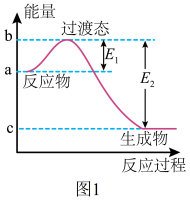
(1)1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图如图1所示,已知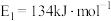 ,
, ,NO2和CO反应的热化学方程式为
,NO2和CO反应的热化学方程式为_______ 。
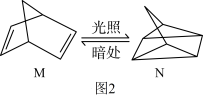
(2)有机物M经过太阳光光照可转化成N,转化过程如图2所示: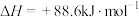 ,分则M、N相比,较稳定的是
,分则M、N相比,较稳定的是_______ 。
(3)25℃、101kPa时,56gCO在足量的O2中充分燃烧,放出565.2kJ热量,则CO的燃烧热为
_______ 。
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料, ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为_______ kJ。
(5)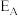 、
、 、
、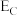 、
、 分别表示A(g)、B(g)、C(g)、D(g)所具有的能量,则对于反应:
分别表示A(g)、B(g)、C(g)、D(g)所具有的能量,则对于反应:
_______  (用含
(用含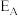 、
、 、
、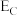 、
、 的代数式表示)。
的代数式表示)。
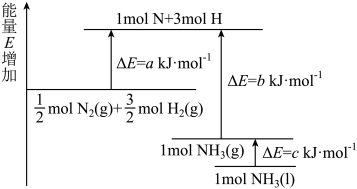
(6)合成氨反应的能量变化如下图所示,则反应
_______  。
。
(7)用50mL0.50mol/L盐酸与50mL0.65mol/LNaOH溶液进行中和反应的反应热的测定实验,测得酸、碱初始温度的平均值为25.0℃,反应过程中监测到最高温度的平均值为28.4℃,实验中盐酸和氢氧化钠溶液的密度均可取为 ,反应后溶液的比热容
,反应后溶液的比热容 。则生成1mol液态水时,反应热
。则生成1mol液态水时,反应热
_______  (
(保留三位有效数字 )。
(1)1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图如图1所示,已知
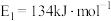 ,
, ,NO2和CO反应的热化学方程式为
,NO2和CO反应的热化学方程式为
(2)有机物M经过太阳光光照可转化成N,转化过程如图2所示:
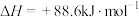 ,分则M、N相比,较稳定的是
,分则M、N相比,较稳定的是
(3)25℃、101kPa时,56gCO在足量的O2中充分燃烧,放出565.2kJ热量,则CO的燃烧热为

(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,
 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(5)
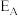 、
、 、
、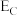 、
、 分别表示A(g)、B(g)、C(g)、D(g)所具有的能量,则对于反应:
分别表示A(g)、B(g)、C(g)、D(g)所具有的能量,则对于反应:
 (用含
(用含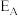 、
、 、
、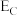 、
、 的代数式表示)。
的代数式表示)。(6)合成氨反应的能量变化如下图所示,则反应

 。
。
(7)用50mL0.50mol/L盐酸与50mL0.65mol/LNaOH溶液进行中和反应的反应热的测定实验,测得酸、碱初始温度的平均值为25.0℃,反应过程中监测到最高温度的平均值为28.4℃,实验中盐酸和氢氧化钠溶液的密度均可取为
 ,反应后溶液的比热容
,反应后溶液的比热容 。则生成1mol液态水时,反应热
。则生成1mol液态水时,反应热
 (
(
更新时间:2023-05-29 06:34:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂H2O2。当它们混合发生反应时,立即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol肼与足量H2O2反应,生成水蒸气和氮气,放出256.625 kJ的热量。
(1)该反应的热化学方程式为:_________________ 。
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ/mo则16 g肼与足量液态H2O2反应生成液态水时放出的热量是_________________ 。
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体之外,还有一个很大的优点是:_________________ 。
(4)发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) ΔH=+66.4 kJ·mol-1;N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
肼和二氧化氮反应的热化学方程式为:_________________ 。
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=_________ 。
(6)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1______ ΔH2。(填“>”“<”或“=”)
(1)该反应的热化学方程式为:
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ/mo则16 g肼与足量液态H2O2反应生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体之外,还有一个很大的优点是:
(4)发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) ΔH=+66.4 kJ·mol-1;N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
肼和二氧化氮反应的热化学方程式为:
(5)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+489.0 kJ·mol-1
CO(g)+
 O2(g)=CO2(g) △H=-283.0 kJ·mol-1
O2(g)=CO2(g) △H=-283.0 kJ·mol-1C(石墨)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=
(6)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某氮肥厂氨氮废水中的氮元素多以 和NH3·H2O的形式存在,该废水的处理流程如图所示:
和NH3·H2O的形式存在,该废水的处理流程如图所示:

过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收a.n
过程Ⅱ:在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
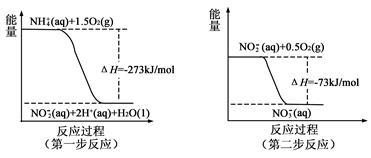
(1)第一步反应是_______ 反应(选填“放热”或“吸热”),判断依据是_______ 。
(2)1 mol (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
 和NH3·H2O的形式存在,该废水的处理流程如图所示:
和NH3·H2O的形式存在,该废水的处理流程如图所示:
过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收a.n
过程Ⅱ:在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
(1)第一步反应是
(2)1 mol
 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答问题
(1)如图所示,N4分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为N2时要_______ (填“吸收”或“放出”)热量______ kJ。

(2)某氢氧燃料电池的工作原理如图所示,a、b均为惰性电极。

①使用时,氢气从_____ 口通入(填“A”或“B”);
②b极的电极反应式为______ 。
③若装置转移了0.16mol电子,则在标准状况下需通入空气的体积为______ L(设氧气占空气体积的20%)
(3)某温度下,在2L恒容密闭容器中,发生反应: ,其中A、B、C三种物质的物质的量随时间变化曲线如图所示:
,其中A、B、C三种物质的物质的量随时间变化曲线如图所示:

①c=______ 。
②0~5min内,用A表示的化学反应速率为_______ 。
③下列条件能够加快其化学反应速率的是______ (填序号)。
a.升高温度 b.加入一定量的D c.加入合适的催化剂
(1)如图所示,N4分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为N2时要

(2)某氢氧燃料电池的工作原理如图所示,a、b均为惰性电极。

①使用时,氢气从
②b极的电极反应式为
③若装置转移了0.16mol电子,则在标准状况下需通入空气的体积为
(3)某温度下,在2L恒容密闭容器中,发生反应:
 ,其中A、B、C三种物质的物质的量随时间变化曲线如图所示:
,其中A、B、C三种物质的物质的量随时间变化曲线如图所示:
①c=
②0~5min内,用A表示的化学反应速率为
③下列条件能够加快其化学反应速率的是
a.升高温度 b.加入一定量的D c.加入合适的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)在200℃、101kPa时,0.5molH2(g)与足量I2(g)完全反应放出7.45kJ的热量,该反应的热化学方程式表示为____ 。
(2)根据键能数据估算
CH4(g)+4F2(g) =CF4(g)+4HF(g)的反应热ΔH为______ kJ/mol
(3) 已知:①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH1=-a kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-b kJ/mol
③2H2(g) + O2(g) = 2H2O(g) ΔH3 = -c kJ/mol
a、b、c均大于0 则:反应①中,ΔS______ (选填“>”、“<”或“=”)0;
2C(s)+4H2(g)+O2(g) = 2CH3OH(l) ΔH=_______ kJ/mol。
(1)在200℃、101kPa时,0.5molH2(g)与足量I2(g)完全反应放出7.45kJ的热量,该反应的热化学方程式表示为
(2)根据键能数据估算
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
CH4(g)+4F2(g) =CF4(g)+4HF(g)的反应热ΔH为
(3) 已知:①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH1=-a kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-b kJ/mol
③2H2(g) + O2(g) = 2H2O(g) ΔH3 = -c kJ/mol
a、b、c均大于0 则:反应①中,ΔS
2C(s)+4H2(g)+O2(g) = 2CH3OH(l) ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s) + O2(g) = CO2(g);ΔH = -393.15 kJ·mol-1 ①
途径Ⅱ 先制成水煤气:
C(s) + H2O(g) = CO(g) + H2(g); ΔH2 ②
再燃料水煤气:
2CO(g) + O2(g) = 2CO2(g); ΔH= -566kJ·mol-1 ③
2H2(g) + O2(g) = 2H2O(g);ΔH= -484 kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上_________ (填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH2=_______________ 。
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为
NO(g)+O3(g)==NO2(g)+O2(g) ΔH=-200.9kJ·mol-1
NO(g)+ O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
SO2(g)+O3(g)==SO3(g)+O2(g) ΔH=-241.6kJ·mol-1
反应3NO(g)+O3(g)==3NO2(g)的ΔH=________ kJ·mol-1。
(4)已知下列各组热化学方程式
① Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 △H=-25kJ/mol
② 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③ Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式______________________________ 。
(5)在标准状况下的11.2L甲烷完全燃烧生成CO2 和液态水放出444.8kJ热量(298K),其燃烧热的热化学方程式______________________________________________________ ; 已知断裂下列1mol化学键需要吸收的能量分别为:C=O:745kJ/mol , O=O:496kJ/mol , C-H:414kJ/mol 则断裂1molH-O键需要提供的能量为____________________ kJ。
途径Ⅰ C(s) + O2(g) = CO2(g);ΔH = -393.15 kJ·mol-1 ①
途径Ⅱ 先制成水煤气:
C(s) + H2O(g) = CO(g) + H2(g); ΔH2 ②
再燃料水煤气:
2CO(g) + O2(g) = 2CO2(g); ΔH= -566kJ·mol-1 ③
2H2(g) + O2(g) = 2H2O(g);ΔH= -484 kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上
(2)ΔH2=
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为
NO(g)+O3(g)==NO2(g)+O2(g) ΔH=-200.9kJ·mol-1
NO(g)+
 O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
O2(g)==NO2(g) ΔH=-58.2kJ·mol-1SO2(g)+O3(g)==SO3(g)+O2(g) ΔH=-241.6kJ·mol-1
反应3NO(g)+O3(g)==3NO2(g)的ΔH=
(4)已知下列各组热化学方程式
① Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 △H=-25kJ/mol
② 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③ Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式
(5)在标准状况下的11.2L甲烷完全燃烧生成CO2 和液态水放出444.8kJ热量(298K),其燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式___ 。
(2)PCl5分解成PCl3和Cl2的热化学方程式___ 。
(3)P和Cl2分两步反应生成1molPCl5的△H3=__ ,P和Cl2一步反应生成1molPCl5的△H4___ △H3 (填“大于”、“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是__ 。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式
(2)PCl5分解成PCl3和Cl2的热化学方程式
(3)P和Cl2分两步反应生成1molPCl5的△H3=
(4)PCl5与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是
您最近一年使用:0次
【推荐1】中和热的测定实验中,分多次将NaOH溶液倒入装盐酸的小烧杯中,测出来的中和热的数值偏小。 _____
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)已知1g的甲烷完全燃烧生成液态水放出akJ的热量,写出表示甲烷燃烧热的热化学方程式为___ 。
(2)某实验小组用100mL0.55mol·L-1NaOH溶液与100mL0.5mol·L-1盐酸进行中和热的测定。装置如图所示。
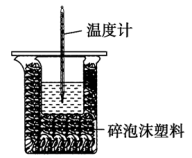
回答下列问题:
①图中装置缺少的仪器是____ 。
②碱稍过量的原因是____ 。
③若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1____ ΔH(填写<、>、=);若测得该反应放出的热量为2.865kJ,请写出盐酸与NaOH溶液反应的中和热的热化学方程式:__
(3)已知拆开1molH-H键、1molCl-Cl键、1molH—Cl键分别需要的能量是akJ、bkJ、ckJ,则反应H2(g)+Cl2(g)=2HCl(g)的∆H=____ 。
(4)①2O2(g)+N2(g)=N2O4(l) ∆H1
②N2(g)+2H2(g)=N2H4(l) ∆H2
③O2(g)+2H2(g)=2H2O(g) ∆H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ∆H4
上述反应热效应之间的关系式为∆H4=____ (用∆H1、∆H2、∆H3表示)。
(2)某实验小组用100mL0.55mol·L-1NaOH溶液与100mL0.5mol·L-1盐酸进行中和热的测定。装置如图所示。

回答下列问题:
①图中装置缺少的仪器是
②碱稍过量的原因是
③若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1
(3)已知拆开1molH-H键、1molCl-Cl键、1molH—Cl键分别需要的能量是akJ、bkJ、ckJ,则反应H2(g)+Cl2(g)=2HCl(g)的∆H=
(4)①2O2(g)+N2(g)=N2O4(l) ∆H1
②N2(g)+2H2(g)=N2H4(l) ∆H2
③O2(g)+2H2(g)=2H2O(g) ∆H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ∆H4
上述反应热效应之间的关系式为∆H4=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学反应过程中发生物质变化的同时,常常伴有能量的变化。
(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 ,两步反应的能量变化示意图如图。
,两步反应的能量变化示意图如图。

①第一步反应是___________ (填“放热”或“吸热”)反应。
② 全部氧化成
全部氧化成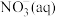 热化学方程式为
热化学方程式为___________ 。
(2)已知红磷比白磷稳定,且有反应:





___________  (填写“>”、“<”或“=”)。
(填写“>”、“<”或“=”)。
(3)研究表明,化学反应能量变化与键能有关。下列是部分化学键的键能数据。
已知:
 ,白磷(
,白磷( )及
)及 的结构如图,则x=
的结构如图,则x=___________ 。

(4)取 溶液与
溶液与 硫酸置于如图所示的简易量热计装置中进行中和反应反应热的测定实验,回答下列问题:
硫酸置于如图所示的简易量热计装置中进行中和反应反应热的测定实验,回答下列问题:

①图中简易量热计装置中缺少的仪器的名称为___________ 。
②分析下列因素会导致测得的中和反应反应热( )的数值变化情况。
)的数值变化情况。
a.量取硫酸时仰视读数:___________ 。(填“偏大”、“偏小”或“无影响”,下同)
b.测定KOH溶液温度的温度计未洗涤直接用于测定硫酸的温度:___________ 。
(1)在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 ,两步反应的能量变化示意图如图。
,两步反应的能量变化示意图如图。
①第一步反应是
②
 全部氧化成
全部氧化成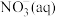 热化学方程式为
热化学方程式为(2)已知红磷比白磷稳定,且有反应:





 (填写“>”、“<”或“=”)。
(填写“>”、“<”或“=”)。(3)研究表明,化学反应能量变化与键能有关。下列是部分化学键的键能数据。
| 化学键 |  |  |  | 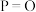 |
键能( ) ) | 197 | 360 | 499 | x |

 ,白磷(
,白磷( )及
)及 的结构如图,则x=
的结构如图,则x=
(4)取
 溶液与
溶液与 硫酸置于如图所示的简易量热计装置中进行中和反应反应热的测定实验,回答下列问题:
硫酸置于如图所示的简易量热计装置中进行中和反应反应热的测定实验,回答下列问题:
①图中简易量热计装置中缺少的仪器的名称为
②分析下列因素会导致测得的中和反应反应热(
 )的数值变化情况。
)的数值变化情况。a.量取硫酸时仰视读数:
b.测定KOH溶液温度的温度计未洗涤直接用于测定硫酸的温度:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据下列两个热化学方程式,回答下列问题:
2H2(g)+O2(g)=2H2O(1) ΔH=−571.6 kJ · mol−1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=−2 220 kJ · mol−1
(1)H2的燃烧热为_______ ,C3H8的燃烧热为_______ 。
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为______________ 。
2H2(g)+O2(g)=2H2O(1) ΔH=−571.6 kJ · mol−1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=−2 220 kJ · mol−1
(1)H2的燃烧热为
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:
①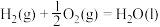
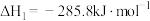
②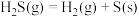
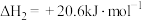
③

请回答下列问题:
(1)反应物的总能量大于生成物的总能量的是_____________ (填标号)。
(2)表示硫化氢的燃烧热的热化学方程式为____________________________________ 。
(3)常温下,将 由
由 和
和 组成的混合气体在足量氧气中充分燃烧,共放出
组成的混合气体在足量氧气中充分燃烧,共放出 的热量。
的热量。
①混合气体中 和
和 的物质的量之比为
的物质的量之比为______ 。
②混合气体中 完全燃烧放出的热量为
完全燃烧放出的热量为______  。若用
。若用 溶液完全吸收生成的
溶液完全吸收生成的 ,则消耗
,则消耗 的物质的量为
的物质的量为_________  ~
~___  。
。
①
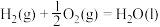
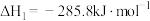
②
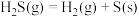
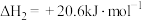
③


请回答下列问题:
(1)反应物的总能量大于生成物的总能量的是
(2)表示硫化氢的燃烧热的热化学方程式为
(3)常温下,将
 由
由 和
和 组成的混合气体在足量氧气中充分燃烧,共放出
组成的混合气体在足量氧气中充分燃烧,共放出 的热量。
的热量。①混合气体中
 和
和 的物质的量之比为
的物质的量之比为②混合气体中
 完全燃烧放出的热量为
完全燃烧放出的热量为 。若用
。若用 溶液完全吸收生成的
溶液完全吸收生成的 ,则消耗
,则消耗 的物质的量为
的物质的量为 ~
~ 。
。
您最近一年使用:0次

 和液态水时,放出的热量为QkJ。经测定,将生成的
和液态水时,放出的热量为QkJ。经测定,将生成的

