常见的可拆分物质有:
(1)强酸:___________ 。
(2)强碱:___________ 。
(3)可溶性盐:___________ 。
(4)浓盐酸、浓硝酸在离子方程式中___________ ,浓硫酸___________ 。
(1)强酸:
(2)强碱:
(3)可溶性盐:
(4)浓盐酸、浓硝酸在离子方程式中
2023高一上·全国·专题练习 查看更多[2]
更新时间:2023-07-20 17:20:54
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有下列物质:①CuSO4·5H2O ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦蔗糖 ⑧熔融氯化钠。请回答下列问题:
(1)可以导电的有_______ (填序号)。
(2)属于电解质的有_____ (填序号)。
(3)属于非电解质的有________ (填序号)。
(4)②在水中的电离方程式为___________ 。
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在水中的电离方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)下列说法中正确的是______ 。
A.NaCl溶液导电,所以NaCl溶液是电解质;
B.固体NaCl不导电,但NaCl是电解质;
C.Cu能导电,所以Cu是电解质;
D.SO2溶于水能导电,所以SO2是电解质;
E.BaSO4的水溶液不导电,所以BaSO4是非电解质;
F.酒精不导电,所以酒精是非电解质。
(2)下列各组物质按组成规律不同分类,请找出与其他种类不同的物质。
①HCl、H2SO4、H2CO3、HNO3:______ ;
②溶液、水、浊液、胶体:______ ;
③Na2CO3、NaNO3、KNO3、Na2SO4:______ 。
A.NaCl溶液导电,所以NaCl溶液是电解质;
B.固体NaCl不导电,但NaCl是电解质;
C.Cu能导电,所以Cu是电解质;
D.SO2溶于水能导电,所以SO2是电解质;
E.BaSO4的水溶液不导电,所以BaSO4是非电解质;
F.酒精不导电,所以酒精是非电解质。
(2)下列各组物质按组成规律不同分类,请找出与其他种类不同的物质。
①HCl、H2SO4、H2CO3、HNO3:
②溶液、水、浊液、胶体:
③Na2CO3、NaNO3、KNO3、Na2SO4:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列反应的离子方程式。
(1)铜与硝酸银溶液反应:___ 。
(2)盐酸除铁锈:___ 。
(3)澄清石灰水中加入稀硫酸:___ 。
(4)将硝酸滴到CuO固体上:___ 。
(5)硫酸镁溶液与烧碱溶液混合:___ 。
(6)NaHCO3与KOH两溶液混合:___ 。
(1)铜与硝酸银溶液反应:
(2)盐酸除铁锈:
(3)澄清石灰水中加入稀硫酸:
(4)将硝酸滴到CuO固体上:
(5)硫酸镁溶液与烧碱溶液混合:
(6)NaHCO3与KOH两溶液混合:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。CrO 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是___________ (填字母)。
a.都不稳定,密封放置沉淀 b.两者均有丁达尔效应 c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mLNa2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明Na2SO4中硫酸根离子能够透过半透膜:___________ 。
(4)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到某溶液,用此溶液进行以下实验:
①取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为___________ 。
②在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,制得的分散系为___________ 。除去该分散系中混有的FeCl3和HCl的方法是___________ 。
③向②中所制备的分散系中逐滴加入稀硫酸,实验现象是___________ 。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀 b.两者均有丁达尔效应 c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mLNa2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明Na2SO4中硫酸根离子能够透过半透膜:
(4)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到某溶液,用此溶液进行以下实验:
①取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为
②在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,制得的分散系为
③向②中所制备的分散系中逐滴加入稀硫酸,实验现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求填空
(1)写出下列物质的电离方程式。
①碳酸氢钠___________
②氯化铁___________
(2)利用锌渣(主要成分是Zn和FeSO4)制备氯化锌的主要工艺流程如下:
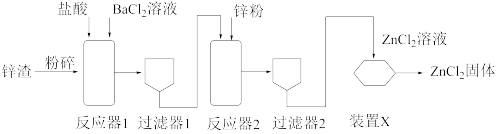
反应器1中的主要反应有:ⅰ.BaCl2+FeSO4=FeCl2+BaSO4↓ⅱ.Zn+FeSO4=ZnSO4+Fe ⅲ.Zn+2HCl=ZnCl2+H2↑
①反应ⅰ属于基本反应类型中的___________ 反应
②反应___________ 属于氧化还原反应
(3)完成下列离子方程式。
①钠和氯化钾溶液反应___________
②铁与稀硫酸反应___________
③碳酸氢钠溶液中加入氢氧化钠溶液___________
④氢氧化钡和硫酸铵溶液反应___________
(1)写出下列物质的电离方程式。
①碳酸氢钠
②氯化铁
(2)利用锌渣(主要成分是Zn和FeSO4)制备氯化锌的主要工艺流程如下:

反应器1中的主要反应有:ⅰ.BaCl2+FeSO4=FeCl2+BaSO4↓ⅱ.Zn+FeSO4=ZnSO4+Fe ⅲ.Zn+2HCl=ZnCl2+H2↑
①反应ⅰ属于基本反应类型中的
②反应
(3)完成下列离子方程式。
①钠和氯化钾溶液反应
②铁与稀硫酸反应
③碳酸氢钠溶液中加入氢氧化钠溶液
④氢氧化钡和硫酸铵溶液反应
您最近一年使用:0次



