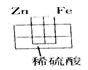
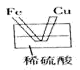
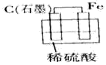
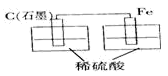
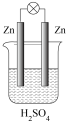
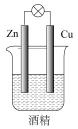
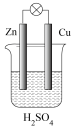
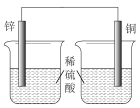
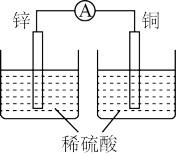
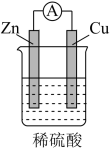
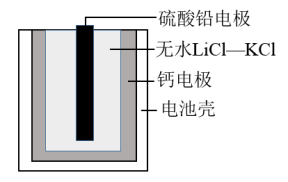
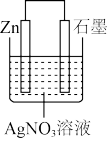某小组进行了如下两组对比实验,下列说法正确的是
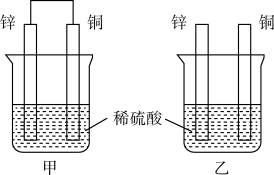

| A.甲烧杯中外电路的电子由铜流向锌 |
B.两烧杯中溶液的 均增大 均增大 |
| C.乙中产生气泡的速率比甲快 |
| D.都能够观察到锌片溶解,铜片表面产生气泡 |
更新时间:2023-07-12 07:12:46
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列判断正确的是
| A.放热反应一定可以设计成原电池 | B.锌锰干电池中碳棒是负极,锌片是正极 |
| C.燃料电池的能量转化率可达到100% | D.充电是使放电时的氧化还原反应逆向进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】我国科学家在天然气脱硫研究方面取得了新进展,其原理如图所示。下列有关说法错误的是( )


| A.图中导线上标记方向为电子流向 |
| B.装置中H+向甲池迁移 |
| C.正极上的电极反应式为O2+4H++4e-=2H2O |
| D.乙池溶液中发生反应的离子方程式:H2S+I3- =3I-+S↓+2H+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】用下图装置探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积,记录实验数据如下表:
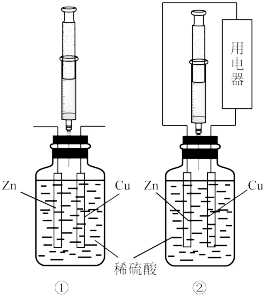
下列说法不正确的是

| 实验 数据 时间/min | ① | ② | ||
| 气体体积/mL | 溶液温度/℃ | 气体体积/mL | 溶液温度/℃ | |
| 0 | 0 | 22.0 | 0 | 22.0 |
| 8.5 | 30 | 24.8 | 50 | 23.8 |
| 10.5 | 50 | 26.0 | — | — |
| A.装置中锌片质量均减轻,发生氧化反应 |
| B.0~8.5 min,生成气体的平均速率①<② |
| C.0~8.5 min,反应①释放的总能量更多 |
| D.根据上述实验可知②中化学能除了转化为电能,也有转化为热能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】关于如图装置的叙述,正确的是
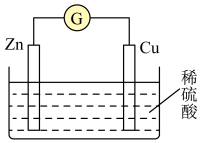

| A.锌是负极,铜片质量逐渐减少 |
| B.电流从锌片经导线流向铜片 |
| C.工作一段时间后,电解质溶液的质量增加 |
| D.氢离子在铜片表面被氧化后生成H2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】某同学设计了如图所示的原电池,发现一开始电流计指针偏向铝极,随后又转而偏向镁极。下列说法错误 的是


| A.镁始终作负极,发生氧化反应 |
| B.最终铝电极逐渐溶解,镁电极表面出现大量气泡 |
| C.电流计指针偏转方向改变后,溶液中OH-流向铝电极 |
D.铝电极的电极反应式: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】《Science》杂志报道了王浩天教授团队发明的制取H2O2的绿色方法,原理如图所示。下列说法正确的是
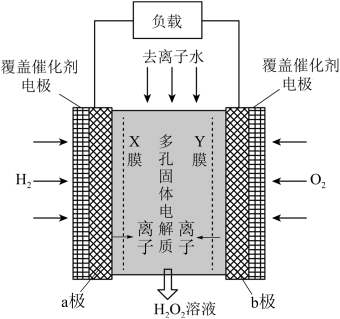

| A.a极为正极,发生还原反应 |
| B.X膜为阳离子交换膜 |
| C.当外电路通过2mol e-时,消耗22.4L O2 |
| D.该装置可实现化学能与电能间的完全转化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】把金属M放入盐N(NO)3溶液中,发生如下反应:M+N2+== M2++N,以下叙述正确的是( )
| A.常温下金属M和N有可能跟水反应 |
| B.M和N用导线连接放入稀H2SO4中,一定构成原电池,且N极上有H2放出 |
| C.M和N用导线连接并平行放入N(NO3)2溶液中,一定构成原电池 |
| D.由M和N构成的原电池,M一定是负极,且N上一定产生H2 |
您最近一年使用:0次