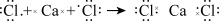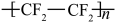某盐的化学式为X3YZ6,已知X、Y、Z均为短周期元素,X、Y位于同一周期,且均为金属元素;Z为非金属元素,其单质与 混合,在暗处即可发生爆炸;Y的最高价氧化物的水化物能与NaOH溶液反应。下列说法正确的是
混合,在暗处即可发生爆炸;Y的最高价氧化物的水化物能与NaOH溶液反应。下列说法正确的是
 混合,在暗处即可发生爆炸;Y的最高价氧化物的水化物能与NaOH溶液反应。下列说法正确的是
混合,在暗处即可发生爆炸;Y的最高价氧化物的水化物能与NaOH溶液反应。下列说法正确的是A.简单离子半径: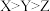 |
| B.X与氧元素形成的化合物中可能存在共价键 |
| C.Z元素的常见价态有-1和+7 |
| D.工业上电解Y的氯化物制备Y的单质 |
更新时间:2023-07-14 13:24:26
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】已知 、
、 、
、 、
、 的原子序数都不超过18,它们的离子
的原子序数都不超过18,它们的离子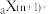 、
、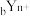 、
、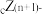 、
、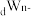 具有相同的电子层结构。则下列说法正确的是
具有相同的电子层结构。则下列说法正确的是
 、
、 、
、 、
、 的原子序数都不超过18,它们的离子
的原子序数都不超过18,它们的离子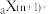 、
、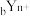 、
、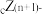 、
、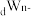 具有相同的电子层结构。则下列说法正确的是
具有相同的电子层结构。则下列说法正确的是| A.原子序数:a>b>c>d |
B.离子半径: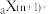 > >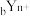 > >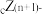 > >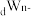 |
C.离子的氧化性: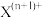 > >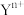 |
| D.单质的氧化性:Z>W |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】W、X、Y、Z是4种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和氖原子的核外电子数相差1;Y的单质是一种常见的半导体材料:Z的非金属性在同周期元素中最强,下列说法不正确的是


| A.对应简单离子半径:X>W |
| B.对应气态氢化物的稳定性:Z>Y |
| C.X的金属性是同周期中最强的 |
| D.Y的氧化物能与X的最高价氧化物对应的水化物反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法中不正确的是
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C.NaCl中所有的原子均为8电子稳定结构 |
D.熔融的NaHSO4发生NaHSO4=Na++HSO ,此时破坏的只有离子键 ,此时破坏的只有离子键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列观点正确的是
| A.H2O2中只存在极性键 |
| B.在氧化钠中,只存在氧离子和钠离子的静电吸引作用 |
| C.某化合物熔融态能导电,该化合物中一定有离子键 |
| D.Na2O和Na2O2所含化学键类型完全相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列金属中,工业上常用热分解法冶炼的是( )
| A.镁 | B.钾 | C.铁 | D.银 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】电化学在生产中有广泛的应用。下列说法正确的是
| A.工业冶炼金属铝,常采用电解熔融的氯化铝的方法 |
| B.电解精炼铜时,用粗铜作阴极 |
| C.在镀件上镀银时可用纯银作阳极 |
| D.铜的电解精炼时,粗铜中含有的杂质锌、金、银等金属在阳极沉降下来形成阳极泥 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】H2O2是一种“绿色”试剂,许多物质都会使较高浓度的H2O2溶液发生催化分解。实验发现向H2O2溶液中加入Br2(Br2的化学性质与Cl2相似)可以加快其分解速率。有人提出反应机理可能有2步,第1步反应为:H2O2+Br2=2H++O2↑+2Br-。下列说法正确的是
| A.H2O2中氧元素的化合价为-2 |
| B.机理中第2步反应为:2H++H2O2+2Br-=2H2O+Br2 |
| C.在第1步反应中,每生成0.1molO2,转移0.4mol电子 |
| D.若在加入Br2的H2O2溶液中检出Br-,则说明第1步反应发生了 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】化学与生活、生产、社会可持续发展密切相关。下列说法错误的是
| A.制作N95型口罩的核心材料是聚丙烯,属于有机高分子材料 |
B.聚合硫酸铁[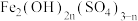 ](n<1)是新型絮凝剂,其中Fe呈+3价 ](n<1)是新型絮凝剂,其中Fe呈+3价 |
| C.用聚氯乙烯代替木材,生产快餐盒,以减少木材的使用 |
| D.地沟油经过加工处理后可用来制生物柴油和肥皂 |
您最近一年使用:0次

 中中心原子的价层电子对数为4
中中心原子的价层电子对数为4