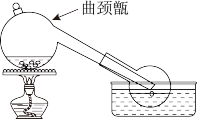
实验室常利用难挥发性酸制备易挥发性酸的原理,用浓硫酸与硝石(NaNO3)反应制备HNO3反应装置如图,下列说法不正确的是
| A.可从实验室中选无色透明洁净的试剂瓶盛装制得的硝酸 |
B.反应方程式为: |
| C.反应温度如果过高,制得HNO3可能会呈现黄色 |
| D.曲颈甑不适宜制备沸点过低的物质 |
更新时间:2023-06-08 16:35:27
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】下列实验过程中,始终无明显现象的是
| A.将NO2通入FeSO4溶液中 |
| B.将CO2通入BaCl2溶液中 |
| C.将NH3通入AlCl3溶液中 |
| D.将SO2通入已酸化的Ba(NO3)2溶液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】为测定Cu和Cu2O混合粉末中Cu的含量。某同学将44.8g Cu和Cu2O混合粉末加入500mL 4.5mol/L的稀硝酸中,得到6.72LNO(标准状况下),忽略溶液体积的变化。下列说法正确的是
| A.反应后有固体剩余 | B.混合粉末中Cu的质量分数约为37% |
| C.反应后的溶液中c(Cu2+)=1.2mol/L | D.在反应后的溶液中加入足量铁粉,可置换出41.6g Cu |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】化学小组同学探究铜与过量浓硝酸反应后溶液呈绿色的原因。
资料:ⅰ.铜与浓硝酸反应过程中可生成 ,
, 易分解产生无色气体。
易分解产生无色气体。
ⅱ. 是一种弱酸。
是一种弱酸。 电离出
电离出 ,
, 与
与 发生如下反应:
发生如下反应: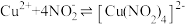 (绿色)
(绿色)
下列说法不正确 的是
资料:ⅰ.铜与浓硝酸反应过程中可生成
 ,
, 易分解产生无色气体。
易分解产生无色气体。ⅱ.
 是一种弱酸。
是一种弱酸。 电离出
电离出 ,
, 与
与 发生如下反应:
发生如下反应: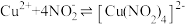 (绿色)
(绿色)| 编号 | 操作 | 现象 |
| ① | 分别向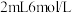  和 和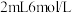  溶液中通入稳定的 溶液中通入稳定的 气流 气流 |  溶液变黄 溶液变黄 溶液不变黄 溶液不变黄 |
| ② | 将实验①的黄色溶液与蓝色 溶液混合 溶液混合 | 溶液呈绿色 |
| ③ | 将  溶液与 溶液与  溶液混合 溶液混合 | 溶液呈绿色 |
| ④ | 向实验③所得溶液中加入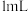 浓硝酸 浓硝酸 | 溶液变蓝 |
A.依据实验①,向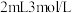  通入稳定的 通入稳定的 气流,溶液可能会变黄 气流,溶液可能会变黄 |
B.实验④加入浓硝酸后可能发生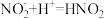 ,使 ,使 浓度下降,绿色消失 浓度下降,绿色消失 |
C.铜与过量浓硝酸反应溶液呈绿色可能原因是:浓硝酸中溶解了生成的 呈黄色,黄色与蓝色叠加呈绿色 呈黄色,黄色与蓝色叠加呈绿色 |
D.铜与过量浓硝酸反应溶液呈绿色可能原因是:铜与浓硝酸反应过程中,生成 使溶液呈绿色 使溶液呈绿色 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】实验室中利用洁净的铜片和浓硫酸进行如下实验,经检测所得固体中含有 和白色物质X,下列说法正确的是
和白色物质X,下列说法正确的是

 和白色物质X,下列说法正确的是
和白色物质X,下列说法正确的是
| A.X溶液显无色 |
| B.NO和Y均为还原产物 |
| C.3molCu参与反应,转移6mol电子 |
| D.若稀硫酸足量,在溶解的环节中至少需要0.8mol的稀硝酸 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将一定量的锌放入200 mL 18.4 mol·L 浓硫酸中加热,充分反应后锌完全溶解,同时生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液
浓硫酸中加热,充分反应后锌完全溶解,同时生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液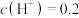 mol·L
mol·L ,则下列判断错误的是
,则下列判断错误的是
 浓硫酸中加热,充分反应后锌完全溶解,同时生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液
浓硫酸中加热,充分反应后锌完全溶解,同时生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液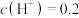 mol·L
mol·L ,则下列判断错误的是
,则下列判断错误的是A.气体X为 和 和 的混合物 的混合物 | B.反应中共转移4 mol电子 |
C.气体X中 和 和 的体积比为4∶1 的体积比为4∶1 | D.反应中共消耗Zn 65 g |
您最近一年使用:0次
单选题
|
较难
(0.4)
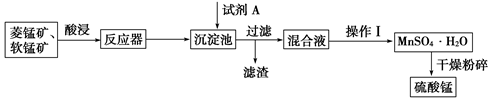
【推荐1】硫酸锰可用于饮料营养强氧化剂和媒染剂。其生产原材料软锰矿(MnO2)、菱锰矿(MnCO3)中常混有硫酸亚铁和硫酸镁等杂质,生产工艺流程如图所示:
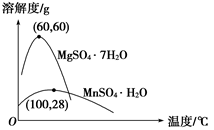
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图所示。
(2)各离子完全沉淀的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6。下列判断正确的是
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图所示。
(2)各离子完全沉淀的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6。下列判断正确的是
| A.试剂A应该选择H2O2,目的是将Fe2+氧化为Fe3+ |
| B.试剂A应该选择氨水,目的是调节溶液的pH |
| C.操作Ⅰ包括蒸发浓缩、冷却结晶、趁热过滤、洗涤等步骤,洗涤时可用稀硫酸作洗涤液 |
| D.通过操作Ⅰ得到MnSO4·H2O的过程中,包括蒸发结晶,在蒸发结晶时,温度应该高于60 ℃ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】高铁酸钾 (K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42- +3Cl-+5H2O,干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑ 下列有关说法不正确的是
| A.低温下,高铁酸钾的溶解度比高铁酸钠更小 |
| B.湿法制备中每生成1mol Na2FeO4 转移3mol电子 |
| C.干法制备中还原剂与氧化剂的物质的量之比为1:3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
您最近一年使用:0次


 2CuO+TeO2,滤渣中TeO2溶于稀硫酸发生的反应为TeO2+H2SO4====TeOSO4+H2O。
2CuO+TeO2,滤渣中TeO2溶于稀硫酸发生的反应为TeO2+H2SO4====TeOSO4+H2O。

