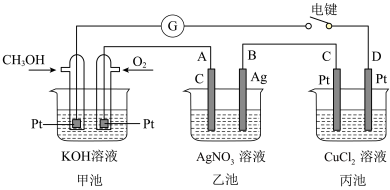
某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。
请回答下列问题:
(1)通入 电极的电极反应式为
电极的电极反应式为_______ 。
(2)乙池中A(石墨)电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),乙池总反应式为_______ 。
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗 的体积为
的体积为_______ mL(标准状况下),丙池中_______ 极析出_______ g铜。
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将_______ (填“增大”“减小”或“不变”;丙中溶液的pH将_______ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)通入
 电极的电极反应式为
电极的电极反应式为(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗
 的体积为
的体积为(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将
更新时间:2023-06-30 15:22:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某科研小组设计利用甲醇(CH3OH)燃料电池(酸性溶液作离子导体),模拟工业电镀、精炼和海水淡化的装置如图。
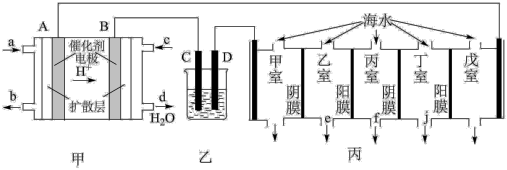
(1)甲装置中c口通入的气体是___________ ,A电极的电极反应式为___________ 。
(2)乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极C是___________ (填“粗铜”或“纯铜”),工作一段时间后,电解质CuSO4溶液的浓度将___________ (填“增大”“减小”或“不变”)。
②若用于电镀金属银,则电镀液宜使用___________ 溶液,镀件是___________ (填“C”或“D”)。
(3)电渗析法是海水淡化的常用方法,某地海水中主要离子的含量如表,现利用“电渗析法”进行淡化,技术原理如图丙所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。
①淡化过程中在___________ 室中易形成水垢[主要成分CaCO3和Mg(OH)2],该室中除发生电极反应外,还发生反应的离子方程式为___________ 。
②产生淡水的出水口为___________ (选填“e”、“f”、“j”)。
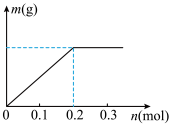
(4)若乙装置中C,D都是惰性电极,溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是___________ 。

(1)甲装置中c口通入的气体是
(2)乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极C是
②若用于电镀金属银,则电镀液宜使用
(3)电渗析法是海水淡化的常用方法,某地海水中主要离子的含量如表,现利用“电渗析法”进行淡化,技术原理如图丙所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。
| 离子 | Na+ | K+ | Ca2+ | Mg2+ | Cl- |  |  |
| 含量/mg•L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |
②产生淡水的出水口为
(4)若乙装置中C,D都是惰性电极,溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、 和
和 )在催化剂的作用下合成甲醇(
)在催化剂的作用下合成甲醇( )是其中的一个研究项目。该研究发生的主要反应如下:
)是其中的一个研究项目。该研究发生的主要反应如下:
I.CO与 反应合成甲醇:
反应合成甲醇: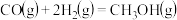
II. 与
与 反应合成甲醇:
反应合成甲醇: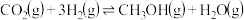
(1)上述反应符合原子经济性的是反应_______ (I或II)。
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是_______。
(3)将2mol 和1molCO充入温度恒定、体积为2L的恒容装置中,充分反应10min达到平衡状态。
和1molCO充入温度恒定、体积为2L的恒容装置中,充分反应10min达到平衡状态。
①下列事实能说明该反应达到平衡状态的是_______ (填字母)。
A.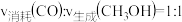
B.容器中混合气体的总压强不再变化
C.容器中混合气体的平均摩尔质量不再变化
D.容器中CO和 的体积分数之比不再变化
的体积分数之比不再变化
E.2molH-H断裂的同时消耗1mol
②测得平衡混合物中 的体积分数为50%,则0~10min内,
的体积分数为50%,则0~10min内,
_______  ,反应体系开始时的压强与平衡时的压强之比为
,反应体系开始时的压强与平衡时的压强之比为_______ 。
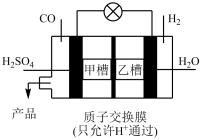
(4)科学家正在研发让该反应在常温常压下进行的原电池装置,如图所示。写出甲槽的电极反应式_______ 。电池工作过程中 通过质子膜向
通过质子膜向_______ (填“左”或者“右”)移动。
 和
和 )在催化剂的作用下合成甲醇(
)在催化剂的作用下合成甲醇( )是其中的一个研究项目。该研究发生的主要反应如下:
)是其中的一个研究项目。该研究发生的主要反应如下:I.CO与
 反应合成甲醇:
反应合成甲醇: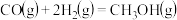
II.
 与
与 反应合成甲醇:
反应合成甲醇: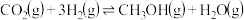
(1)上述反应符合原子经济性的是反应
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是_______。
| A.恒温恒容下,再充入CO | B.升高温度 |
| C.恒温恒容下,向其中充入Ar | D.恒温恒压下,向其中充入Ar |
 和1molCO充入温度恒定、体积为2L的恒容装置中,充分反应10min达到平衡状态。
和1molCO充入温度恒定、体积为2L的恒容装置中,充分反应10min达到平衡状态。①下列事实能说明该反应达到平衡状态的是
A.
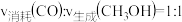
B.容器中混合气体的总压强不再变化
C.容器中混合气体的平均摩尔质量不再变化
D.容器中CO和
 的体积分数之比不再变化
的体积分数之比不再变化E.2molH-H断裂的同时消耗1mol

②测得平衡混合物中
 的体积分数为50%,则0~10min内,
的体积分数为50%,则0~10min内,
 ,反应体系开始时的压强与平衡时的压强之比为
,反应体系开始时的压强与平衡时的压强之比为(4)科学家正在研发让该反应在常温常压下进行的原电池装置,如图所示。写出甲槽的电极反应式
 通过质子膜向
通过质子膜向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)依据反应:Cu2++Zn(s)=Zn2+(aq)+Cu(s)设计的原电池如下图甲所示。
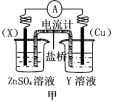
①电极X的材料是___________ ;Y溶液可以是___________ 。
②Cu电极上发生的电极反应式是___________ 。
③电池放电时,电子从___________ 电极经电流计流向___________ 电极。(填电极材料)
④电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向ZnSO4溶液一端扩散的离子是___________ 。(填离子符号)
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防腐。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:___________ 。
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案:
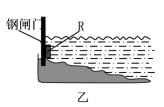
其中连接在铁闸门上的固体材料R可以采用___________ (填写字母序号)。
A.铜 B.钠 C.锌 D.石墨
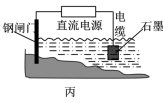
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则石墨应连接直流电源的___________ 极。

①电极X的材料是
②Cu电极上发生的电极反应式是
③电池放电时,电子从
④电池放电过程中,盛有饱和KCl琼脂溶胶的盐桥中,向ZnSO4溶液一端扩散的离子是
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防腐。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图乙所示的方案:

其中连接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
③图丙所示方案也可以减缓铁闸门的腐蚀速率,则石墨应连接直流电源的

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化和还原是认识物质性质、分析化学变化的重要视角之一,对生产、生活乃至生命活动中有着十分重要的作用。
(1)下列物质间的转化,需要加入氧化剂才能实现的是_____。
(2)下列溶液中的离子因发生氧化还原反应而不能大量共存的是_____。
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2
①配平下列化学方程式并标出电子转移方向和个数。_____
_____NaIO3+_____NaHSO3—_____I2+_____Na2SO4+_____H2SO4+_____H2O
②在该反应中NaHSO3体现_____ (填“氧化性”或“还原性”),I2为_____ (填“氧化产物”或“还原产物”)。
③已知: 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
_____ I-(填“>”或“<”),写出该反应的化学方程式_____ 。
化学能与电能之间的转化,是能量转化的重要形式之一,对于生产与生活有很多。

(4)汽车的启动电源常用铅酸蓄电池。其结构如图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O。根据此反应判断下列叙述中正确的是_____。
(5)港珠澳大桥设计寿命120年,对桥体钢构件采用了多种防腐方法。下列分析错误的是_____。
(6)用如图装置可以模拟铁的电化学防护,下列说法不正确的是_____。

(7)如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少
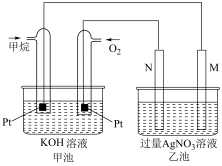
①甲池中通入乙醇的铂电极名称是_____ (选填“正极”、“负极”、“阴极”、“阳极”),通入O2的铂电极反应式为_____ 。
②乙池属于_____ (填“原电池”或“电解池”),工作时,乙池中电子流出的电极是_____ (选填“M”或N”);
③若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为_____ L(标况下);
④若用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是_____ (选填“粗铜”或“精铜”),反应一段时间以后,电解液溶液的浓度_____ 。(选填“增大”、“减小”“不变”)
(1)下列物质间的转化,需要加入氧化剂才能实现的是_____。
| A.NH3→NO | B.Fe2O3→Fe |
| C.KClO3→Cl2 | D.H2SO4→SO2 |
(2)下列溶液中的离子因发生氧化还原反应而不能大量共存的是_____。
A.Fe2+、H+、 、 、 |
B.Cu2+、Al3+、 、Cl- 、Cl- |
C.K+、Al3+、OH-、 |
D.Ba2+、Na+、 、ClO- 、ClO- |
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2
①配平下列化学方程式并标出电子转移方向和个数。
_____NaIO3+_____NaHSO3—_____I2+_____Na2SO4+_____H2SO4+_____H2O
②在该反应中NaHSO3体现
③已知:
 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
化学能与电能之间的转化,是能量转化的重要形式之一,对于生产与生活有很多。

(4)汽车的启动电源常用铅酸蓄电池。其结构如图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O。根据此反应判断下列叙述中正确的是_____。
| A.PbO2是电池的负极 |
| B.Pb是负极 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
(5)港珠澳大桥设计寿命120年,对桥体钢构件采用了多种防腐方法。下列分析错误的是_____。
| A.防腐原理主要是避免发生反应:2Fe+O2+2H2O=2Fe(OH)2 |
| B.钢构件表面喷涂环氧树脂涂层,是为了隔绝空气、水等防止形成原电池 |
| C.采用外加电流的阴极保护时需外接镁、锌等作辅助阳极 |
| D.钢构件可采用不锈钢材料以减缓电化学腐蚀 |
(6)用如图装置可以模拟铁的电化学防护,下列说法不正确的是_____。

| A.若X为碳棒,开关K置于A处时,铁电极反应2H2O+2e-=H2+2OH- |
| B.若X为碳棒,开关K置于A处可以减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| D.若X为锌棒,开关K置于B处时,铁电极反应为2H++2e-=H2 |
(7)如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少

①甲池中通入乙醇的铂电极名称是
②乙池属于
③若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为
④若用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示是用石墨和铁作电极电解饱和食盐水的装置,请填空:

(1)X的电极反应式为:___________________________________ ,Y极的电极材料是_______________ 。
(2)某同学在实验时误将两种电极材料接反,导致X极上未收集到预期产物,一段时间后又将两极的连接方式纠正过来,发现X极附近出现了白色沉淀,此沉淀是________ (填化学式),其形成原因是:___________________________________ 。

(3)工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是_____________ ,阳极室(A处)加入________ ,离子交换膜只许________ 通过。

(1)X的电极反应式为:
(2)某同学在实验时误将两种电极材料接反,导致X极上未收集到预期产物,一段时间后又将两极的连接方式纠正过来,发现X极附近出现了白色沉淀,此沉淀是

(3)工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是石墨电极。当将电源接通后,向乙中滴入酚酞试液,发现在F极附近溶液显红色。按要求回答下列问题:

(1)电极F的名称是__ ,电源B极的名称是__ 。
(2)甲装置中C电极的电极反应式是__ ;D电极的电极反应式是__ 。
(3)乙装置中电解反应的总化学方程式__ 。
(4)欲使丙装置发生:2Ag+2HCl=2AgCl+H2↑反应,则G电极的材料应是__ (填化学式)。
(5)丁装置中装有Fe(OH)3胶体,一段时间后胶体颜色变深的电极是:__ (填字母)。

(1)电极F的名称是
(2)甲装置中C电极的电极反应式是
(3)乙装置中电解反应的总化学方程式
(4)欲使丙装置发生:2Ag+2HCl=2AgCl+H2↑反应,则G电极的材料应是
(5)丁装置中装有Fe(OH)3胶体,一段时间后胶体颜色变深的电极是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解是一种非常强有力的促进氧化还原反应的手段,许多很难进行的氧化还原反应,都可以通过电解来实现。
(1)工业上常以石墨做电极,电解NaCl水溶液时,阴极区产物有____ ,其溶液可用于吸收工业尾气中的SO2,写出反应的化学方程式_____ 。
(2)电解NaCl水溶液时,用盐酸控制阳极区溶液的pH在2~3,用平衡移动原理解释盐酸的作用_____ 。离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液时,可在钢制品上发生电镀,有铝产生。
(3)铝原子的核外电子排布式是____ ,其中有____ 种不同能级的电子。
(4)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当所得还原产物为6g时,转移电子的物质的量为___ mol。
(5)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有____ (填编号)。
a.KClO3 b.Mg c.MnO2 d.KCl
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,不能说明固体混合物中无Fe2O3,理由是________ (用离子方程式说明)。
(1)工业上常以石墨做电极,电解NaCl水溶液时,阴极区产物有
(2)电解NaCl水溶液时,用盐酸控制阳极区溶液的pH在2~3,用平衡移动原理解释盐酸的作用
(3)铝原子的核外电子排布式是
(4)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当所得还原产物为6g时,转移电子的物质的量为
(5)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a.KClO3 b.Mg c.MnO2 d.KCl
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,不能说明固体混合物中无Fe2O3,理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO +2H+
+2H+ Cr2O
Cr2O +H2O)。
+H2O)。

(1)阳极的电极反应式为____ 。
(2)电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为____ mol。
 +2H+
+2H+ Cr2O
Cr2O +H2O)。
+H2O)。
(1)阳极的电极反应式为
(2)电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题。
(1)某同学设计了一个甲醚 燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题:
燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题:_____ 。
②乙装置中溶液为500ml,反应一段时间后,乙装置中生成NaOH主要在_____ (填“铁极”或“石墨极”)区,X膜是_____ (填“阳离子交换膜”或“阴离子交换膜”),当消耗标况下 时,乙装置溶液中
时,乙装置溶液中
_____ (忽略溶液体积变化)。
③如果粗铜中含有锌、银等杂质,丙装置中阳极减少的质量_____ 阴极增加的质量(填“大于”“小于”或“等于”)。反应一段时间,硫酸铜溶液浓度将_____ (填“增大”“减小”或“不变”)。
(2)我国科学家采用单原子Ni和纳米Cu作串联催化剂,通过电解法将 转化为乙烯。装置示意图如下。
转化为乙烯。装置示意图如下。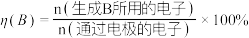
①纳米Cu催化剂上发生反应:_____ ;
②若乙烯的电解效率为60%,电路中通过1mol电子时,电解法将 转化为乙烯的物质的量是
转化为乙烯的物质的量是_____ mol。
(1)某同学设计了一个甲醚
 燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题:
燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题: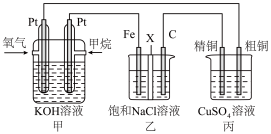
②乙装置中溶液为500ml,反应一段时间后,乙装置中生成NaOH主要在
 时,乙装置溶液中
时,乙装置溶液中
③如果粗铜中含有锌、银等杂质,丙装置中阳极减少的质量
(2)我国科学家采用单原子Ni和纳米Cu作串联催化剂,通过电解法将
 转化为乙烯。装置示意图如下。
转化为乙烯。装置示意图如下。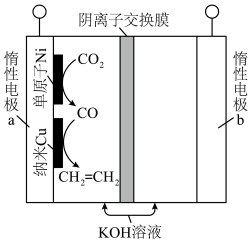
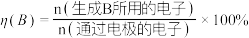
①纳米Cu催化剂上发生反应:
②若乙烯的电解效率为60%,电路中通过1mol电子时,电解法将
 转化为乙烯的物质的量是
转化为乙烯的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学电源在日常生活和工业生产中有着重要的应用。
Ⅰ.如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池负极的电极反应式为_______ 。
(2)C极的电极反应式为_______ 。
(3)若有2.24 L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为_______ L(标准状况下);丙装置中阴极析出铜的质量为_______ g。
Ⅱ.“长征”火箭发射使用的燃料是液态偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的优点是能在短时间内产生巨大能量将火箭送2上太空,且产物不污染空气(产物都是空气的成分)。某校外研究性学习小组拟将此原理设计为原电池,如图2所示,结合学习过的电化学原理分析其设计方案,回答相关问题:

(4)从a口加入_______ (填名称)。H+的移动方向是_______ (填“由A到B”或“由B到A”)。
(5)A极发生的电极反应为_______ 。
(6)若以该电池为电源,用石墨作电极电解200 mL0.5 mol/L的CuSO4溶液,电解一段时间后,两极收集到相同体积(相同条件下)的气体,则整个电解过程转移电子_______ mol,要恢复原溶液可以加入_______ 。
Ⅰ.如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池负极的电极反应式为
(2)C极的电极反应式为
(3)若有2.24 L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为
Ⅱ.“长征”火箭发射使用的燃料是液态偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的优点是能在短时间内产生巨大能量将火箭送2上太空,且产物不污染空气(产物都是空气的成分)。某校外研究性学习小组拟将此原理设计为原电池,如图2所示,结合学习过的电化学原理分析其设计方案,回答相关问题:

(4)从a口加入
(5)A极发生的电极反应为
(6)若以该电池为电源,用石墨作电极电解200 mL0.5 mol/L的CuSO4溶液,电解一段时间后,两极收集到相同体积(相同条件下)的气体,则整个电解过程转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
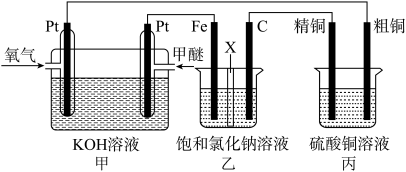
(1)写出甲中负极的电极反应式__ 。
(2)反应一段时间后,乙装置中生成NaOH主要在___ (填“铁极”或“石墨极”)区。
(3)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为___ ,反应一段时间,硫酸铜溶液浓度将___ (填“增大”“减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为___ 。

(1)写出甲中负极的电极反应式
(2)反应一段时间后,乙装置中生成NaOH主要在
(3)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
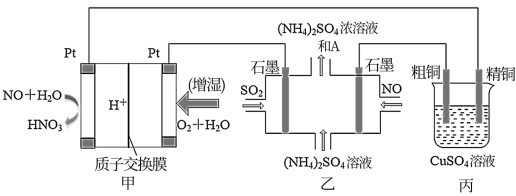
(1)燃料电池放电过程中正极的电极反应式________ 。
(2)乙装置中物质A是________ (填化学式),该装置电解过程阴极的电极反应式________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将________ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有________ mol;丙装置中阴极析出的质量为________ g。
 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
(1)燃料电池放电过程中正极的电极反应式
(2)乙装置中物质A是
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有
您最近一年使用:0次



