下列关于居民生活用的天然气(主要成分为甲烷)燃烧(如图)的说法正确的是

已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=—890.3kJ/mol

已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=—890.3kJ/mol
| A.每进行1mol该反应,有890.3kJ热能转化为化学能 |
| B.甲烷燃烧的过程中存在非极性键的断裂与形成 |
| C.该反应中,反应物的总键能大于生成物的总键能 |
D.当有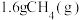 完全燃烧时,放出89.03kJ热量 完全燃烧时,放出89.03kJ热量 |
更新时间:2023-08-04 11:12:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知完全分解1molH2O2放出热量为98kJ,在含有少量I-的溶液中H2O2分解的机理为
反应Ⅰ:H2O2(aq)+I-(aq) IO-(aq)+H2O(l) △H1
IO-(aq)+H2O(l) △H1
反应Ⅱ:H2O2(aq)+IO-(aq) O2(g)+I-(aq)+H2O(l) △H2
O2(g)+I-(aq)+H2O(l) △H2
在一定温度下,其反应过程能量变化如图所示,下列有关该反应的说法不正确的是
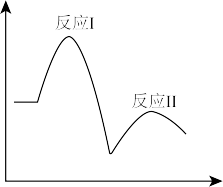
反应Ⅰ:H2O2(aq)+I-(aq)
 IO-(aq)+H2O(l) △H1
IO-(aq)+H2O(l) △H1反应Ⅱ:H2O2(aq)+IO-(aq)
 O2(g)+I-(aq)+H2O(l) △H2
O2(g)+I-(aq)+H2O(l) △H2在一定温度下,其反应过程能量变化如图所示,下列有关该反应的说法不正确的是

| A.反应Ⅱ高温下能自发进行 |
| B.H2O2分解产生氧气的速率是由反应I决定的 |
| C.I-、IO-都是催化剂 |
| D.△H1+△H2=-196kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】研究表明,化学反应的能量变化与反应物和生成物的键能有关。键能可以简单的理解为断开1mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
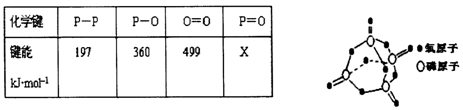
已知白磷的燃烧方程式为:P4(s)+ 5O2=P4O10(s),该反应放出热量2378.0kJ,且白磷分子结构为正四面体,4个磷原子分别位于正四面体的四个顶点,白磷完全燃烧的产物结构如右图所示,则上表中X为

已知白磷的燃烧方程式为:P4(s)+ 5O2=P4O10(s),该反应放出热量2378.0kJ,且白磷分子结构为正四面体,4个磷原子分别位于正四面体的四个顶点,白磷完全燃烧的产物结构如右图所示,则上表中X为
| A.434 | B.335 | C.237 | D.188 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:CH3COOH(aq)+ NaOH(aq)= CH3COONa(aq)+ H2O(1) △H=-Q1kJ/mol
1/2 H2SO4(浓)+ NaOH(aq)=1/2 Na2SO4(aq) + H2O(1) △H=-Q2kJ/mol
HNO3(aq) + KOH(aq)= KNO3(aq) + H2O(1) △H=-Q3kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系为( )
1/2 H2SO4(浓)+ NaOH(aq)=1/2 Na2SO4(aq) + H2O(1) △H=-Q2kJ/mol
HNO3(aq) + KOH(aq)= KNO3(aq) + H2O(1) △H=-Q3kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系为( )
| A.Q2=Q3 > Q1 | B.Q2 > Q1 > Q3 | C.Q2 > Q3 > Q1 | D.Q3 > Q2 > Q1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列描述的反应中产物的总能量高于反应物的总能量的是


A.金属 与稀盐酸的反应 与稀盐酸的反应 | B.高温分解 |
C.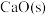 溶于水 溶于水 | D.能量变化如图所示的化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氢气可以在氯气中燃烧,下列说法正确的是
| A.反应在点燃条件下发生,是吸热反应 |
| B.反应中的能量变化与反应物的用量多少无关 |
| C.反应物的总能量高于生成物的总能量 |
| D.化学键断裂吸收的总能量高于化学键形成放出的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是


| A.W、R元素单质分子内都存在非极性键 | B.W4呈正四面体构型,键角为109°28′ |
| C.键长W—H<Y—H,键的极性Y—H>W—H | D.键长X—H<W—H,键能X—H>W—H |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.有机物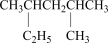 的系统命名为2-甲基-4-乙基戊烷 的系统命名为2-甲基-4-乙基戊烷 |
B.有机物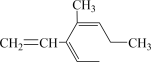 与溴单质按物质的量之比1:1发生加成反应,生成的产物有4种 与溴单质按物质的量之比1:1发生加成反应,生成的产物有4种 |
C.1,3-丁二烯分子中碳原子均采用 杂化方式,碳原子与氢原子形成 杂化方式,碳原子与氢原子形成 键 键 |
D. 和 和 具有相同的官能团,互为同系物 具有相同的官能团,互为同系物 |
您最近一年使用:0次

 2CO(g)
2CO(g)

