铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式: 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、
负极,并写出电极反应式。
正极反应: 。
负极反应: 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤 。
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。有关反应的化学方程式 ; ;劣质不锈钢腐蚀的实验现象 。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式: 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、
负极,并写出电极反应式。
正极反应: 。
负极反应: 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤 。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀 完全时的pH | |
| Fe3+ Fe2+ | 1.9 7.0 | 3.2 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu | ||
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。有关反应的化学方程式 ; ;劣质不锈钢腐蚀的实验现象 。
2011·甘肃天水·一模 查看更多[3]
更新时间:2014-04-10 19:29:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图所示,是原电池的装置图。请回答:

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为_____________ ;反应进行一段时间后溶液C的pH将_____ (填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为____ ,B(正极)极材料为______ ,溶液C为_______ 。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是____ (填“正极”或“负极”),c电极的反应方程式为______________ 。若线路中转移2mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为_____ 。

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请分析下图装置。

⑴Fe电极是_____ (填“正”或“负”)极,其电极反应为________ ;
⑵Cu电极是_____ 电极,其电极反应为________________ 。
⑶若用浓硝酸做电解质溶液____ 做负极。

⑴Fe电极是
⑵Cu电极是
⑶若用浓硝酸做电解质溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.“价-类”二维图是化学研究的重要手段。如图是S元素的常见化合价与部分物质类别的对应关系(G、H均为正盐)。回答下列问题:_____ (填标号)。
A.将D通入 溶液中,溶液中无明显现象,再通入
溶液中,溶液中无明显现象,再通入 ,则溶液中会出现白色沉淀
,则溶液中会出现白色沉淀
B.F的浓溶液能与B反应同时生成A和D
C.将足量的F加入含H的溶液中,可以闻到臭鸡蛋气味
(2)请写出用生石灰除去燃煤产生的D,直接生成G的化学方程式_____ 。
Ⅱ.水是生命之源,也是化学反应中的主角。
关于 的反应,已知断开
的反应,已知断开 键、
键、 键、
键、 键分别需要吸收436kJ、498kJ、463kJ的能量。
键分别需要吸收436kJ、498kJ、463kJ的能量。
(3)若有 生成,需要
生成,需要_____ 。(填“吸收”或“放出”)热量_____ kJ。
(4)化学反应过程中伴随着能量变化,下列变化中属于吸热反应的是_____ (填序号)。
①铝片与稀盐酸的反应 ②食物因氧化而腐败 ③甲烷在氧气中的燃烧反应
④ 固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥
固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥ 与
与 反应
反应
其中⑥中发生的化学方程式为_____ 。
Ⅲ.天然气(主要成分 )和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。
)和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。_____

A.将D通入
 溶液中,溶液中无明显现象,再通入
溶液中,溶液中无明显现象,再通入 ,则溶液中会出现白色沉淀
,则溶液中会出现白色沉淀B.F的浓溶液能与B反应同时生成A和D
C.将足量的F加入含H的溶液中,可以闻到臭鸡蛋气味
(2)请写出用生石灰除去燃煤产生的D,直接生成G的化学方程式
Ⅱ.水是生命之源,也是化学反应中的主角。
关于
 的反应,已知断开
的反应,已知断开 键、
键、 键、
键、 键分别需要吸收436kJ、498kJ、463kJ的能量。
键分别需要吸收436kJ、498kJ、463kJ的能量。(3)若有
 生成,需要
生成,需要(4)化学反应过程中伴随着能量变化,下列变化中属于吸热反应的是
①铝片与稀盐酸的反应 ②食物因氧化而腐败 ③甲烷在氧气中的燃烧反应
④
 固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥
固体溶于水⑤碳酸氢钠与盐酸的反应 ⑥ 与
与 反应
反应其中⑥中发生的化学方程式为
Ⅲ.天然气(主要成分
 )和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。
)和氧气的反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示。
您最近一年使用:0次
【推荐1】电化学原理在化学工业中有着广泛的应用。利用如图所示的装置能够完成很多电化学实验。回答下列问题:
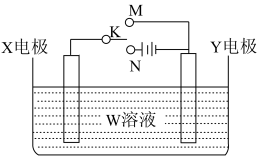
(1)将开关K置于N处:若X、Y都是石墨电极,W是饱和CuSO4溶液,则X电极上的电极反应式为_______ ;若X是石墨电极,Y是铁电极,W还是饱和CuSO4溶液,可以_______ (填“加快”或“减慢”)铁的腐蚀,这种方法称为_______ 。
(2)若粗铜中含有Au、Ag、Fe等杂质,要用电解方法精炼粗铜,则电解质溶液中Cu2+的浓度将_______ (填“增大”“减小”或“不变”),沉积在电解槽底部(阳极泥)的杂质是_______ 。
(3)若X为石墨棒,Y为铁棒,W是饱和NaCl溶液,将开关K置于M处,可以_______ (填“加快”或“减慢”)铁的腐蚀,则X电极上的电极反应式为_______ 。
(4)若X为铜棒,Y为铁棒,W是饱和CuSO4溶液,将开关K置于M处,当外电路中转移2 mol e-时,溶液_______ (填“增重”或“减轻”)_______ g。

(1)将开关K置于N处:若X、Y都是石墨电极,W是饱和CuSO4溶液,则X电极上的电极反应式为
(2)若粗铜中含有Au、Ag、Fe等杂质,要用电解方法精炼粗铜,则电解质溶液中Cu2+的浓度将
(3)若X为石墨棒,Y为铁棒,W是饱和NaCl溶液,将开关K置于M处,可以
(4)若X为铜棒,Y为铁棒,W是饱和CuSO4溶液,将开关K置于M处,当外电路中转移2 mol e-时,溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】利用烧结的铁碳混合材料可除去废水中的污染物,在有、无溶解氧的情况下均可在溶液中生成絮凝剂,实现高效工作,其作用原理图示如下:
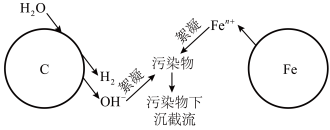
请回答:
(1)写出铁电极上电极方程式_________ 。
(2)下列叙述正确的是。
(3)有溶解氧时絮凝过程是利用了铁离子水解产物吸附污染物完成截流,写出相关的离子方程式_______ 。
(4)无溶解氧时,可以利用生成的絮凝剂处理含铬废水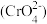 ,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为
,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为________ (以铬元素的量计算)。

请回答:
(1)写出铁电极上电极方程式
(2)下列叙述正确的是。
| A.铁电极为正极,碳电极为负极 |
| B.经过加热烧结的铁碳混合物表面空隙发达,吸附能力大幅提高,有利除污 |
| C.碳电极上的反应环境为无溶解氧环境 |
| D.铁碳混合材料工作过程中电子从铁电极流出,被絮凝剂运输至碳电极表面 |
(4)无溶解氧时,可以利用生成的絮凝剂处理含铬废水
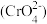 ,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为
,最终溶液中的金属离子均生成氢氧化物沉淀。已知国家标准中污染物排放浓度的单位为mg·L-1,若每处理10.0 m3污水,电极上共转移1.20 mol电子,则该污水在处理前的排放浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 6SO2+Fe3O4,有3 molFeS2参加反应,转移
6SO2+Fe3O4,有3 molFeS2参加反应,转移_______ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_________ ;从腐蚀废液回收得到金属铜,还需要的试剂是_______________ 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是____________________________
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向___________________ 。
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2
 6SO2+Fe3O4,有3 molFeS2参加反应,转移
6SO2+Fe3O4,有3 molFeS2参加反应,转移(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)如图利用氧化还原反应设计而成的原电池:
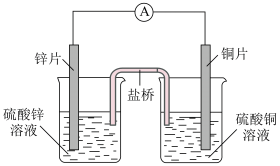
①左边烧杯内发生___________ (填“氧化”或“还原”)反应。
②右边烧杯内的电极反应式是___________ 。
③外电路中电子的流向是___________ 。
④电池总反应离子方程式是___________ 。盐桥M中装有KCl溶液和琼脂,其作用是 ___________ 。
(2)采用惰性电极电解饱和食盐水,阴极电极反应方程式___________ 。总反应的离子方程式___________ 。
(3)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图示。
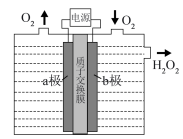
①a电极的名称是___________ 极。
②b极的电极反应方程式是___________ 。
(1)如图利用氧化还原反应设计而成的原电池:

①左边烧杯内发生
②右边烧杯内的电极反应式是
③外电路中电子的流向是
④电池总反应离子方程式是
(2)采用惰性电极电解饱和食盐水,阴极电极反应方程式
(3)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图示。

①a电极的名称是
②b极的电极反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用。已知某镍镉电池的电解质溶液为 溶液,其充、放电按下式进行:
溶液,其充、放电按下式进行: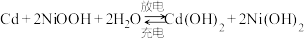 。
。
负极:_______ 。
阳极:_______ 。
(2)某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为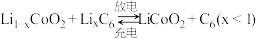 。则:
。则:
负极:_______ 。
正极:_______ 。
(1)镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用。已知某镍镉电池的电解质溶液为
 溶液,其充、放电按下式进行:
溶液,其充、放电按下式进行: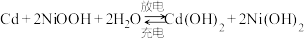 。
。负极:
阳极:
(2)某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为
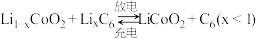 。则:
。则:负极:
正极:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学习小组用如图所示装置分别探究金属铁与稀硫酸反应。
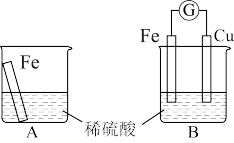
回答下列问题:
(1)A烧杯中反应的离子方程式为_______ 。
(2)B烧杯中正极为_______ (填“铜”或“铁”),电极反应式为_______ 。该原电池电解质溶液中 移向
移向_______ (填“正”或“负”)极,一段时间后,负极减少2.8g,产生气体的物质的量为_______ mol。
(3)从能量角度考虑,A、B中反应物的总能量_______ (填“>”或“<”,下同)生成物的总能量。
(4)在相同时间内两烧杯中产生气泡的速率:A_______ B.
(5)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_______(填字母)。

回答下列问题:
(1)A烧杯中反应的离子方程式为
(2)B烧杯中正极为
 移向
移向(3)从能量角度考虑,A、B中反应物的总能量
(4)在相同时间内两烧杯中产生气泡的速率:A
(5)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_______(填字母)。
| A.氯化亚铁溶液 | B.氢氧化钠溶液 | C. 溶液 溶液 | D.氯化钙溶液 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上通过氮气和氢气反应合成氨,氨经一系列反应可以得到硝酸。反应如图所示:

请回答:
(1)下列说法不正确的是(填序号字母)_______ 。
a.氮气可用作保护气
b.铵态氮肥一般不能与碱性化肥共同使用
c.硝酸可用于制化肥、农药、炸药、染料、盐类等
d.某浓硝酸中含有溶质2mol,该浓硝酸与足量铜反应最多可生成1molNO2
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大。
①合成氨反应中的能量变化如图所示,该反应是_______ 反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量_______ (填“大于”或“小于”)生成物化学键形成放出的总能量。
②在一定条件下,将一定量N2和H2的混合气体充入某恒容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是_______ (填序号字母)。
a.容器中N2、H2、NH3共存
b.N2、H2、NH3的物质的量之比为1∶3∶2
c.容器中的压强不随时间变化
d.N2、NH3浓度相等
(3)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①水吸收法。用化学方程式说明用水吸收NO2的缺陷_______ 。
②NaOH溶液吸收法。发生的反应有:
2NaOH+NO+NO2=2NaNO2+H2O
NaOH+NO2—_______+NaNO2+H2O
填化学式,并配平方程式_______ 。
③用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:(α表示尾气里NO、NO2中NO2的含量)

i.根据图得知_______ (填序号字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。
(4)随着社会的发展和科技的进步,越来越多的电池被制造出来。请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“ ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡。在下图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极
”代表小灯泡。在下图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极_______ 。

请回答:
(1)下列说法不正确的是(填序号字母)
a.氮气可用作保护气
b.铵态氮肥一般不能与碱性化肥共同使用
c.硝酸可用于制化肥、农药、炸药、染料、盐类等
d.某浓硝酸中含有溶质2mol,该浓硝酸与足量铜反应最多可生成1molNO2
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大。
①合成氨反应中的能量变化如图所示,该反应是

②在一定条件下,将一定量N2和H2的混合气体充入某恒容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是
a.容器中N2、H2、NH3共存
b.N2、H2、NH3的物质的量之比为1∶3∶2
c.容器中的压强不随时间变化
d.N2、NH3浓度相等
(3)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①水吸收法。用化学方程式说明用水吸收NO2的缺陷
②NaOH溶液吸收法。发生的反应有:
2NaOH+NO+NO2=2NaNO2+H2O
NaOH+NO2—_______+NaNO2+H2O
填化学式,并配平方程式
③用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:(α表示尾气里NO、NO2中NO2的含量)

i.根据图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
(4)随着社会的发展和科技的进步,越来越多的电池被制造出来。请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“
 ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡。在下图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极
”代表小灯泡。在下图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为(填化学式):___________ ;当线路中转移0.4 mol电子时,则被腐蚀铜的质量为:___________ g。
(2)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
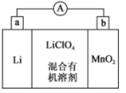
①电子流动方向是由___________ 极流向___________ 极(填字母)。
②电池正极反应式为___________ 。
③是否可用水代替电池中的混合有机溶剂?___________ (填“是”或“否”),原因是___________ 。
(3)近几年开发的甲烷—氧气燃料电池采用铂作电极催化剂,用KOH作为电池中的电解液。则通入CH4的电极为___________ 极(填“正”或“负”),通入O2的电极反应为___________ 。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为(填化学式):
(2)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。

①电子流动方向是由
②电池正极反应式为
③是否可用水代替电池中的混合有机溶剂?
(3)近几年开发的甲烷—氧气燃料电池采用铂作电极催化剂,用KOH作为电池中的电解液。则通入CH4的电极为
您最近一年使用:0次



