依据氧化还原反应: 设计的原电池如图所示。
设计的原电池如图所示。
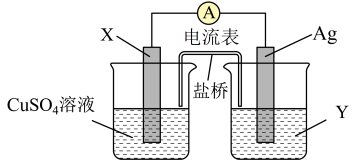
请回答下列问题:
(1)电极X的材料是___________ ;电解质溶液Y是___________ 。
(2)银电极为电池的___________ 极,发生的电极反应为___________ ;X电极上发生的电极反应为___________ 。
(3)外电路中的电子从___________ 电极流向___________ 电极。
 设计的原电池如图所示。
设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子从
更新时间:2023-09-23 08:42:12
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】请仔细观察下列三种装置的构造示意图。根据要求回答问题:
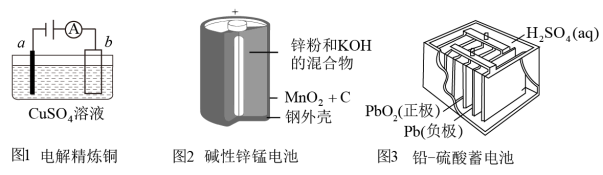
(1)电解精炼铜(如图1)时,a极材料是_________ (填“纯铜”或“粗铜”);其电解质溶液能否用CuCl2替代?答:_________ (“能”或“否”)。
(2)碱性锌锰电池(如图2)的总反应式为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,该电池的负极反应式为_________ 。若有6.5g锌参与了电池反应,则转移电子的物质的量为_________ mol。
(3)铅-硫酸蓄电池(如图3)放电过程中,正极的电极反应式为_________ ,充电时,Pb电极应接电源的_________ 极(填“正”或“负”)。

(1)电解精炼铜(如图1)时,a极材料是
(2)碱性锌锰电池(如图2)的总反应式为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,该电池的负极反应式为
(3)铅-硫酸蓄电池(如图3)放电过程中,正极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学电源的发明是化学对人类的一项重大贡献。
(1)将锌片、铜片按照如图所示装置连接,铜片做__ 极(填“正”或“负”),外电路电子的流向为__ (填“Cu→Zn”或“Zn→Cu”)。
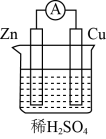
(2)若将装置中的稀H2SO4用CuSO4溶液替代,则相应原电池的总反应的化学方程式为__ 。
(3)下列化学反应通过原电池装置,可实现化学能直接转化为电能的是__ (填序号)。
①NaOH+HCl=NaCl+H2O
②CH4+2O2 CO2+2H2O
CO2+2H2O
③Fe+Cu2+=Cu+Fe2+
(1)将锌片、铜片按照如图所示装置连接,铜片做

(2)若将装置中的稀H2SO4用CuSO4溶液替代,则相应原电池的总反应的化学方程式为
(3)下列化学反应通过原电池装置,可实现化学能直接转化为电能的是
①NaOH+HCl=NaCl+H2O
②CH4+2O2
 CO2+2H2O
CO2+2H2O③Fe+Cu2+=Cu+Fe2+
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】电化学手段对于研究物质性质以及工业生产中都有重要价值。
Ⅰ.结合所学知识,按要求回答问题。
(1)碱性锌锰电池的总反应为 ,写出正极反应式
,写出正极反应式___________ 。
Ⅱ.载人航天工程对科学研究及太空资源开发具有重要意义,其发展水平是衡量一个国家综合国力的重要指标。中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩瀚星辰的征途。
(2)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的___________ 极, 向
向___________ (填“正”或“负”)极作定向移动,Y极的电极反应式为___________ 。
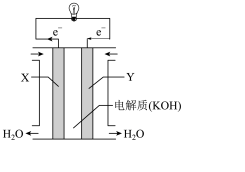
(3)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲得常温下1.8L水,则电池内电子转移的物质的量约为___________ mol
(4)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将________ 能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为: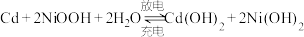 ,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性________ (填“增大”“减小”或“不变”)。
Ⅰ.结合所学知识,按要求回答问题。
(1)碱性锌锰电池的总反应为
 ,写出正极反应式
,写出正极反应式Ⅱ.载人航天工程对科学研究及太空资源开发具有重要意义,其发展水平是衡量一个国家综合国力的重要指标。中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩瀚星辰的征途。
(2)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的
 向
向
(3)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲得常温下1.8L水,则电池内电子转移的物质的量约为
(4)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将
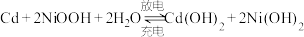 ,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:____________ 。
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是_____________ (填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是____________ 。(填字母)
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
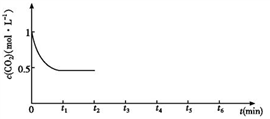
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。_____________
⑵改变温度,使反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)______ K(II)(填“﹥”“﹤”或“=”下同);平衡时CH3OH的浓度c(I)____ c(II)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=_______ 。在其他条件不变的情况下,若30min时只改变温度T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”)。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡_____ 移动(填“正向”“逆向”或“不”)。
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:
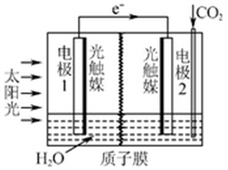
①电极2的电极反应式是____________ ;
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量_____ (填“增加”或“减少”______ g。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。

⑵改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:

①电极2的电极反应式是
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求回答下列问题:
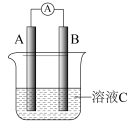
(1)如图所示是原电池的装置图。若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为___________ ,B(正极)极材料为___________ ,溶液C为___________ 。
(2)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向___________ (填“从a到b”或“从b到a”),负极发生的电极反应式为:___________ 。

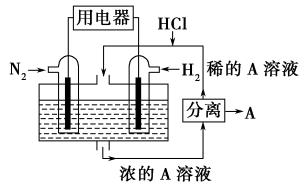
(3)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。
(1)如图所示是原电池的装置图。若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为

(2)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向

(3)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。
①电池正极发生的反应式是
②A是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据组成原电池的条件,试以反应:Fe+Cu2+=Fe2++Cu设计一个原电池,画出示意图并标出原电池的正、负极和电子的流向(画在方框中)。_________________
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:______________ ,电极反应式:___________________ ,
正极材料:______________ ,电极反应式:___________________ ,
电解质溶液:__________________ 。
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:
正极材料:
电解质溶液:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
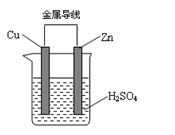
【推荐1】右图为原电池示意图,回答下列问题:
(1)该装置能够将_________ 能转化成电能。
(2)锌是原电池的_______ 极,放电过程中____ (填“得”或“失”)电子,发生_______ 反应。
(3)电子是由_______ 极通过导线流向________ 极。
(4)铜电极的电极的反应式为____________________
(5)总反应的化学方程式为_______________________

(1)该装置能够将
(2)锌是原电池的
(3)电子是由
(4)铜电极的电极的反应式为
(5)总反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据组成原电池的条件,试以反应:Fe+Cu2+=Fe2++Cu设计一个原电池,画出示意图并标出原电池的正、负极和电子的流向(画在方框中)。_________________
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:______________ ,电极反应式:___________________ ,
正极材料:______________ ,电极反应式:___________________ ,
电解质溶液:__________________ 。
供选用的电解质溶液有:稀硫酸、硫酸铜溶液
供选用的电极材料有:锌片、铜片、铁片
电极材料及电极反应式:
负极材料:
正极材料:
电解质溶液:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电池的种类繁多,应用广泛,根据电化学原理回答下列问题。
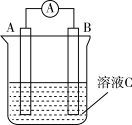
(1)下图中,若溶液 为稀
为稀 ,电流表指针发生偏转,
,电流表指针发生偏转, 电极材料为
电极材料为 且作负极,则
且作负极,则 电极上发生的电极反应式为
电极上发生的电极反应式为___________ ;反应进行一段时间后溶液酸性将___________ (填“增强”“减弱”或“基本不变”)。
(2) 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为
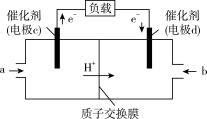
组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为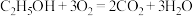 ,则
,则 电极是
电极是___________ (填“正极”或“负极”), 电极的电极反应式为
电极的电极反应式为___________ 。若线路中转移 电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(3)一种熔融碳酸盐燃料电池的原理示意图如下。请回答下列问题:
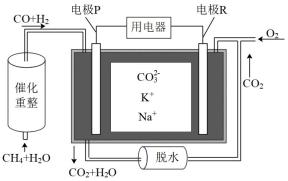
①反应 ,每消耗
,每消耗 理论上转移的电子数目为
理论上转移的电子数目为___________
②电池工作时, 向电极
向电极___________ (填“A”或“B”)移动。
③电极 上发生的电极反应为
上发生的电极反应为___________ 。
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。

①系统工作时,a极为___________ 极,b极区的电极反应式为___________ 。
②系统工作时b极区有少量固体析出,可能的原因是___________ 。
(1)下图中,若溶液
 为稀
为稀 ,电流表指针发生偏转,
,电流表指针发生偏转, 电极材料为
电极材料为 且作负极,则
且作负极,则 电极上发生的电极反应式为
电极上发生的电极反应式为
(2)
 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为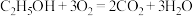 ,则
,则 电极是
电极是 电极的电极反应式为
电极的电极反应式为 电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为
(3)一种熔融碳酸盐燃料电池的原理示意图如下。请回答下列问题:

①反应
 ,每消耗
,每消耗 理论上转移的电子数目为
理论上转移的电子数目为②电池工作时,
 向电极
向电极③电极
 上发生的电极反应为
上发生的电极反应为(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。

①系统工作时,a极为
②系统工作时b极区有少量固体析出,可能的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】分析原电池的工作原理,制作简易电池。
(1)某原电池实验装置如图1所示。_______ (填“铜片”或“锌片”)。
②写出铜片上发生的电极反应:_______ 。
(2)小组同学制作的水果电池如图2所示。_______ (填字母)。
a.水果汁中含有自由移动的离子
b.该装置使氧化反应和还原反应分别在两极进行
②电流表指针偏转,说明该装置实现了化学能向_______ 的转化。
(1)某原电池实验装置如图1所示。
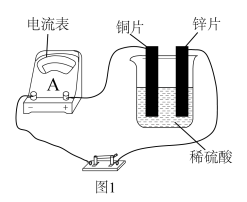
②写出铜片上发生的电极反应:
(2)小组同学制作的水果电池如图2所示。

a.水果汁中含有自由移动的离子
b.该装置使氧化反应和还原反应分别在两极进行
②电流表指针偏转,说明该装置实现了化学能向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学在生活、科研中有重要的作用。
(1)将 转化为甲醇是实现碳中和途径之一,原理为:
转化为甲醇是实现碳中和途径之一,原理为: 。在恒温恒容条件下反应
。在恒温恒容条件下反应 ,能说明反应一定达到平衡状态的是_______。
,能说明反应一定达到平衡状态的是_______。
(2)在一定温度下,体积为1L的密闭容器中,充入2mol 和6mol
和6mol ,测得
,测得 和
和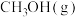 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

①2min时的
_______  (填写“大于”、“小于”、“等于”);
(填写“大于”、“小于”、“等于”);
②2min~5min的平均反应速率
_______ 。
(3)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含量,其工作原理如图所示:

①NiO电极为_______ (填“正极”或“负极”)。
②Pt电极上发生的电极反应式为_______ 。
(4)一种新型催化剂能使NO和CO发生反应 。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
①a=_______ ,b=_______ 。
②能验证温度对化学反应速率影响规律的实验是_______ (填实验编号)。
(1)将
 转化为甲醇是实现碳中和途径之一,原理为:
转化为甲醇是实现碳中和途径之一,原理为: 。在恒温恒容条件下反应
。在恒温恒容条件下反应 ,能说明反应一定达到平衡状态的是_______。
,能说明反应一定达到平衡状态的是_______。| A.氢气的浓度保持不变 |
| B.气体的压强不变 |
| C.体系的密度不变 |
D.生成1mol 同时反应1mol 同时反应1mol |
 和6mol
和6mol ,测得
,测得 和
和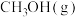 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
①2min时的

 (填写“大于”、“小于”、“等于”);
(填写“大于”、“小于”、“等于”);②2min~5min的平均反应速率

(3)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含量,其工作原理如图所示:

①NiO电极为
②Pt电极上发生的电极反应式为
(4)一种新型催化剂能使NO和CO发生反应
 。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。
。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如下三组实验。| 实验编号 | T(℃) | NO初始浓度 (  ) ) | CO初始浓度( ) ) | 催化剂的比表面积(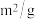 ) ) |
| I | 280 |  |  | 82 |
| II | 280 |  | b | 124 |
| III | 35 | a |  | 82 |
②能验证温度对化学反应速率影响规律的实验是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
①2FeCl3 + Cu = 2FeCl2 + CuCl2
②Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是___ (填反应序号),理由是___ 。
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。_____
(3)写出该原电池电极反应式:负极:___ ;正极:___ 。
(一)现有如下两个反应:
①2FeCl3 + Cu = 2FeCl2 + CuCl2
②Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:负极:
您最近一年使用:0次



