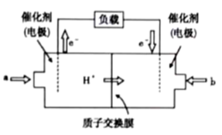
镁-空气电池的工作原理如图所示,电池反应方程式为:2Mg+O2+2H2O=2Mg(OH)2.有关该电池的说法正确的是
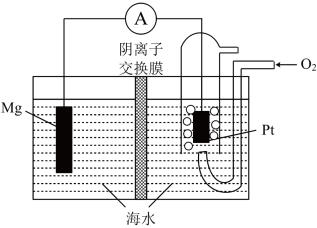

| A.通入氧气的电极为负极 |
| B.电池工作时,溶液中Na+由负极移向正极 |
| C.负极的电极反应为Mg-2e-+2OH-=Mg(OH)2 |
| D.当参加反应的O2为0.01mol时,流经电解液的电子为0.04 mol |
更新时间:2023-08-30 19:09:01
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】水系可充电电池因其成本低、高离子电导率、高安全性和环境友好性等优势而备受关注。一种 新型无隔膜Zn/MnO2液流电池的工作原理如图所示。电池以锌箔、石墨毡为集流体,ZnSO4和MnSO4的混合液作电解质溶液,下列叙述正确的是
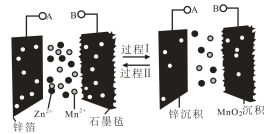

| A.过程Ⅱ为放电过程,石墨毡电极的电极反应为MnO2-2e-+4H+=Mn2++2H2O |
| B.放电时,当外电路转移2mole-时,两电极质量变化的差值为22g |
| C.过程I为锌沉积过程,B连电源的正极,电极附近pH增大 |
| D.将电解质溶液换成强酸或强碱性溶液都可延长电池的使用寿命 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为2Zn+O2===2ZnO,原料为锌粒、KOH电解液和空气,则下列叙述正确的是( )
| A.锌为正极,空气进入负极反应 | B.负极反应为Zn+2OH--2e-===ZnO+H2O |
| C.正极发生氧化反应 | D.放电时电子在溶液中从正极向负极移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列事实解释准确的是
| A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为Fe-2e- =Fe2+ |
| B.轮船的船壳吃水线以下常装有一些锌块,这是利用了外加电流的阴极保护法 |
| C.用石墨电极电解CuCl2溶液,阳极上发生的反应:2Cl--2e- =Cl2↑ |
| D.铅蓄电池的正极反应为PbO2+4H++2e-=Pb2++2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室可利用如图所示微生物电池将污水中的乙二胺[H2N(CH2)2NH2]转化为无毒无害的物质并产生电能(M、N均为石墨电极)。有关该电池工作时的说法,正确的是
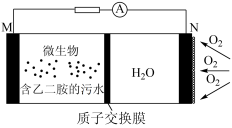

| A.该电池在微生物作用下将电能转化为化学能 |
| B.负极的电极反应式为H2N(CH2)2NH2-16e-+4H2O=2CO2↑+N2↑+16H+ |
| C.每消耗22. 4LO2时,通过质子交换膜的质子数为4NA |
| D.该电池中电子由N经导线流向M |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】近日,某团队分步进行8电子转移的电化学硝酸盐还原反应实现高效合成氨,装置如图所示。原理是:按照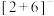 电子路径进行还原(先将硝酸盐还原成亚硝酸盐,再将亚硝酸盐还原成氨),可大幅度地降低8电子还原过程的能垒,提高其反应活性。
电子路径进行还原(先将硝酸盐还原成亚硝酸盐,再将亚硝酸盐还原成氨),可大幅度地降低8电子还原过程的能垒,提高其反应活性。
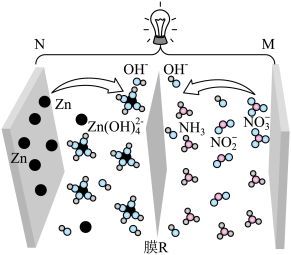
下列叙述正确的是
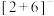 电子路径进行还原(先将硝酸盐还原成亚硝酸盐,再将亚硝酸盐还原成氨),可大幅度地降低8电子还原过程的能垒,提高其反应活性。
电子路径进行还原(先将硝酸盐还原成亚硝酸盐,再将亚硝酸盐还原成氨),可大幅度地降低8电子还原过程的能垒,提高其反应活性。
下列叙述正确的是
| A.N极为负极,发生了还原反应 |
B. 、 、 的VSEPR模型名称分别为三角锥形、直线形 的VSEPR模型名称分别为三角锥形、直线形 |
C.生成 的电极反应式为 的电极反应式为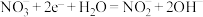 |
D.由 生成34g 生成34g  时至少转移12mol电子 时至少转移12mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】学习小组设计如图所示装置,进行NO和NO2(假设二者物质的量之比为1:1的处理并制取硝酸。下列说法正确的是


| A.ab适宜选用阳离子交换膜 |
| B.该电池工作时,正极区溶液的pH减小 |
| C.导线中流过2mol电子的电量时,有71g离子通过交换膜 |
| D.负极的电极反应式为NO+H2O-2e-=NO2+2H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】右图是一种正在投入生产的大型蓄电系统的原理图。电池的中间为只允许钠离子通过的离子选择性膜。电池充、放电的总反应方程式为:2Na2S2+NaBr3 Na2S4+3NaBr
Na2S4+3NaBr
下述关于此电池说法正确的是

| A.充电的过程中当0.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子 |
| B.电池放电时,负极反应为:3NaBr-2e-=NaBr3+2Na+ |
| C.充电过程中,电极a与电源的正极相连 |
| D.放电过程中钠离子从右到左通过离子交换膜 |
您最近一年使用:0次

 凝胶中允许离子存在、生成或迁移)。
凝胶中允许离子存在、生成或迁移)。
 极经用电器流向
极经用电器流向 极
极 减小
减小
 电子
电子