某兴趣小组利用如图所示装置进行实验。
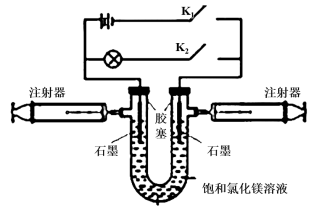
(1)断开K2、闭合K1,U形管内除电极上有气泡外,还可观察到的现象是_____ ;阳极电极反应式为________________ 。当电路中转移0.001mol电子时,右侧注射器最多可以收集到气体_______ mL(折算为标准状况)。
(2)断开K2、闭合K1一段时间,待注射器中充有一定量的气体后,断开K1、闭合K2,此时装置内化学能转化为电能。实现能量转化的化学方程式为_______________ ;
(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,U形管内的溶液理论上_______ (填“能”或“不能”)恢复原样。

(1)断开K2、闭合K1,U形管内除电极上有气泡外,还可观察到的现象是
(2)断开K2、闭合K1一段时间,待注射器中充有一定量的气体后,断开K1、闭合K2,此时装置内化学能转化为电能。实现能量转化的化学方程式为
(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,U形管内的溶液理论上
14-15高二上·福建龙岩·阶段练习 查看更多[3]
河南省鹤壁市高中2020-2021学年高二年级上学期尖子生联赛调研(三)化学试题(已下线)2014-2015学年福建三明市一中高二上第一次月考化学试卷(已下线)2013-2014学年福建省龙岩市高二第一学期教学质量检测化学试卷
更新时间:2016-12-09 05:43:59
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)如图1是一个化学过程的示意图。
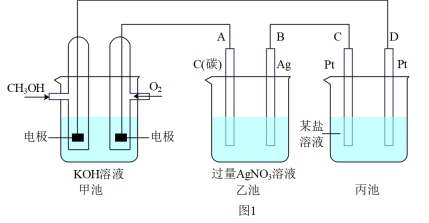
①甲池中OH-移向_______ 极(填“CH3OH”或“O2”)。
②写出通入CH3OH的电极的电极反应式_______ 。
③乙池中总反应的离子方程式_______ 。
④当乙池中B(Ag)极的质量增加5.40g,此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是_______
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)镍镉可充电电池在现代生活中有着广泛的应用,装置如图所示,它的充、放电反应为Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。请回答下列问题:
Cd(OH)2+2Ni(OH)2。请回答下列问题:
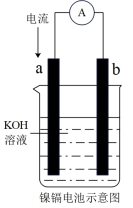
放电时,负极的电极反应式为_______ ,在放电过程中,正极附近的电解质溶液碱性会_______ (填“增强”或“减弱”)。
(1)如图1是一个化学过程的示意图。

①甲池中OH-移向
②写出通入CH3OH的电极的电极反应式
③乙池中总反应的离子方程式
④当乙池中B(Ag)极的质量增加5.40g,此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)镍镉可充电电池在现代生活中有着广泛的应用,装置如图所示,它的充、放电反应为Cd+2NiOOH+2H2O
 Cd(OH)2+2Ni(OH)2。请回答下列问题:
Cd(OH)2+2Ni(OH)2。请回答下列问题:
放电时,负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学能与电能的相互转化在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
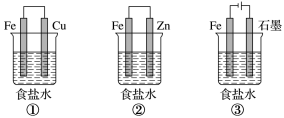
在相同条件下,三组装置中铁电极腐蚀最快的是___________ (填装置序号);装置③中 电极的电极反应式为
电极的电极反应式为___________ 。
(2)温室气体 转化为甲酸或CO,可实现资源化利用。电还原
转化为甲酸或CO,可实现资源化利用。电还原 制甲酸的装置如图所示。
制甲酸的装置如图所示。

①HCOOH在___________ 极产生,其电极反应式为___________ 。
② 的移动方向是
的移动方向是___________ (填“向左”或“向右”)。
③理论上,电路中每转移 电子,生成标准状况下的
电子,生成标准状况下的 体积为
体积为___________ L。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是
 电极的电极反应式为
电极的电极反应式为(2)温室气体
 转化为甲酸或CO,可实现资源化利用。电还原
转化为甲酸或CO,可实现资源化利用。电还原 制甲酸的装置如图所示。
制甲酸的装置如图所示。
①HCOOH在
②
 的移动方向是
的移动方向是③理论上,电路中每转移
 电子,生成标准状况下的
电子,生成标准状况下的 体积为
体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1) 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生 ,若将此反应设计成原电池,则负极所用电极材料为
,若将此反应设计成原电池,则负极所用电极材料为___________ ,当线路中转移 电子时,则被腐蚀铜的质量为
电子时,则被腐蚀铜的质量为___________ g.
(2)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压.高铁电池的总反应式为: .放电时,负极反应式充电为
.放电时,负极反应式充电为___________________ ,
(3)实验小组对可逆反应 进行探究。
进行探究。 时,起始向
时,起始向 恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度
恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度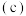 与时间
与时间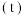 的关系如图所示.
的关系如图所示. 内的反应速率
内的反应速率
____________________ ;
②为提高此反应的速率,下列措施可行的是_________ (填字母代号);
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达③最大限度时Y的体积分数为_____________________ ;
④下列描述能表示该反应达平衡状态的是_____________________ ;
A.容器内的混合气体的平均相对分子质量不再改变 B.容器内压强不再发生变化
C. D.X的体积分数不再改变
D.X的体积分数不再改变
(1)
 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生 ,若将此反应设计成原电池,则负极所用电极材料为
,若将此反应设计成原电池,则负极所用电极材料为 电子时,则被腐蚀铜的质量为
电子时,则被腐蚀铜的质量为(2)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压.高铁电池的总反应式为:
 .放电时,负极反应式充电为
.放电时,负极反应式充电为(3)实验小组对可逆反应
 进行探究。
进行探究。 时,起始向
时,起始向 恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度
恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度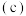 与时间
与时间 的关系如图所示.
的关系如图所示.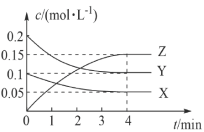
 内的反应速率
内的反应速率
②为提高此反应的速率,下列措施可行的是
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达③最大限度时Y的体积分数为
④下列描述能表示该反应达平衡状态的是
A.容器内的混合气体的平均相对分子质量不再改变 B.容器内压强不再发生变化
C.
 D.X的体积分数不再改变
D.X的体积分数不再改变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】用如图所示的装置进行电解,A中盛有NaOH溶液,B中盛有饱和Na2SO4溶液,通电一会儿,发现湿润的淀粉KI试纸的D端变为蓝色。回答下列问题:
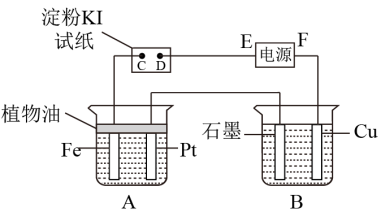
(1)电源的E端为__ (填“正”或“负”)极。
(2)A中Fe电极上的电极反应式为___ ;一段时间后,A中溶液pH__ (填“升高”、“降低”或“不变”)。
(3)B中发生反应的总化学方程式为___ 。
(4)电池工作tmin后,B装置中共收集到16.8L(折算为标准状况下)气体,此时电路中转移了__ mole-。
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸D端变为蓝色,下列做法可行的是__ (填标号)。
a. 将A中的溶液换成稀硫酸
b. 将A中的溶液换成浓硝酸
c. 将B中的溶液换成稀硫酸
d. 将B中的溶液换成浓硝酸

(1)电源的E端为
(2)A中Fe电极上的电极反应式为
(3)B中发生反应的总化学方程式为
(4)电池工作tmin后,B装置中共收集到16.8L(折算为标准状况下)气体,此时电路中转移了
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸D端变为蓝色,下列做法可行的是
a. 将A中的溶液换成稀硫酸
b. 将A中的溶液换成浓硝酸
c. 将B中的溶液换成稀硫酸
d. 将B中的溶液换成浓硝酸
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某小组采用电化学方法处理废气或废水中的污染物。
(一)电解法处理废气中的氨(NH3),装置如图所示。

(1)一段时间后,溶液中Fe3+、Fe2+的总物质的量___ (填“增大”“减小”或“基本不变”)。
(2)阳极的电极反应式为____ 。
(3)若要处理8.96LNH3(标准状况),理论上消耗O2___ mol。
(二)采用纳米铁粉、炭粉的混合物可处理废水中的NO ,原理如图1所示。
,原理如图1所示。

(4)纳米铁粉中掺杂炭粉的原因是____ 。正极的电极反应式为____ 。
(5)实验表明酸性废水中NO 的浓度与溶液pH的关系如图2所示。pH<a时,pH越低,NO
的浓度与溶液pH的关系如图2所示。pH<a时,pH越低,NO 处理率越低的主要原因可能是
处理率越低的主要原因可能是____ 。

(一)电解法处理废气中的氨(NH3),装置如图所示。

(1)一段时间后,溶液中Fe3+、Fe2+的总物质的量
(2)阳极的电极反应式为
(3)若要处理8.96LNH3(标准状况),理论上消耗O2
(二)采用纳米铁粉、炭粉的混合物可处理废水中的NO
 ,原理如图1所示。
,原理如图1所示。
(4)纳米铁粉中掺杂炭粉的原因是
(5)实验表明酸性废水中NO
 的浓度与溶液pH的关系如图2所示。pH<a时,pH越低,NO
的浓度与溶液pH的关系如图2所示。pH<a时,pH越低,NO 处理率越低的主要原因可能是
处理率越低的主要原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用石墨电极电解一定量的硫酸铜溶液,实验装置如图①。电解过程中的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

(1)a电极是___________ 极,其中 移向
移向___________ 极(填a或b)。
(2)电解过程中,b电极的电极反应式:___________ 。
(3)电解过程中,a电极表面现象:___________ 。
(4)从P到Q点时收集到的混合气体的平均摩尔质量为___________ 。

(1)a电极是
 移向
移向(2)电解过程中,b电极的电极反应式:
(3)电解过程中,a电极表面现象:
(4)从P到Q点时收集到的混合气体的平均摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】用如图所示的装置进行电解,A中盛有NaCl溶液,B中盛有饱和Na2SO4溶液,通电一会儿,发现湿润的淀粉KI试纸的D端变为蓝色。回答下列问题:

(1)电源的 F端为_______ (填“正”或“负”)极。
(2)A中发生反应的总化学方程式为_______ 。
(3)B中石墨电极上的电极反应式为_______ ;Cu电极观察到的现象是_______ ;一段时间后,B中溶液pH_______ (填“升高”、“降低”或“不变”)
(4)电池工作t min后,B装置中共收集到16.8 L(折算为标准状况下)气体,此时A中溶液的质量减轻了_______ g。
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸的D端变为蓝色,可将_______ (填“A”或“B”)中的溶液换成_______ (填“稀硫酸”或“浓硝酸”)。

(1)电源的 F端为
(2)A中发生反应的总化学方程式为
(3)B中石墨电极上的电极反应式为
(4)电池工作t min后,B装置中共收集到16.8 L(折算为标准状况下)气体,此时A中溶液的质量减轻了
(5)去掉该装置中的电源,改用导线连接,为使湿润的淀粉KI试纸的D端变为蓝色,可将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
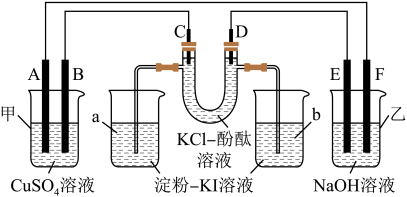
【推荐2】按下图所示装置进行实验,并回答下列问题:

(1)判断装置A和B的能量转化形式:A池为______________ ,B池为_________________ 。
(2)锌电极发生_________ 反应;铜极发生__________________________ 反应;石墨棒C1为____ 极,电极反应式为_________ ;石墨棒C2附近发生的实验现象___________ 。
(3)当C2极析出44.8 L气体(标准状况下),锌的质量变化为(增加或减少)________ g。CuSO4溶液的质量变化为(增加或减少)________ g。

(1)判断装置A和B的能量转化形式:A池为
(2)锌电极发生
(3)当C2极析出44.8 L气体(标准状况下),锌的质量变化为(增加或减少)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某实验兴趣小组利用如下图所示装置进行电解饱和食盐水并检验其生成物的实验,当图中开关K闭合片刻后,请回答下列问题:

(1)电解饱和食盐水的化学方程式为___________ 。
(2)a为电源的___________ (填“正”或“负”)极;D中收集的气体是___________ 。
(3)C试管盛放___________ 溶液。溶液中A电极附近的现象为___________ 。

(1)电解饱和食盐水的化学方程式为
(2)a为电源的
(3)C试管盛放
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜是与人类关系非常密切的有色金属。已知:常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:Cu+=Cu2++Cu。大多数+1价铜的化合物是难溶物,Cu2O、CuI、CuCl、CuH等。
(1)在CuCl2溶液中逐滴加入过量KI溶液可能发生以下反应:
a.2Cu2++4I-=2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-=2CuCl↓(白色)+I2
为顺利观察到白色沉淀可以加入的最佳试剂是___________。
(2)一定条件下,在CuSO4中加入NH5反应生成氢化亚铜(CuH)。写出CuH在过量稀盐酸中有气体生成的离子方程式:___________ 。
(3)纳米级Cu2O具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一、以铜作阳极,石墨作阴极电解。已知:铜作阳极时,铜先被氧化生成Cu+,后Cu+继续氧化生成Cu2+;在碱性溶液中CuCl浊液易转化为Cu2O。
①以NaOH溶液作为电解质溶液时需添加NaCl,其目的是___________ ,写出阳极反应式:___________ 。
②写出在碱性溶液中CuCl浊液转化为Cu2O的离子方程式:___________ 。
(1)在CuCl2溶液中逐滴加入过量KI溶液可能发生以下反应:
a.2Cu2++4I-=2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-=2CuCl↓(白色)+I2
为顺利观察到白色沉淀可以加入的最佳试剂是___________。
| A.SO2 | B.苯 | C.NaOH溶液 | D.乙醇 |
(3)纳米级Cu2O具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一、以铜作阳极,石墨作阴极电解。已知:铜作阳极时,铜先被氧化生成Cu+,后Cu+继续氧化生成Cu2+;在碱性溶液中CuCl浊液易转化为Cu2O。
①以NaOH溶液作为电解质溶液时需添加NaCl,其目的是
②写出在碱性溶液中CuCl浊液转化为Cu2O的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是一个化学过程的示意图,回答下列问题:
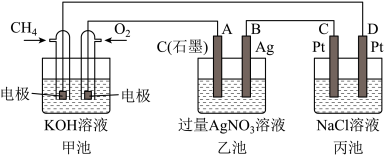
(1)甲池是_____ 装置,乙装置中电极A的名称是______ 。
(2)甲装置中通入CH4的电极反应式为_____ ,乙装置中电极B(Ag)的电极反应式为_____ ,丙装置中D极的产物是_____ (写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=_____ 。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入_______ (写名称)。

(1)甲池是
(2)甲装置中通入CH4的电极反应式为
(3)一段时间,当丙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=
您最近一年使用:0次