按要求书写下列反应的离子方程式:
(1)碳酸氢钠溶液和稀盐酸混合:________ 。
(2)少量二氧化碳通入澄清的石灰水:_________ 。
(3)氧化钠与稀盐酸反应:_________ 。
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:________ 。
(1)碳酸氢钠溶液和稀盐酸混合:
(2)少量二氧化碳通入澄清的石灰水:
(3)氧化钠与稀盐酸反应:
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
更新时间:2023-10-25 10:25:48
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】已知下列各物质:
① CO2 ② Mg ③ NaHSO4 溶液 ④ CaCO3 ⑤ NaOH 溶液 ⑥ NH3·H2O ⑦ 乙醇 ⑧ 盐酸
(1)属于电解质的有___________ (填序号,下同), 非电解质的有___________ 。
(2)写出⑥的电离方程式:___________ 。
(3)写出③与⑤发生反应的离子方程式:___________ 。
(4)已知①与②发生反应的化学方程式为 2 Mg+CO 2 MgO+C 请用双线桥标出该反应的电子 转移方向和数目:
2 MgO+C 请用双线桥标出该反应的电子 转移方向和数目:___________ 。
① CO2 ② Mg ③ NaHSO4 溶液 ④ CaCO3 ⑤ NaOH 溶液 ⑥ NH3·H2O ⑦ 乙醇 ⑧ 盐酸
(1)属于电解质的有
(2)写出⑥的电离方程式:
(3)写出③与⑤发生反应的离子方程式:
(4)已知①与②发生反应的化学方程式为 2 Mg+CO
 2 MgO+C 请用双线桥标出该反应的电子 转移方向和数目:
2 MgO+C 请用双线桥标出该反应的电子 转移方向和数目:
您最近一年使用:0次
【推荐2】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用,某博物馆修复出土铁器的过程如表:
(1)检测锈蚀产物。
铁器被腐蚀本质上可以看成是铁被___________ (填氧化或是还原)。Fe3O4中铁元素的化合价为___________ 。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ. Fe转化为Fe2+
Ⅱ. Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为___________ 。写出FeO(OH)与盐酸的反应方程式:___________ 。
Ⅲ. FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe3O4保护层被氧化成FeO(OH),如此往复腐蚀。
___________Fe3O4+___________O2+___________H2O=___________FeO(OH)(将反应方程式配平)___________ 。
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:将铁器浸没在盛有0.5mol/L Na2SO3、0.5mol/L NaOH溶液的容器中,缓慢加热至60~90℃,一段时间,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是___________ 。
②脱氯反应:FeOCl+OH-=FeO(OH)+Cl-,离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:___________ 较大【填FeOCl或FeO(OH)】。
(1)检测锈蚀产物。
| 主要成分的化学式 | |||
| Fe3O4 | Fe2O3·H2O | FeO(OH) | FeOCl |
铁器被腐蚀本质上可以看成是铁被
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ. Fe转化为Fe2+
Ⅱ. Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为
Ⅲ. FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe3O4保护层被氧化成FeO(OH),如此往复腐蚀。
___________Fe3O4+___________O2+___________H2O=___________FeO(OH)(将反应方程式配平)
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:将铁器浸没在盛有0.5mol/L Na2SO3、0.5mol/L NaOH溶液的容器中,缓慢加热至60~90℃,一段时间,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是
②脱氯反应:FeOCl+OH-=FeO(OH)+Cl-,离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列反应的离子方程式:
(1)氢氧化钡溶液和稀硫酸反应_______ ;
(2)氢氧化钾溶液和稀醋酸反应_______ ;
(3)碳酸钠溶液和稀硝酸反应_______ ;
(4)碳酸钙和稀盐酸反应_______ ;
(5)氧化钙和稀硫酸反应_______ 。
(1)氢氧化钡溶液和稀硫酸反应
(2)氢氧化钾溶液和稀醋酸反应
(3)碳酸钠溶液和稀硝酸反应
(4)碳酸钙和稀盐酸反应
(5)氧化钙和稀硫酸反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】依次书写下列有关反应化学方程式或离子方程式,并指出某些反应的氧化剂。
(1)铁与水蒸气反应_________________________ 氧化剂_________________
(2)二氧化硅与碳在高温下反应_______________________________ 氧化剂_________
(3)硝酸银与氯化钠反应的离子方程式______________________
(4)粗盐提纯中与氯化钡反应的相关离子方程式_____________________________________
(1)铁与水蒸气反应
(2)二氧化硅与碳在高温下反应
(3)硝酸银与氯化钠反应的离子方程式
(4)粗盐提纯中与氯化钡反应的相关离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某无色透明溶液中可能存在大量Cl-、Mg2+、Fe3+、K+、Cu2+中的一种或几种,请回答下列问题:
(1)不用做任何实验就可以肯定溶液中不存在的离子是______ 。
(2)取少量原溶液,加入过量硝酸银溶液,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是______ ,反应的离子方程式为______ 。
(3)取少量原溶液,向其中加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是______ ,生成沉淀的离子方程式为______ 。
(4)检验原溶液中可能存在的阳离子的实验方法(写出实验操作、现象及结论)______ ,原溶液中还可能大量存在的阴离子是______ (填字母)。
A.SO B.NO
B.NO C.CO
C.CO D.OH-
D.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量硝酸银溶液,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取少量原溶液,向其中加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)检验原溶液中可能存在的阳离子的实验方法(写出实验操作、现象及结论)
A.SO
 B.NO
B.NO C.CO
C.CO D.OH-
D.OH-
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】运用分类的方法,可以发现物质及其变化的规律。
(1) 与CaO都属于
与CaO都属于______ 氧化物(填“酸性”或“碱性”)。
(2)请书写 与HCl反应的化学方程式
与HCl反应的化学方程式______ 。
(3)请书写 与
与 反应的离子方程式
反应的离子方程式______ 。
(1)
 与CaO都属于
与CaO都属于(2)请书写
 与HCl反应的化学方程式
与HCl反应的化学方程式(3)请书写
 与
与 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】向酚酞溶液中加入 会出现大量气体,溶液颜色变化为
会出现大量气体,溶液颜色变化为________ ;说明 具有
具有________ 性质。
 会出现大量气体,溶液颜色变化为
会出现大量气体,溶液颜色变化为 具有
具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)工业上将含有硫化物的废水(以H2S、HS-、S2−的形式存在)引入氧化池,加入高锰酸钾溶液氧化。已知高锰酸钾在酸性条件下的还原产物为Mn2+,碱性条件下的为MnO2。
①pH>7时高锰酸钾将废水中的硫化物氧化为S,该反应的离子方程式为_______ 。
②研究发现:其他条件相同时,废水呈酸性时硫化物的去除率明显大于呈碱性时去除率,则可能的原因_______ 。
(2)表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用图1表示。其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。

①适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是_______ 。
②若水膜过厚,H2S的氧化去除率减小的原因是_______ 。
(3)向100mL含Na2CO3、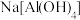 的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:

①已知 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式为
在溶液中反应而不能大量共存,写出两者反应的离子方程式为_______ 。
②d曲线表示的离子方程式为_______ 。
③加入HCl溶液的物质的量浓度为_______ 。
④原混合溶液中的Na+与 的物质的量之比为
的物质的量之比为_______ 。
(1)工业上将含有硫化物的废水(以H2S、HS-、S2−的形式存在)引入氧化池,加入高锰酸钾溶液氧化。已知高锰酸钾在酸性条件下的还原产物为Mn2+,碱性条件下的为MnO2。
①pH>7时高锰酸钾将废水中的硫化物氧化为S,该反应的离子方程式为
②研究发现:其他条件相同时,废水呈酸性时硫化物的去除率明显大于呈碱性时去除率,则可能的原因
(2)表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用图1表示。其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。

①适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是
②若水膜过厚,H2S的氧化去除率减小的原因是
(3)向100mL含Na2CO3、
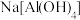 的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
①已知
 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式为
在溶液中反应而不能大量共存,写出两者反应的离子方程式为②d曲线表示的离子方程式为
③加入HCl溶液的物质的量浓度为
④原混合溶液中的Na+与
 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】书写下列反应的离子方程式。
(1)用碳酸钙与稀盐酸反应制备二氧化碳______ 。
(2)碳酸氢钠与盐酸反应______ 。
(3)少量二氧化碳通入氢氧化钠溶液中反应______ 。
(4)钠与水反应的离子方程式表示为______ 。
(5)向Na2CO3溶液中通入CO2生成NaHCO3溶液。离子方程式表示为______ 。
(1)用碳酸钙与稀盐酸反应制备二氧化碳
(2)碳酸氢钠与盐酸反应
(3)少量二氧化碳通入氢氧化钠溶液中反应
(4)钠与水反应的离子方程式表示为
(5)向Na2CO3溶液中通入CO2生成NaHCO3溶液。离子方程式表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)都可作为食用碱.
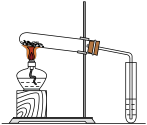
(1)用如图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中受热的固体是______ .通过本实验证明,这两种固体对热的稳定性是Na2CO3______ 于(选填“强”或“弱”)NaHCO3。
(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,都能观察到的现象是______ ,其中碳酸氢钠和稀盐酸反应的化学方程式为_________________________ .
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有____________ (写出两个物质名称或化学式)等.
(1)用如图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中受热的固体是

(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,都能观察到的现象是
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有
您最近一年使用:0次

 的溶液中,逐滴加入NaOH溶液至过量,反应的离子方程式依次为
的溶液中,逐滴加入NaOH溶液至过量,反应的离子方程式依次为

