依次书写下列有关反应化学方程式或离子方程式,并指出某些反应的氧化剂。
(1)铁与水蒸气反应_________________________ 氧化剂_________________
(2)二氧化硅与碳在高温下反应_______________________________ 氧化剂_________
(3)硝酸银与氯化钠反应的离子方程式______________________
(4)粗盐提纯中与氯化钡反应的相关离子方程式_____________________________________
(1)铁与水蒸气反应
(2)二氧化硅与碳在高温下反应
(3)硝酸银与氯化钠反应的离子方程式
(4)粗盐提纯中与氯化钡反应的相关离子方程式
更新时间:2019-12-28 17:13:35
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)画出钠离子结构示意图_______ 。
(2)写出Cl元素的最高价含氧酸的化学式_______ 。
(3)写出N2的结构式_______ 。
(4) Al2(SO4)3固体溶于水的电离方程式是_______ 。
(5)用电子式表示MgCl2的形成过程_______ 。
(6)写出AlCl3溶液中滴加过量氨水的离子方程式_______ 。
(2)写出Cl元素的最高价含氧酸的化学式
(3)写出N2的结构式
(4) Al2(SO4)3固体溶于水的电离方程式是
(5)用电子式表示MgCl2的形成过程
(6)写出AlCl3溶液中滴加过量氨水的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】按要求完成下列填空:
(1)用98%的浓硫酸(密度为1.84g/mL)配制0.5mol/L稀硫酸溶液480mL,所需浓硫酸的体积为______ mL(保留一位小数)。
(2) 相对分子质量为M的某物质在室温下的溶解度为Sg/100g水,此时饱和溶液的密度为dg/mL,则该饱和溶液的物质的量浓度是____________ mol/L。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,写出发生反应的离子方程式___________ 。
(4)以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥蔗糖 ⑦AgCl ⑧Fe(OH)3胶体。
A.其中能导电的是____________ (填序号,下同)
B.属于电解质的是__________
C.属于非电解质的是_________________
D.NaHSO4熔融状态下的电离方程式____________________
E.某同学向⑧中逐滴加入了稀硫酸,结果出现了一系列变化,先出现红褐色沉淀,原因是______________________________________ ,随后沉淀溶解,此反应的离子方程式是______________________________________ 。
(1)用98%的浓硫酸(密度为1.84g/mL)配制0.5mol/L稀硫酸溶液480mL,所需浓硫酸的体积为
(2) 相对分子质量为M的某物质在室温下的溶解度为Sg/100g水,此时饱和溶液的密度为dg/mL,则该饱和溶液的物质的量浓度是
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,写出发生反应的离子方程式
(4)以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥蔗糖 ⑦AgCl ⑧Fe(OH)3胶体。
A.其中能导电的是
B.属于电解质的是
C.属于非电解质的是
D.NaHSO4熔融状态下的电离方程式
E.某同学向⑧中逐滴加入了稀硫酸,结果出现了一系列变化,先出现红褐色沉淀,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】SiO2广泛存在自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。
(1)写出工业上制备粗硅的化学反应方程式_________________ 。
(2)SiO2耐腐蚀,但易溶于氢氟酸,写出化学反应方程式:______________ 。
(1)写出工业上制备粗硅的化学反应方程式
(2)SiO2耐腐蚀,但易溶于氢氟酸,写出化学反应方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)石英耐高温,可制成石英坩埚,下列试剂可用石英坩埚加热的是________ ;
A.NaOH B.CaCO3 C.Na2CO3 D.KHSO4
(2)奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用氧化物的形式可表示为________________________ ;
(3)有以下13种物质,请回答下列问题(填序号):
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
其中能导电的是_________ ; 属于电解质的是 _________ ;属于非电解质的是 _________ 。
A.NaOH B.CaCO3 C.Na2CO3 D.KHSO4
(2)奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,则其用氧化物的形式可表示为
(3)有以下13种物质,请回答下列问题(填序号):
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
其中能导电的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】中学化学常见物质的转化关系如图所示。已知M、N为常见的活泼金属单质,F为黄绿色气体单质,I为红褐色固体,P为淡黄色固体。回答下列问题:
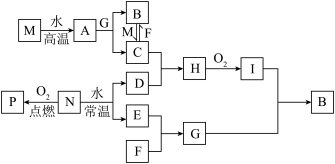
(1)B的化学式为___________ ;C溶液的颜色为:___________ ;
(2)N长期置于空气中,最后形成的物质是:___________ (填化学式)
(3)H生成I的化学方程式为:___________ 。
(4)C和F在溶液中反应生成B的离子方程式为___________ 。
(5)C、D在溶液中反应的实验现象(在空气中)___________ 。
(6)P可以做供氧剂,其原理是___________ 。(用方程式表示)

(1)B的化学式为
(2)N长期置于空气中,最后形成的物质是:
(3)H生成I的化学方程式为:
(4)C和F在溶液中反应生成B的离子方程式为
(5)C、D在溶液中反应的实验现象(在空气中)
(6)P可以做供氧剂,其原理是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)鉴别NaCl溶液和KCl溶液的实验方法是______ 。
(2)铁与水蒸气反应的方程式为______ 。
(3)除去CO2中混有的HCl气体所用试剂为______ 。
(2)铁与水蒸气反应的方程式为
(3)除去CO2中混有的HCl气体所用试剂为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】金属和非金属在人类生产生活中得到了广泛应用,请你回答下列问题。
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为________ ;漂白粉的有效成分为__________ (写化学式);FeCl3常用作净水剂,其原理为_________ (用离子方程式表示)。
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是_________ 。
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是____________
A.亚硝酸盐是还原剂B.维生素C是氧化剂
C.维生素C被氧化D.亚硝酸盐发生氧化反应
(1)面包发酵粉的主要成分之一是一种钠盐,其俗称为
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是
(3)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是
A.亚硝酸盐是还原剂B.维生素C是氧化剂
C.维生素C被氧化D.亚硝酸盐发生氧化反应
您最近一年使用:0次

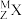 ,已知 M=30,且 M−Z=16,则:
,已知 M=30,且 M−Z=16,则:

