下列说法错误 的是
A.同温同压下, 在光照和点燃条件下的ΔH相同 在光照和点燃条件下的ΔH相同 |
| B.化学键断裂和形成时的能量变化是化学反应中能量变化的主要原因 |
C.甲烷的燃烧热为890.3kJ·mol-1,则1molCH4发生反应 放出的热量小于890.3kJ 放出的热量小于890.3kJ |
D.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,其热化学方程式可表示为: 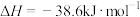 |
更新时间:2023-10-26 19:33:08
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】对于反应2H2(g) + 2Cl2(g) →4HCl(g), 25°C下该反应的ΔH° = -369.2 kJ/mol。下列说法中,不正确的是
| A.逆反应的△H°为+369.2 kJ/mol |
| B.四个HCl分子的键强于H2和Cl2分子的四个键 |
| C.每产生1 mol HCl(g)将放出92.3 kJ的热量 |
| D.当产生1 mol HCl(1)时反应的△H°为 -92.3 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】物质在发生化学变化时,下列说法正确的是
| A.反应物的总质量等于生成物的总质量 |
| B.发生电子得失或偏移 |
| C.化学反应中有化学键的断裂,可能释放能量 |
| D.反应物所具有的总能量大于生成物所具有的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列热化学方程式中ΔH的数值表示物质燃烧热的是
| A.CH4(g)+O2(g)=2H2O(l)+CO(g) ΔH | B.H2(g)+Cl2(g)=2HCl(g) ΔH |
| C.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH | D.2CO(g)+O2(g)=2CO2(g) ΔH |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实与对应的方程式不相符的是( )
| A.已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH<0,灼热的铂丝与NH3、O2混合气接触,铂丝继续保持红热 |
B.已知:2NO2(g)(红棕色) N2O4(g)(无色) ΔH<0,将“NO2球”浸泡在冷水中,颜色变浅 N2O4(g)(无色) ΔH<0,将“NO2球”浸泡在冷水中,颜色变浅 |
| C.因H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,故向含0.1molHCl的盐酸中加入4.0gNaOH固体,放出的热量等于5.73kJ |
| D.甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1,则甲烷的燃烧热为890.3kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】1 mol H2在O2中完全燃烧生成液态水放出285.8kJ的热量,下列热化学方程式正确的是
A.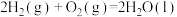 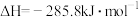 |
B.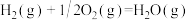 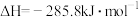 |
C.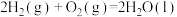 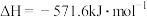 |
D. 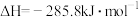 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】甲烷是一种高效清洁的新能源,4g甲烷完全燃烧生成液态水时放出222.5kJ热量,则下列热化学方程式中表示甲烷燃烧热的热化学方程式是
| A.1/2CH4(g) + O2(g) = 1/2CO2(g) + H2O(l) ΔH= +445 kJ·mol-1 |
| B.CH4(g) + 2O2(g) = CO2(g) +2H2O(l) ΔH= +890 kJ·mol-1 |
| C.CH4(g) + 2O2(g) = CO2(g) +2H2O(l) ΔH= -890 kJ·mol-1 |
| D.2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l) ΔH= -1780 kJ·mol-1 |
您最近一年使用:0次

 甲烷与
甲烷与 发生取代反应生成
发生取代反应生成 ,需
,需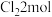
 的变化需吸收能量
的变化需吸收能量 葡萄糖
葡萄糖 和1.5mol
和1.5mol 置于密闭的容器中充分反应生成
置于密闭的容器中充分反应生成 ,放热19.3kJ,热化学方程式为:
,放热19.3kJ,热化学方程式为:

 完全燃烧生成
完全燃烧生成 放出的热量叫
放出的热量叫 的燃烧热是
的燃烧热是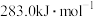 ,
, 分解的热化学方程式为:
分解的热化学方程式为:



