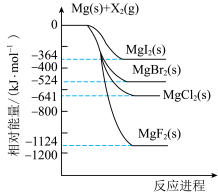
镁和卤素单质( )反应的相对能量变化如图所示,下列说法正确的是
)反应的相对能量变化如图所示,下列说法正确的是
 )反应的相对能量变化如图所示,下列说法正确的是
)反应的相对能量变化如图所示,下列说法正确的是
A.热稳定性: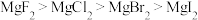 |
| B.1mol碘晶体与足量的Mg充分反应,放热364kJ |
C.工业上常用电解 溶液的方法冶炼金属Mg 溶液的方法冶炼金属Mg |
D.由图可知, 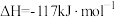 |
更新时间:2023-10-28 17:22:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在298K、1.01×105Pa下,将22gCO2通入750mL1mol•L-1NaOH溶液中充分反应,测得反应放出xkJ的热量。已知该条件下,将1molCO2通入1L2mol•L-1NaOH溶液中充分反应放出ykJ的热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是
| A.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(2y-x)kJ•mol-1 |
| B.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(2x-y)kJ•mol-1 |
| C.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(4x-y)kJ•mol-1 |
| D.2CO2(g)+2NaOH(aq)=2NaHCO3(aq) ΔH=-(4x-2y)kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲醇与水蒸气重整可获得清洁能源,在催化剂作用下发生如下两步反应∶
反应①∶CH3OH(g)==CO(g)+2H2(g) △H1
反应②∶CO(g) + H2O(g)==CO2(g)+H2(g) △H2
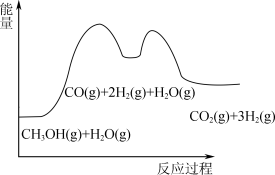
根据能量变化示意图,下列说法不正确 的是( )
反应①∶CH3OH(g)==CO(g)+2H2(g) △H1
反应②∶CO(g) + H2O(g)==CO2(g)+H2(g) △H2
根据能量变化示意图,下列说法

A.总反应的热化学方程式为∶ CH3OH(g)+H2O(g)= =CO2(g)+3H2(g) 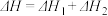 |
| B.1mol CO(g)和1mol H2O(g)的总键能大于lmol CO2(g)和1mol H2(g)的总键能 |
| C.甲醇与水蒸气催化重整的总反应速率取决于反应① |
| D.催化剂在反应中改变了活化能,加快了反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】能源问题是人类社会面临的重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为285.8 kJ·mol-1、282.5 kJ·mol-1、726.7 kJ·mol-1。已知CO和H2在一定条件下可以合成甲醇CO(g)+2H2(g)===CH3OH(l)。则CO与H2反应合成甲醇的热化学方程式为( )
| A.CO(g)+2H2(g)===CH3OH(l) ΔH=+127.4 kJ·mol-1 |
| B.CO(g)+2H2(g)===CH3OH(l) ΔH=-127.4 kJ·mol-1 |
| C.CO(g)+2H2(g)===CH3OH(g) ΔH=-127.4 kJ·mol-1 |
| D.CO(g)+2H2(g)===CH3OH(g) ΔH=+127.4 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】金刚石和石墨都能燃烧,氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。下列说法正确的是
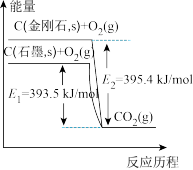

| A.金刚石和石墨互为同素异形体,它们之间的转化属于化学变化 |
| B.金刚石比石墨稳定 |
| C.相同物质的量的金刚石比石墨所含有的能量低 |
| D.由金刚石制取石墨放出1.9 kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于化学反应中物质或能量变化的判断正确的是
| A.任何化学反应中的能量变化都表现为热量变化 |
| B.化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因 |
| C.需要加热才能进行的反应一定是吸热反应,放热反应不需要加热 |
| D.由C(石墨,s)=C(金刚石,s) △H=+1.9kJ•mol-1,可知金刚石比石墨稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学与生产、生活及环境密切相关,下列说法错误的是
| A.纯碱去除油污时发生了水解反应 |
B.火法炼铜的矿石原料主要含 |
| C.煤经过气化和液化等化学变化可转化为清洁能源 |
| D.体积分数为95%的酒精溶液可以更有效地灭活新型冠状病毒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】前20号主族元素W、 X、Y 、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3 倍。X、Y 、Z分属不同的周期,它们的原子序数之和是W原子序数的5倍。含有元素Z的盐的焰色反应为紫色。下到说法正确的是
| A.原子半径的大小W<X<Y<Z | B.简单氢化物的热稳定性W>X |
| C.Z的单质与水反应比Y的单质与水反应剧烈 | D.工业上通过电解W、Y组成的化合物制备单质Y |
您最近一年使用:0次

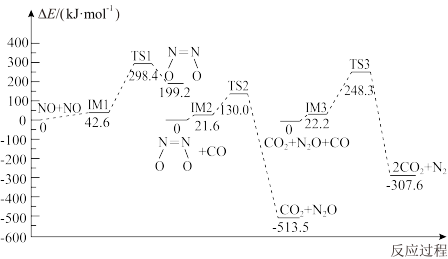
 N2(g) +2CO2(g) ΔH>0
N2(g) +2CO2(g) ΔH>0 )比N2O分子更容易与CO发生反应
)比N2O分子更容易与CO发生反应 Zn+3CO↑
Zn+3CO↑

