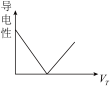
甲、乙、丙、丁是分别由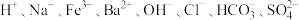 八种离子中的两种(不重复)组成的四种可溶性化合物,且已知:①甲+乙→红褐色沉淀;②甲+丙→白色沉淀;③甲+丁→白色沉淀,向甲溶液中逐滴加入丁溶液,其导电能力随丁加入的体积变化曲线如图所示:
八种离子中的两种(不重复)组成的四种可溶性化合物,且已知:①甲+乙→红褐色沉淀;②甲+丙→白色沉淀;③甲+丁→白色沉淀,向甲溶液中逐滴加入丁溶液,其导电能力随丁加入的体积变化曲线如图所示:
下列说法不正确的是
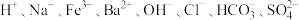 八种离子中的两种(不重复)组成的四种可溶性化合物,且已知:①甲+乙→红褐色沉淀;②甲+丙→白色沉淀;③甲+丁→白色沉淀,向甲溶液中逐滴加入丁溶液,其导电能力随丁加入的体积变化曲线如图所示:
八种离子中的两种(不重复)组成的四种可溶性化合物,且已知:①甲+乙→红褐色沉淀;②甲+丙→白色沉淀;③甲+丁→白色沉淀,向甲溶液中逐滴加入丁溶液,其导电能力随丁加入的体积变化曲线如图所示:
下列说法不正确的是
| A.甲是Ba(OH)2,乙是FeCl3 |
| B.丙是NaHCO3,丁是H2SO4 |
| C.乙溶液中,S2-、Br-、K+可与其大量共存 |
D.少量丙与甲混合的离子反应方程式为 |
更新时间:2023-09-25 08:11:01
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.在水溶液中或熔融状态下能导电的物质称为电解质 |
| B.强酸、强碱和大多数盐属于强电解质 |
| C.自由移动离子数目多,导电能力一定强 |
| D.非金属氧化物都是酸性氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某兴趣小组的同学向一定体积的 溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
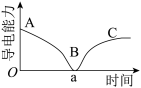
 溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的说法中正确的是
A.AB段溶液的导电能力不断减弱,说明生成的 不是电解质 不是电解质 |
| B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 |
C.BC段溶液的导电能力不断增大,主要是由于过量的 电离出的离子导电 电离出的离子导电 |
D.该过程发生反应的离子方程式为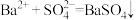 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的有几项
(1)AgCl难溶于水,故属于弱电解质
(2)氨水中存在NH3·H2O分子,故氨水属于弱电解质
(3)稀醋酸加水稀释,电离程度和溶液的pH均增大
(4)稀氨水通入NH3,电离平衡向电离方向移动,溶液导电能力增强
(5)稀醋酸中加入CH3COONa固体,醋酸的电离程度减小,溶液导电能力增强
(6)对于0.1mol/L醋酸溶液,适当加热,溶液中 的值增大
的值增大
(7)将液面在8.20mL处的25mL碱式滴定管中的NaOH溶液全部放出,其体积为16.80mL
(8)中和滴定实验时,滴定管、锥形瓶均用待装溶液润洗
(9)测定中和热时,应迅速将酸、碱稀溶液在有保温措施的容器内混合、搅拌,记录最后温度
(10)用广泛pH试纸测定NaClO溶液的pH为12
(1)AgCl难溶于水,故属于弱电解质
(2)氨水中存在NH3·H2O分子,故氨水属于弱电解质
(3)稀醋酸加水稀释,电离程度和溶液的pH均增大
(4)稀氨水通入NH3,电离平衡向电离方向移动,溶液导电能力增强
(5)稀醋酸中加入CH3COONa固体,醋酸的电离程度减小,溶液导电能力增强
(6)对于0.1mol/L醋酸溶液,适当加热,溶液中
 的值增大
的值增大(7)将液面在8.20mL处的25mL碱式滴定管中的NaOH溶液全部放出,其体积为16.80mL
(8)中和滴定实验时,滴定管、锥形瓶均用待装溶液润洗
(9)测定中和热时,应迅速将酸、碱稀溶液在有保温措施的容器内混合、搅拌,记录最后温度
(10)用广泛pH试纸测定NaClO溶液的pH为12
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是
A.少量 通入 通入 溶液中: 溶液中: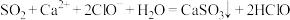 |
B. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
C. 通入 通入 溶液中: 溶液中: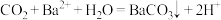 |
D. 和 和 按 按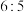 反应: 反应: |
您最近一年使用:0次
单选题
|
适中
(0.64)
名校
【推荐2】能正确表示下列反应的离子方程式为
| A.向Fe(NO3)2稀溶液中加入稀盐酸:Fe2++2H++NO3-=Fe3++NO2↑+H2O |
| B.向(NH4)2Mg(SO4)2溶液中加入少量的Na2O:Mg2++Na2O+H2O =Mg(OH)2↓+2Na+ |
| C.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
| D.向漂白粉溶液中通入SO2:Ca2++ClO-+SO2+H2O=CaSO3↓+ 2HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色NaCl溶液可能存在 、Mg2+、Fe3+、I-、Ba2+、
、Mg2+、Fe3+、I-、Ba2+、 等离子,某学生进行下列实验:①取少量原溶液,测得溶液呈强碱性;②在其中滴加足量氯水和淀粉溶液,产生无色气体,溶液不变色。关于该溶液的推测正确的是
等离子,某学生进行下列实验:①取少量原溶液,测得溶液呈强碱性;②在其中滴加足量氯水和淀粉溶液,产生无色气体,溶液不变色。关于该溶液的推测正确的是
 、Mg2+、Fe3+、I-、Ba2+、
、Mg2+、Fe3+、I-、Ba2+、 等离子,某学生进行下列实验:①取少量原溶液,测得溶液呈强碱性;②在其中滴加足量氯水和淀粉溶液,产生无色气体,溶液不变色。关于该溶液的推测正确的是
等离子,某学生进行下列实验:①取少量原溶液,测得溶液呈强碱性;②在其中滴加足量氯水和淀粉溶液,产生无色气体,溶液不变色。关于该溶液的推测正确的是| A.溶液中可能存在Ba2+和Fe3+ |
B.溶液中一定存在 |
| C.溶液中可能存在I- |
D.无法确定溶液中是否存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某溶液中可能含有 、
、 、
、 中的一种或几种,为确定该溶液的离子组成,现进行如下实验:
中的一种或几种,为确定该溶液的离子组成,现进行如下实验:
①取少量该溶液滴加硝酸钡溶液,产生白色沉淀;②滴加稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的无色气体,白色沉淀部分溶解;③取上层清液继续滴加硝酸钡溶液至无沉淀时,再滴加硝酸银溶液,产生白色沉淀。根据上述实验,以下对原溶液的推测不正确的是( )
 、
、 、
、 中的一种或几种,为确定该溶液的离子组成,现进行如下实验:
中的一种或几种,为确定该溶液的离子组成,现进行如下实验:①取少量该溶液滴加硝酸钡溶液,产生白色沉淀;②滴加稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的无色气体,白色沉淀部分溶解;③取上层清液继续滴加硝酸钡溶液至无沉淀时,再滴加硝酸银溶液,产生白色沉淀。根据上述实验,以下对原溶液的推测不正确的是( )
A.一定有 |
B.一定有 |
C.不能确定 是否存在 是否存在 |
D.不能确定 是否存在 是否存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是( )
| A.向明矾溶液中逐滴滴入Ba(OH)2溶液,至沉淀质量最大时反应为:2Al3++3SO42﹣+3Ba2++6OH﹣═3BaSO4↓+2Al(OH)3↓ |
| B.向澄清石灰水中滴入少量NaHCO3溶液:Ca2++2OH﹣+2HCO3﹣═CaCO3↓+CO32﹣+2H2O |
| C.已知:2Br﹣+Cl2=2Cl﹣+Br2,Br2+2Fe2+=2Fe3++2Br﹣,向含0.2molFeBr2的溶液中通入标准状况下3.36LCl2时,发生的反应为:4Fe2++2Br﹣+3Cl2═4Fe3++Br2+6Cl﹣ |
| D.向NaHSO4中滴入Ba(OH)2溶液至恰好显中性:H++SO42﹣+Ba2++OH﹣═H2O+BaSO4↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式书写正确的是:
A.CuS与浓硝酸反应: |
B. 溶液与过量 溶液与过量 溶液反应: 溶液反应: |
C. 溶于水: 溶于水: |
D.A1溶于NaOH溶液: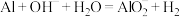 |
您最近一年使用:0次

 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下: 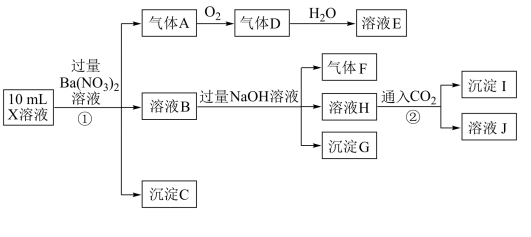
 ,10mL X溶液中
,10mL X溶液中 ,沉淀C物质的量小于
,沉淀C物质的量小于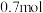 ,根据以上信息,下列说法正确的是
,根据以上信息,下列说法正确的是
 可知,气体A一定是NO,沉淀C一定是
可知,气体A一定是NO,沉淀C一定是 可知,沉淀I可能是
可知,沉淀I可能是 和
和


