已知:①

②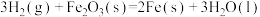

③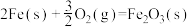

则 为
为  (用a、b表示)
(用a、b表示)


②
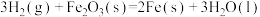

③
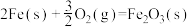

则
 为
为  (用a、b表示)
(用a、b表示)A.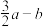 | B.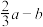 | C.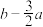 | D.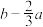 |
更新时间:2023-11-02 20:32:31
|
【知识点】 盖斯定律及其有关计算
相似题推荐
【推荐1】已知2H2O(l)=2H2(g)+O2(g) ∆H=+571.0 kJ·mol-1,两步热循环制H2的过程如图。下列说法正确的是
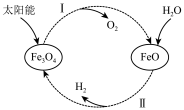
过程I:2Fe3O4(s)=6FeO(s)+O2(g) ∆HⅠ =+604.8 kJ·mol-1
过程II:H2O(l)+3FeO(s)=Fe3O4(s)+H2(g) ∆H II

过程I:2Fe3O4(s)=6FeO(s)+O2(g) ∆HⅠ =+604.8 kJ·mol-1
过程II:H2O(l)+3FeO(s)=Fe3O4(s)+H2(g) ∆H II
| A.该制氢过程中FeO为催化剂 |
| B.整个过程中能量转化形式只存在太阳能转化为化学能 |
| C.过程II在任何温度下均为自发反应 |
| D.根据盖斯定律∆H I+∆H II=0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】羰基硫(COS)常作粮食的熏蒸剂,一种制备原理如下:
 ∆H1,其反应分两步进行:
∆H1,其反应分两步进行:
①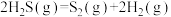 ∆H2
∆H2
② ∆H3
∆H3
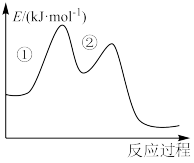
反应的能量变化如图所示。下列说法正确的是
 ∆H1,其反应分两步进行:
∆H1,其反应分两步进行:①
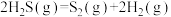 ∆H2
∆H2②
 ∆H3
∆H3反应的能量变化如图所示。下列说法正确的是

| A.∆H1、∆H2、∆H3都小于0 | B.活化能:①>② |
C. 是总反应的催化剂 是总反应的催化剂 | D.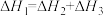 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:
CH3OH(1)+O2(g)=CO(g)+2H2O(g) ΔH1=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
CH3OH(1)+O2(g)=CO(g)+2H2O(g) ΔH1=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
| A.CO的燃烧热为﹣566.0kJ•mol﹣1 |
| B.2molCO和1molO2的总能量比2molCO2的总能量低 |
| C.完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3kJ |
| D.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g) ΔH=﹣1453.28kJ•mol﹣1 |
您最近一年使用:0次



