下列热化学方程式正确的是
A.表示硫的燃烧热的热化学方程式: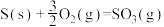  |
B.表示肼( )的燃烧热的热化学方程式: )的燃烧热的热化学方程式: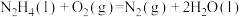   |
C.表示乙烷的燃烧热的热化学方程式: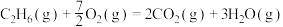 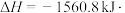  |
D.表示CO燃烧热的热化学方程式: 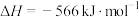 |
更新时间:2023-11-05 20:14:10
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-801.3KJ/mol结论:CH4的燃烧热为801.3KJ |
B.Sn(s,灰) Sn(s,白);ΔH=+2.1KJ/mol(灰锡为粉末状)结论:锡制品在寒冷的冬天因易转化为灰锡而损坏 Sn(s,白);ΔH=+2.1KJ/mol(灰锡为粉末状)结论:锡制品在寒冷的冬天因易转化为灰锡而损坏 |
| C.稀溶液中有:H+(aq)+OH-(aq)=H2O(l);ΔH=-57.3KJ/mol结论:将盐酸与氨水的稀溶液混合后,若生成1molH2O,则会放出57.3KJ的能量 |
| D.C(s,金刚石)+O2(g)=CO2(g);ΔH=-395kJ·mol-1 结论:相同条件下金刚石性质比石墨稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列四幅图示所表示的信息与对应的叙述相符的是
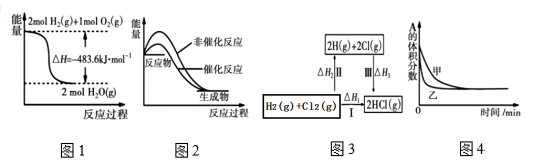

| A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ·mol−1 |
| B.图2表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C.图3表示一定条件下H2和Cl2生成HCl的反应热与途径无关,则 △H1=△H2+△H3 |
D.图4表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知25℃、101 KPa下,10 kg丁烷(C4H10)完全燃烧生成CO2和液态水时,放出5×105kJ的热量,下列热化学方程式书写正确的是
A.C4H10 +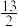 O2 = 4CO2 +5H2O △H= -2900 kJ/mol O2 = 4CO2 +5H2O △H= -2900 kJ/mol |
B.C4H10(l) +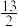 O2(g) = 4CO2(g) +5H2O(l) △H=+2900 kJ/mol O2(g) = 4CO2(g) +5H2O(l) △H=+2900 kJ/mol |
C.C4H10(l)+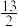 O2(g) = 4CO2(g)+5H2O(g) △H= -2900 kJ/mol O2(g) = 4CO2(g)+5H2O(g) △H= -2900 kJ/mol |
| D.2C4H10(l)+13O2(g)= 8CO2(g)+10H2O(l) △H= -5800 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法中正确的选项是
①已知25℃时H2(g)的燃烧热是285.8 kJ·mol-1,则323.15K、101kPa时,2H2O(l) =2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
②中和热测定实验中为减少热量散失,NaOH溶液应分多次到入量热计中。
③同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下反应的ΔH不同
④由N2O4(g) 2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ
2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ
⑤在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量为57.3 kJ
⑥煤、石油、天然气均为化石能源,是非再生能源
⑦已知相同条件下2SO2(g)+O2(g) 2SO3(g) ΔH1,反应2SO2(g)+O2(g)
2SO3(g) ΔH1,反应2SO2(g)+O2(g)  2SO3(s) ΔH2,则ΔH1>ΔH2
2SO3(s) ΔH2,则ΔH1>ΔH2
⑧C(石墨,s)=C(金刚石,s) ΔH >0,说明石墨比金刚石稳定
①已知25℃时H2(g)的燃烧热是285.8 kJ·mol-1,则323.15K、101kPa时,2H2O(l) =2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
②中和热测定实验中为减少热量散失,NaOH溶液应分多次到入量热计中。
③同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下反应的ΔH不同
④由N2O4(g)
 2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ
2NO2(g) ΔH=-56.9 kJ·mol-1,可知将1 mol N2O4(g)置于密闭容器中充分反应后放出热量为56.9 kJ⑤在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量为57.3 kJ
⑥煤、石油、天然气均为化石能源,是非再生能源
⑦已知相同条件下2SO2(g)+O2(g)
 2SO3(g) ΔH1,反应2SO2(g)+O2(g)
2SO3(g) ΔH1,反应2SO2(g)+O2(g)  2SO3(s) ΔH2,则ΔH1>ΔH2
2SO3(s) ΔH2,则ΔH1>ΔH2⑧C(石墨,s)=C(金刚石,s) ΔH >0,说明石墨比金刚石稳定
| A.0项 | B.1项 | C.3项 | D.4项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】沼气是一种能源,它的主要成分是CH4,常温下0.5molCH4完全燃烧生成CO2和水时,放出445kJ热量,则下列热化学方程式中正确的是
| A.2CH4(g)+4O2(g)=2CO2(g)+4H2O(g) ΔH=+890kJ·mol-1 |
| B.CH4(g)+2O2(g)= CO2(g)+2H2O(g) ΔH=+445kJ·mol-1 |
| C.CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH=-890kJ·mol-1 |
| D.2CH4(g)+4O2(g)=2CO2(g)+4H2O(l) ΔH=-890kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关说法正确的是
| A.已知:① C(s石墨)+O2(g)=CO2(g) ∆H1= -393.5 kJ/mol,②C(s金刚石)+O2(g)=CO2(g) ∆H2= -395.0 kJ/mol,则金刚石比石墨稳定 |
| B.在101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ热量,H2燃烧热为-285.8 kJ/mol |
| C.一定条件下2SO2(g)+O2(g)⇌2SO3(g) △H1,2SO2(g)+O2(g)⇌2SO3(l) △H2则△H1>△H2 |
| D.在一定温度和压强下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为 N2(g)+3H2(g)⇌2NH3(g) △H=﹣38.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列热化学方程式中ΔH能表示可燃物燃烧热的是( )
| A.2H2(g) + O2(g) = 2H2O(g) ΔH= -483.6kJ·mol-1 |
B.CO(g) + O2(g) = CO2(g) ΔH= -283kJ·mol-1 O2(g) = CO2(g) ΔH= -283kJ·mol-1 |
| C.CH4(g) + 2O2(g) = CO2(g) +2H2O(g) ΔH= -802kJ·mol-1 |
D.C(s) + O2(g) = CO(g) ΔH= -108kJ·mol-1 O2(g) = CO(g) ΔH= -108kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法或表示方法中正确的是
| A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g)ΔH=-38.6kJ·mol-1 2NH3(g)ΔH=-38.6kJ·mol-1 |
| C.等质量的硫蒸气和硫磺(s)分别完全燃烧,前者放出的热量多 |
| D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中和,放出28.7kJ的热量 |
您最近一年使用:0次

 O2(g)=2CO2(g)+H2O(l)ΔH=-2b kJ·mol-1
O2(g)=2CO2(g)+H2O(l)ΔH=-2b kJ·mol-1 O2(g)=SO3(g)ΔH=-315 kJ·mol-1
O2(g)=SO3(g)ΔH=-315 kJ·mol-1

