从不同的角度对物质进行分类有利于研究物质的组成与性质。现有以下物质:①Cu②NaC1③盐酸④KHSO4晶体⑤干冰⑥熔融NaOH⑦SiO2⑧Fe(OH)3胶体⑨蔗糖固体。回答下列问题:
(1)以上物质属于氧化物的有___________ (填序号)。
(2)以上物质能导电的有___________ (填序号)。
(3)以上物质属于电解质的有___________ (填序号)。
(4)以上物质属于非电解质的有___________ (填序号)。
(5)实验室制备⑧的化学反应方程式为___________ 。
(1)以上物质属于氧化物的有
(2)以上物质能导电的有
(3)以上物质属于电解质的有
(4)以上物质属于非电解质的有
(5)实验室制备⑧的化学反应方程式为
更新时间:2023-11-07 15:26:12
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】利用如图可从不同角度研究含氯物质的性质及具转化关系。回答下列问题:

(1)a物质的化学式为____ ,b属于____ (填“酸性”或“碱性”)氧化物。
(2)用Cl2O消毒水时,Cl2O还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH)3胶体,说明Cl2O具有____ 性,检验有胶体生成的简便方法是____ 。
(3)工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4制备Cl2O,若生成1molCl2O,则反应中转移电子的物质的量为____ 。
(4)实验室可用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的离子方程式:____ ;一般Cl2都用NaOH溶液吸收,请写出该反应的化学方程式:_____ 。

(1)a物质的化学式为
(2)用Cl2O消毒水时,Cl2O还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH)3胶体,说明Cl2O具有
(3)工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4制备Cl2O,若生成1molCl2O,则反应中转移电子的物质的量为
(4)实验室可用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】酸的主要化学性质
[思考] 从微观角度来看,不同的酸溶液中都含有___________ ,故酸的化学通性都由___________ 体现。
| 酸的主要化学性质 | 反应实例(以盐酸为例,写出化学方程式) |
| (1)与活泼金属反应 | |
| (2)与碱性氧化物反应 | |
| (3)与碱反应 | |
| (4)与某些盐反应 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求完成下列习题
(1)以下物质:①冰水混合物、②空气、③Mg、④CaO、⑤H2SO4、⑥Ca(OH)2、⑦CuSO4·H2O、⑧液氧、⑨NaHCO3。其中,属于混合物的是_______ (填序号,下同)属于氧化物的是_______ ;属于酸的是_______ ;属于碱的是_______ ;属于电解质的是_______
(2)如何制备Fe(OH)3胶体(用文字表达过程)_______ ,实验室制备Fe(OH)3胶体的化学方程式为_______ 。
(3)鉴别Fe(OH)3胶体和FeCl3溶液最简单的方法是_______ 。(填字母)
a.观察液体颜色 b.丁达尔效应 c.加入AgNO3溶液是否出现沉淀
(1)以下物质:①冰水混合物、②空气、③Mg、④CaO、⑤H2SO4、⑥Ca(OH)2、⑦CuSO4·H2O、⑧液氧、⑨NaHCO3。其中,属于混合物的是
(2)如何制备Fe(OH)3胶体(用文字表达过程)
(3)鉴别Fe(OH)3胶体和FeCl3溶液最简单的方法是
a.观察液体颜色 b.丁达尔效应 c.加入AgNO3溶液是否出现沉淀
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生的反应的化学方程式为___________ ;该反应的离子方程式为___________ ;反应后所得溶液为___________ 色。用此溶液进行以下反应。
(2)取少量溶液于一支试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为___________ ;
(3)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至溶液变成红褐色,即可制得___________ ;
(4)另取一个小烧杯,也加入25mL蒸馏水,向烧杯中加入1mLFeCl3溶液,振荡摇匀后,将此烧杯甲与(3)中的烧杯乙一起放置在暗处,用激光笔照射杯中的液体,可看到___________ 烧杯中的液体有丁达尔效应。
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生的反应的化学方程式为
(2)取少量溶液于一支试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为
(3)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至溶液变成红褐色,即可制得
(4)另取一个小烧杯,也加入25mL蒸馏水,向烧杯中加入1mLFeCl3溶液,振荡摇匀后,将此烧杯甲与(3)中的烧杯乙一起放置在暗处,用激光笔照射杯中的液体,可看到
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】FeCl3是中学实验室常用的试剂。
(1)写出氯化铁在水中的电离方程式:_________ 。
(2)利用氯化铁溶液制备氢氧化铁胶体。
①下列制备氢氧化铁胶体的操作方法正确的是_______ (填字母)。
A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体
②区别氯化铁溶液和氢氧化铁胶体的方法是___________ 。
(3)为了探究离子反应的本质,设计如下实验:

写出生成A的离子方程式:_________ 。
(1)写出氯化铁在水中的电离方程式:
(2)利用氯化铁溶液制备氢氧化铁胶体。
①下列制备氢氧化铁胶体的操作方法正确的是
A.向饱和氯化铁溶液中滴加适量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至出现红褐色液体
②区别氯化铁溶液和氢氧化铁胶体的方法是
(3)为了探究离子反应的本质,设计如下实验:

写出生成A的离子方程式:
您最近一年使用:0次
【推荐3】 是一种重要的工业原料。
是一种重要的工业原料。
(1)取少量 粉末(红棕色),加入适量盐酸,发生反应的离子方程式为
粉末(红棕色),加入适量盐酸,发生反应的离子方程式为__________________ 。
用上述溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,反应的化学方程式为__________________ 。
(3)在小烧杯中加入蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至液体呈______ 色,即可制得Fe(OH)3胶体。
(4)已知强酸氢碘酸(HI)具有较强的还原性。取上述烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的HI稀溶液,边滴边振荡,会出现一系列变化。先出现红褐色沉淀,原因是__________________ 。随后沉淀溶解,溶液呈黄色,最后溶液颜色加深。若此时向该溶液中加淀粉溶液,溶液变蓝,请写出Fe(OH)3与 反应的离子方程式:
反应的离子方程式:__________________ 。
(5)已知氧化性: ,则向FeBr2溶液中通入等物质的量的Cl2发生反应的总离子方程式为
,则向FeBr2溶液中通入等物质的量的Cl2发生反应的总离子方程式为__________________ ,向FeI2溶液中通入等物质的量的Cl2发生反应的总离子方程式为__________________ 。
 是一种重要的工业原料。
是一种重要的工业原料。(1)取少量
 粉末(红棕色),加入适量盐酸,发生反应的离子方程式为
粉末(红棕色),加入适量盐酸,发生反应的离子方程式为用上述溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,反应的化学方程式为
(3)在小烧杯中加入蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸直至液体呈
(4)已知强酸氢碘酸(HI)具有较强的还原性。取上述烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的HI稀溶液,边滴边振荡,会出现一系列变化。先出现红褐色沉淀,原因是
 反应的离子方程式:
反应的离子方程式:(5)已知氧化性:
 ,则向FeBr2溶液中通入等物质的量的Cl2发生反应的总离子方程式为
,则向FeBr2溶液中通入等物质的量的Cl2发生反应的总离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.有下列物质:①氢氧化钠固体、②铜丝、③氯化氢气体、④稀硫酸、⑤干冰、⑥氨水、⑦碳酸钠粉末、⑧蔗糖晶体、⑨熔融氯化钠、⑩ 晶体。请用序号回答问题:
晶体。请用序号回答问题:
(1)属于电解质的是___________ 。
(2)属于非电解质的是___________ 。
(3)上述状态下可导电的是___________ 。
(4)上述状态下的电解质不能导电的是___________ 。
Ⅱ.请写出下列物质溶于水的电离方程式。
(5) :
:___________ 。
(6) :
:___________ 。
(7) :
:___________ 。
 晶体。请用序号回答问题:
晶体。请用序号回答问题:(1)属于电解质的是
(2)属于非电解质的是
(3)上述状态下可导电的是
(4)上述状态下的电解质不能导电的是
Ⅱ.请写出下列物质溶于水的电离方程式。
(5)
 :
:(6)
 :
:(7)
 :
:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求完成下列填空。
(1)对于混合物的分离或提纯,常采用的方法有“过滤、蒸发、蒸馏、萃取、渗析、加热分解”等。
下列各组混和物的分离或提纯应采用什么方法:
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用__ 的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
②实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用__ 的方法除去Fe(OH)3胶体中混有的杂质Cl-离子。
③除去乙醇中溶解的微量食盐可采用__ 的方法。
(2)现有下列七种物质:①铝②蔗糖③CO2④H2SO4⑤Ba(OH)2⑥红褐色的氢氧化铁胶体⑦HCl⑧冰水混合物⑨碳酸钙⑩CuSO4·5H2O。
①上述物质中属于电解质的有__ (填序号)。
②向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是__ 。
(1)对于混合物的分离或提纯,常采用的方法有“过滤、蒸发、蒸馏、萃取、渗析、加热分解”等。
下列各组混和物的分离或提纯应采用什么方法:
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用
②实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用
③除去乙醇中溶解的微量食盐可采用
(2)现有下列七种物质:①铝②蔗糖③CO2④H2SO4⑤Ba(OH)2⑥红褐色的氢氧化铁胶体⑦HCl⑧冰水混合物⑨碳酸钙⑩CuSO4·5H2O。
①上述物质中属于电解质的有
②向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学源自生活和生产实践,并随着人类社会的进步而不断发展。根据所学知识,回答下列问题:
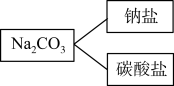
(1)分类是认识和研究物质及其变化的一种常用的科学方法,如图所示分类方法是______ (选填“树状分类法”或“交叉分类法”)。
(2)氢化钠(NaH)可在野外用作生氢剂,其原理为NaH+H2O=NaOH+H2↑,该反应的还原剂是______ (填化学式),生成1molH2转移的电子数目为______ 。
(3)碳酸钠是一种重要的化工基本原料,俗称______ ,向碳酸钠溶液中滴加少量稀盐酸,会生成NaCl和______ (填化学式)。除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法是______ (用化学方程式表达)。
(4)下列物质:①液氯②盐酸③CO2④硝酸钾固体⑤熔融NaHSO4;⑥铝,其中属于电解质的是______ (填序号,后同),能导电的是______ ,⑤的电离方程式为______ 。
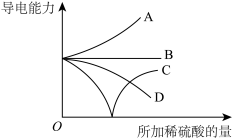
(5)向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中______ (填字母)所示。
(6)把5.1g镁铝合金(不含其他杂质)的粉末放入过量的盐酸中,充分反应后得到5.6LH2(标准状况),该合金中铝和镁的物质的量之比为______ 。
(1)分类是认识和研究物质及其变化的一种常用的科学方法,如图所示分类方法是

(2)氢化钠(NaH)可在野外用作生氢剂,其原理为NaH+H2O=NaOH+H2↑,该反应的还原剂是
(3)碳酸钠是一种重要的化工基本原料,俗称
(4)下列物质:①液氯②盐酸③CO2④硝酸钾固体⑤熔融NaHSO4;⑥铝,其中属于电解质的是
(5)向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中

(6)把5.1g镁铝合金(不含其他杂质)的粉末放入过量的盐酸中,充分反应后得到5.6LH2(标准状况),该合金中铝和镁的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥熔融氢氧化钾;⑦石墨;⑧氨水;⑨空气;⑩硫酸铁溶液.
(1)上述十种物质中,属于电解质的有_____ 。
(2)能导电的有_____ 。
(3)有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为_____ 。
(4)实验室制备物质④的离子方程式是_____ 。
(5)物质⑩的电离方程式是:______ 。
(1)上述十种物质中,属于电解质的有
(2)能导电的有
(3)有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,该反应的化学方程式为
(4)实验室制备物质④的离子方程式是
(5)物质⑩的电离方程式是:
您最近一年使用:0次

 c.
c. d.
d. 单质 e.乙醇 f.醋酸 g.
单质 e.乙醇 f.醋酸 g. h.
h. 溶液 i.
溶液 i. 晶体
晶体

