原电池原理在工农业生产、日常生活、科学研究中具有广泛的应用。
(1)甲酸是基本有机化工原料之一,广泛用于农药、皮革、染料、医约和橡胶等工业。某科研团队利用光催化制甲酸如图所示:已知: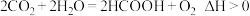 。
。
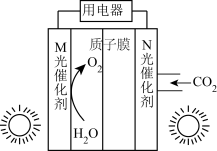
①两个电极中,电极电势较高的电极是___________ (填“M”或“N”)。
②正极电极反应式为___________ 。
③若制得 ,不考虑气体溶解,整套装置质量增加
,不考虑气体溶解,整套装置质量增加___________ g。
(2)热激活电池主要用于导弹、火箭以及应急电子仪器供电,是一种电解质受热熔融即可开始工作的电池。一种热激活电池的结构如图所示。
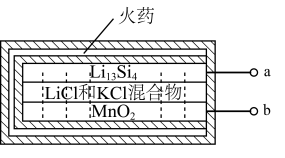
已知放电后的两极产物分别为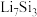 和
和 ,则a极的电极方程式为
,则a极的电极方程式为___________ 。
(3)我国《政府工作报告》写入“推动充电、加氢等设施的建设”。如下图是一种新型“全氢电池”,能量效率可达 。
。
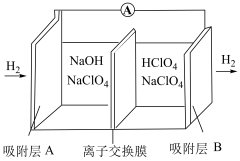
①该电池的总反应方程式为___________ 。
②该电池工作一段时间后,离子交换膜右侧质量增大,则透过离子交换膜迁移的离子是___________ 。
③该电池以恒定电流2A输出,当电池左侧消耗标况下 时,可持续对外供电
时,可持续对外供电___________ 小时(已知法拉第常数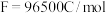 ,计算结果保留到整数)。
,计算结果保留到整数)。
(1)甲酸是基本有机化工原料之一,广泛用于农药、皮革、染料、医约和橡胶等工业。某科研团队利用光催化制甲酸如图所示:已知:
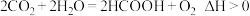 。
。
①两个电极中,电极电势较高的电极是
②正极电极反应式为
③若制得
 ,不考虑气体溶解,整套装置质量增加
,不考虑气体溶解,整套装置质量增加(2)热激活电池主要用于导弹、火箭以及应急电子仪器供电,是一种电解质受热熔融即可开始工作的电池。一种热激活电池的结构如图所示。

已知放电后的两极产物分别为
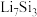 和
和 ,则a极的电极方程式为
,则a极的电极方程式为(3)我国《政府工作报告》写入“推动充电、加氢等设施的建设”。如下图是一种新型“全氢电池”,能量效率可达
 。
。
①该电池的总反应方程式为
②该电池工作一段时间后,离子交换膜右侧质量增大,则透过离子交换膜迁移的离子是
③该电池以恒定电流2A输出,当电池左侧消耗标况下
 时,可持续对外供电
时,可持续对外供电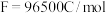 ,计算结果保留到整数)。
,计算结果保留到整数)。
更新时间:2023-10-02 16:04:48
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置:
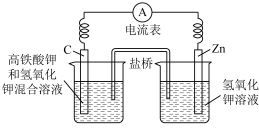
①该电池放电时正极的电极反应式为____________________ ;若维持电流强度为1 A,电池工作十分钟,理论上消耗Zn______ g(计算结果保留一位小数,已知F=96500 C·mol-1)。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向______ (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向________ (填“左”或“右”)移动。
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________ 。
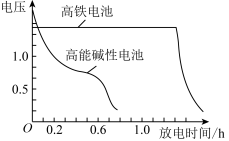
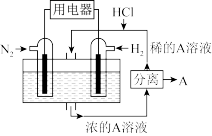
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是__________________________ ,A是________ 。
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON (固溶体)内自由移动,工作时O2-的移动方向________ (填“从a到b”或“从b到a”),负极发生的电极反应式为__________________________ 。
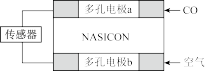

①该电池放电时正极的电极反应式为
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是

(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON (固溶体)内自由移动,工作时O2-的移动方向
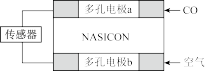
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
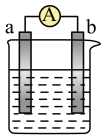
【推荐2】(1)下图是某化学兴趣小组探究化学能转变为电能的装置,若依据氧化还原反应: Cu+2Fe3+= Cu2++2Fe2+设计原电池,电极a为石墨、则电极b为电池的______ 极,发生的电极反应式为:___________ ,电极a上发生的电极反应为_____ (填“氧化”或“还原"反应。
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为某种甲烷燃料电池示意图,工作时电子流向如图所示。
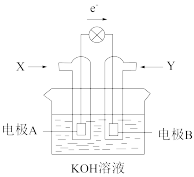
写出电极A的电极方程式________________ ,电极A附近pH如何变化?______________ (填“变大”或“变小”)。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4- SOCl2。电池的总反应可表示为:4Li+2SOCl= 4LiCl+S+ SO2。已知SOCl2会与水反应有刺激性气味的气体生成:SOCl2+ H2O=2HCl↑+ SO2↑。电池的负极材料为_________ ; 电池正极发生的电极反应式为_________ ;组装该电池必须在无水、无氧的条件下进行,原因是______________ 。

(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为某种甲烷燃料电池示意图,工作时电子流向如图所示。

写出电极A的电极方程式
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4- SOCl2。电池的总反应可表示为:4Li+2SOCl= 4LiCl+S+ SO2。已知SOCl2会与水反应有刺激性气味的气体生成:SOCl2+ H2O=2HCl↑+ SO2↑。电池的负极材料为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】回答下列问题
(1)二氧化氯具有杀菌、漂白、除臭、消毒、保鲜的功能。电解法制取 的新工艺如图所示。
的新工艺如图所示。
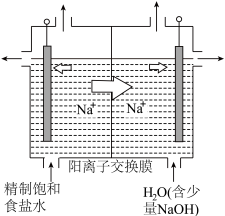
①用石墨作电极,在一定条件下电解饱和食盐水制取 (如图所示),阳极产生
(如图所示),阳极产生 的电极反应式为
的电极反应式为________ 。
②电解一段时间,当阴极产生的气体体积为 (标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为________  。
。
(2)粗银精炼装置如图所示,电解液为稀硫酸。
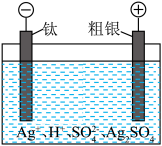
①阳极的电极反应式为________ 。
②下列说法正确的是________ (填字母)。
a.一段时间后,阳极质量减小
b.阴极区可获得银单质的原理:
c.体系中存在沉淀溶解平衡: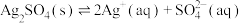
(3)一种用于心脏起搏器的微型电池具有容量大、寿命长和电压稳定等特点。该电池的电极材料是石墨和锂,电解质溶液为等物质的量的 、
、 溶解在
溶解在 中形成的溶液。这种电池的总反应为
中形成的溶液。这种电池的总反应为 。
。
①锂电极的电势比石墨电极的________ (填“低”或“高”)。
②放电时,石墨电极发生________ (填“氧化”或“还原”)反应。
③电池的正极反应为________ 。
(1)二氧化氯具有杀菌、漂白、除臭、消毒、保鲜的功能。电解法制取
 的新工艺如图所示。
的新工艺如图所示。
①用石墨作电极,在一定条件下电解饱和食盐水制取
 (如图所示),阳极产生
(如图所示),阳极产生 的电极反应式为
的电极反应式为②电解一段时间,当阴极产生的气体体积为
 (标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为 。
。(2)粗银精炼装置如图所示,电解液为稀硫酸。

①阳极的电极反应式为
②下列说法正确的是
a.一段时间后,阳极质量减小
b.阴极区可获得银单质的原理:

c.体系中存在沉淀溶解平衡:
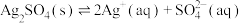
(3)一种用于心脏起搏器的微型电池具有容量大、寿命长和电压稳定等特点。该电池的电极材料是石墨和锂,电解质溶液为等物质的量的
 、
、 溶解在
溶解在 中形成的溶液。这种电池的总反应为
中形成的溶液。这种电池的总反应为 。
。①锂电极的电势比石墨电极的
②放电时,石墨电极发生
③电池的正极反应为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】 自重轻、体积小、容量大、使用安全、环保是新型电池的典型特点,回答下列问题:
I.“阿波罗”飞船中使用的氢氧燃料电池部分结构如图所示。
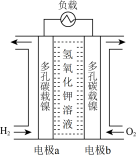
(1)电池的正极为电极___________ (填“a”或“b”),其表面上发生的电极反应为___________ (填电极反应式)。
(2)“神舟”飞船是中国自行研制的,具有自主知识产权的载人飞船,其返回舱使用的是银锌蓄电池组。银锌电池结构如图所示,放电时总反应为 。电池放电时负极质量
。电池放电时负极质量___________ (填“增大”、“减小”或“不变”),电池放电时电解质溶液的
___________ (填“增大”、“减小”或“不变”)。

Ⅱ.非水系锂氧(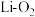 )电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许
)电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许 通过。
通过。

(3)放电时,电池的总反应为___________ ;电解液a不选用 水溶液的原因可能是
水溶液的原因可能是___________ 。
(4)不考虑其他副反应,若放电前两电极质量完全相同,放电时,电路中转移1mole-,正、负电极的质量之差为___________ g(假设生成的不溶物全覆盖在电极表面,生成的可溶物全部扩散至电解液中,参与电极反应的物质均过量)。(相对原子质量:Li~7 O~16 )
I.“阿波罗”飞船中使用的氢氧燃料电池部分结构如图所示。

(1)电池的正极为电极
(2)“神舟”飞船是中国自行研制的,具有自主知识产权的载人飞船,其返回舱使用的是银锌蓄电池组。银锌电池结构如图所示,放电时总反应为
 。电池放电时负极质量
。电池放电时负极质量

Ⅱ.非水系锂氧(
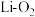 )电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许
)电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许 通过。
通过。
(3)放电时,电池的总反应为
 水溶液的原因可能是
水溶液的原因可能是(4)不考虑其他副反应,若放电前两电极质量完全相同,放电时,电路中转移1mole-,正、负电极的质量之差为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
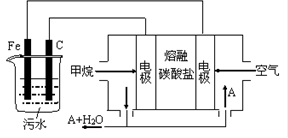
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的____________ 。
a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向____ 极(填:“正”或“负”或“阴”或“阳”)。
(3)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ. Fe-2e-=Fe2+ Ⅱ.______________________________________ 。
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是____________________________________________ ;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为__________ 。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)_________ L。

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的
a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向
(3)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ. Fe-2e-=Fe2+ Ⅱ.
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)
您最近一年使用:0次
【推荐3】新能源汽车所用蓄电池分为铅酸蓄电池、二次锂电池、空气电池等类型。请回答下列问题:
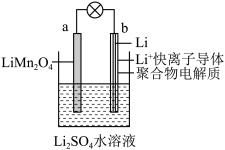
(1)2019年诺贝尔化学奖授予了为锂离子电池发展做出贡献的约翰·班宁斯特·古迪纳夫等三位科学家。如图所示为水溶液锂离子电池体系。放电时,电池的负极是_______ (填a或b),溶液中Li+从______ 迁移(填“a向b”或“b向a”)。
(2)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
①放电时,正极的电极反应式是________________________ ,电解质溶液中硫酸的浓度_____ (填“增大”、“减小”或“不变”),当外电路通过0.5 mol e-时,理论上负极板的质量增加_______ g。
②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如下图所示,电解液c选用________ 溶液,A电极的材料是_______ ,B电极反应式是_________ 。
③用该蓄电池作电源,A、B为石墨电极,c为氯化钠溶液,进行电解。如上图所示,则A电极产生的气体是________ ,B电极附近溶液的pH_____ (填“增大”、“减小”或“不变”)。
(1)2019年诺贝尔化学奖授予了为锂离子电池发展做出贡献的约翰·班宁斯特·古迪纳夫等三位科学家。如图所示为水溶液锂离子电池体系。放电时,电池的负极是

(2)铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为Pb(s)+PbO2(s)+2H2SO4(aq)
 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)①放电时,正极的电极反应式是
②用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。如下图所示,电解液c选用
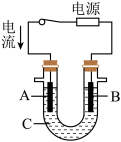
③用该蓄电池作电源,A、B为石墨电极,c为氯化钠溶液,进行电解。如上图所示,则A电极产生的气体是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】请回答下列问题:
I:某兴趣小组依据反应 探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。
探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。________ (填“有”或“无”,下同)氧化还原反应发生,导线上________ 电流产生。
(2)连接K,锌片上的电极反应式为________ 。 后测得锌片和铜片之间的质量差为
后测得锌片和铜片之间的质量差为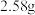 ,则导线中通过电子的物质的量为
,则导线中通过电子的物质的量为________  。
。
(3)若连接K一段时间后,实际测得铜片质量增加 ,同时锌片质量减少
,同时锌片质量减少 ,那么这段时间内该装置消耗的化学能转化为电能的百分比为
,那么这段时间内该装置消耗的化学能转化为电能的百分比为________ 。
II:常温下,将除去表面氧化膜的铝片、铜片插入浓 中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间
中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间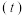 的变化如图乙所示,反应过程中有红棕色气体产生。
的变化如图乙所示,反应过程中有红棕色气体产生。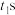 前,该原电池的正极反应式为
前,该原电池的正极反应式为________ 。
(5)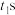 后,外电路中电子流动方向发生改变,原因是
后,外电路中电子流动方向发生改变,原因是________ 。
I:某兴趣小组依据反应
 探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。
探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。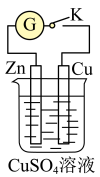
(2)连接K,锌片上的电极反应式为
 后测得锌片和铜片之间的质量差为
后测得锌片和铜片之间的质量差为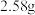 ,则导线中通过电子的物质的量为
,则导线中通过电子的物质的量为 。
。(3)若连接K一段时间后,实际测得铜片质量增加
 ,同时锌片质量减少
,同时锌片质量减少 ,那么这段时间内该装置消耗的化学能转化为电能的百分比为
,那么这段时间内该装置消耗的化学能转化为电能的百分比为II:常温下,将除去表面氧化膜的铝片、铜片插入浓
 中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间
中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间 的变化如图乙所示,反应过程中有红棕色气体产生。
的变化如图乙所示,反应过程中有红棕色气体产生。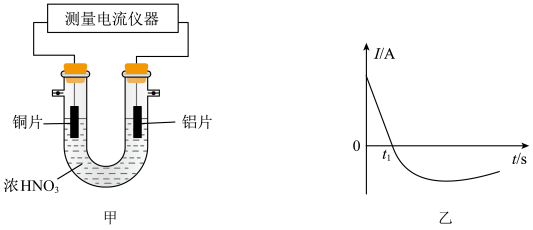
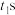 前,该原电池的正极反应式为
前,该原电池的正极反应式为(5)
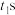 后,外电路中电子流动方向发生改变,原因是
后,外电路中电子流动方向发生改变,原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】我国科学家最近发明了一种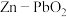 电池,电解质为
电池,电解质为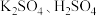 和
和 ,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
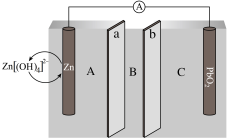
回答下列问题:
(1)电池中, 为
为_____ 极,B区域的电解质为_____ (填“ ”“
”“ ”或“
”或“ ”)。
”)。
(2)电池反应的离子方程式为_______ 。
(3)阳离子交换膜为图中的_______ (填“a”或“b”)膜。
(4)此电池中,消耗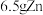 ,理论上可产生的容量(电量)为
,理论上可产生的容量(电量)为_______ 毫安时 (
( 电子的电量为
电子的电量为 ,
, ,结果保留整数)。
,结果保留整数)。
(5)已知E为电池电动势[电池电动势即电池的理论电压,是两个电极电位之差, ],
], 为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较,
为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较,
______  ;
;
_______  (填“>”或“<”)。
(填“>”或“<”)。
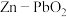 电池,电解质为
电池,电解质为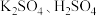 和
和 ,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
回答下列问题:
(1)电池中,
 为
为 ”“
”“ ”或“
”或“ ”)。
”)。(2)电池反应的离子方程式为
(3)阳离子交换膜为图中的
(4)此电池中,消耗
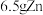 ,理论上可产生的容量(电量)为
,理论上可产生的容量(电量)为 (
( 电子的电量为
电子的电量为 ,
, ,结果保留整数)。
,结果保留整数)。(5)已知E为电池电动势[电池电动势即电池的理论电压,是两个电极电位之差,
 ],
], 为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较,
为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较,
 ;
;
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
【推荐3】根据下列要求回答下列问题。
(1)次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图:

则Co的电极反应式为___________ ,A、B、C为离子交换膜,其中B为___________ 离子交换膜(填“阳”或“阴”)。
(2)我国科研人员研制出的可充电“NaCO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:

①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是___________ 。
(1)次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图:

则Co的电极反应式为
(2)我国科研人员研制出的可充电“NaCO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是
您最近一年使用:0次



