汽车的启动电源常用铅酸蓄电池,该电池在放电时的总反应为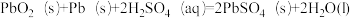 。
。
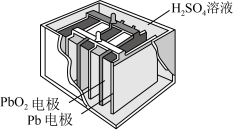
下列说法正确的是
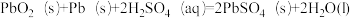 。
。
下列说法正确的是
| A.该铅酸蓄电池属于一次电池 |
B.负极的电极反应式为 |
| C.铅酸蓄电池放电时,每转移0.2mol电子消耗0.4molH2SO4 |
| D.电池放电时,两电极质量均增加,且每转移1mol电子,电池正极质量增加32g |
更新时间:2023-10-05 15:59:09
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意如图。下列有关该电池说法正确的是


| A.B电极发生还原反应 |
| B.A电极上发生的一个电极反应为:2Li++S8+2e-=Li2S8 |
| C.每生成1mol Li2S8转移0.25mol电子 |
| D.电子从B电极经过外电路流向A电极,再经过电解质流回B电极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】由我国科学家研发成功的铝锰电池是一种比能量很高的新型干电池,以氯化钠和稀氨水混合溶液为电解质,铝和二氧化锰石墨为两极,其电池反应为Al+3MnO2+3H2O=3MnO(OH)+Al(OH)3。下列有关该电池放电时的说法不正确的是( )
| A.二氧化锰石墨为电池正极 |
B.负极反应式为Al-3e-+3NH3·H2O=Al(OH)3+3 |
| C.OH-不断由负极向正极移动 |
| D.每生成1 mol MnO(OH)转移1 mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】高温时通过以下反应制备金属铝。用铝制作的“快速放电铝离子二次电池”的原理如右图所示(EMI+为有机阳离子)。

①Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) ΔH1=a kJ·mol-1
②3AlCl(g)===2Al(l)+AlCl3(g) ΔH2=b kJ·mol-1
③Al2O3(s)+3C(s)===2Al(l)+3CO(g) ΔH3
下列说法正确的是( )

①Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) ΔH1=a kJ·mol-1
②3AlCl(g)===2Al(l)+AlCl3(g) ΔH2=b kJ·mol-1
③Al2O3(s)+3C(s)===2Al(l)+3CO(g) ΔH3
下列说法正确的是( )
| A.ΔH3<0 |
| B.Al2O3(s)+3C(s)===2Al(l)+3CO(g) ΔH3=(a-b) kJ·mol-1 |
| C.该电池充电时石墨电极与电源负极相连 |
D.该电池放电时的负极反应方程式为Al-3e-+7AlCl ===4Al2Cl ===4Al2Cl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】锂电池作为最主要的便携式能量电源,影响着我们生活的方方面面。锂空气电池放电的工作原理如图所示。下列叙述不正确的是


| A.电池放电时负极电极方程式为O2+2H2O+4e−=4OH− |
| B.放电时电子由A极向B极移动 |
| C.电解液a,b之间可采用阳离子交换膜 |
| D.电解液b可能为稀LiOH溶液 |
您最近一年使用:0次

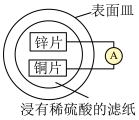
 向锌片移动
向锌片移动



