现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤ 固体;⑥蔗糖;⑦浓盐酸;⑧熔融的
固体;⑥蔗糖;⑦浓盐酸;⑧熔融的 ;⑨酒精溶液;⑩
;⑨酒精溶液;⑩ 溶液
溶液
请回答下列问题(填序号)
(1)以上物质能导电的是___________ 。
(2)以上物质属于电解质的是___________ 。
(3)以上物质属于非电解质的是___________ 。
(4)物质④铜在氧化还原反应中应该只能表现___________ (填“氧化性”和“还原性”)。实验室常用高锰酸钾与⑦反应制备 ,请你配平其化学方程式
,请你配平其化学方程式___________ 。
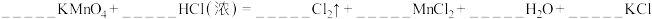
在此反应中,浓盐酸表现的化学性质是___________ 。
(5)向⑩ 溶液中滴加
溶液中滴加 溶液至中性,写出该反应的离子方程式
溶液至中性,写出该反应的离子方程式___________ 。
 固体;⑥蔗糖;⑦浓盐酸;⑧熔融的
固体;⑥蔗糖;⑦浓盐酸;⑧熔融的 ;⑨酒精溶液;⑩
;⑨酒精溶液;⑩ 溶液
溶液请回答下列问题(填序号)
(1)以上物质能导电的是
(2)以上物质属于电解质的是
(3)以上物质属于非电解质的是
(4)物质④铜在氧化还原反应中应该只能表现
 ,请你配平其化学方程式
,请你配平其化学方程式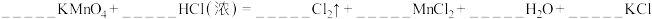
在此反应中,浓盐酸表现的化学性质是
(5)向⑩
 溶液中滴加
溶液中滴加 溶液至中性,写出该反应的离子方程式
溶液至中性,写出该反应的离子方程式
更新时间:2023-11-23 15:04:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】准确掌握化学基本概念和研究方法是学好化学的重要手段。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
每组分类均有错误,其错误的物质分别是___________ 、___________ (填化学式)。
(2)有以下物质:
①熔融氯化钠 ②铝 ③乙醇 ④氨水 ⑤氯化氢气体 ⑥ 固体
固体
i.其中能导电的是___________ (填序号,下同);属于非电解质的是___________ ;属于电解质的是___________ ;属于混合物的是___________ 。
ii.写出物质⑥溶于水时的电离方程式:___________ 。
(3)关于酸、碱、盐的下列各种说法中,正确的是___________(填字母)。
(1)下列是某同学对有关物质进行分类的列表:
| 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 |  |  |  |  |
| 第二组 |  |  |  |  |
(2)有以下物质:
①熔融氯化钠 ②铝 ③乙醇 ④氨水 ⑤氯化氢气体 ⑥
 固体
固体i.其中能导电的是
ii.写出物质⑥溶于水时的电离方程式:
(3)关于酸、碱、盐的下列各种说法中,正确的是___________(填字母)。
| A.化合物电离时,生成的阳离子有氢离子的是酸 |
| B.化合物电离时,生成的阴离子有氢氧根离子的是碱 |
| C.化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐 |
| D.酸溶液一定显酸性,碱溶液一定显碱性,盐溶液一定显中性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列9种物质∶①NaHSO4固体,②CO2气体,③Ba(OH)2固体,④盐酸,⑤蔗糖,⑥Al,⑦食盐水,⑧H2SO4⑨熔融 NaHCO3。请回答下列问题∶
(1)上述物质中属升电解质的是___________ (填序号),属于非电解质的是_____ (填序号),能导电的是___________ (填序号)
(2)①溶液与⑨溶液反应的离子方程式为_____
(3)0.8mol·L-1 NaHSO4溶液与0.1mol·L-1 Ba(OH)2溶液等体积混合。发生反应的离子方程式为___________ 。若在混合溶液中继续滴加Ba(OH)溶液,发生反应的离子方程式为_______
(1)上述物质中属升电解质的是
(2)①溶液与⑨溶液反应的离子方程式为
(3)0.8mol·L-1 NaHSO4溶液与0.1mol·L-1 Ba(OH)2溶液等体积混合。发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩矿泉水
请回答下列问题:
(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于电解质的是___________ (填序号);以上纯净物中能导电的是___________ (填序号)。
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是___________
(3)写出⑧在水溶液中的电离方程式___________ 。
(4)在含40g溶质的①溶液中缓缓通入标准状况下66g CO2,则反应后溶液的溶质有___________ (填化学式)。
请回答下列问题:
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
(3)写出⑧在水溶液中的电离方程式
(4)在含40g溶质的①溶液中缓缓通入标准状况下66g CO2,则反应后溶液的溶质有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)如图所示是在一定温度下向不同电解质溶液中加入新物质时其电流强度(I)随新物质加入量(m)的变化曲线。以下a、b、c三个导电性实验,其中与A图变化趋势一致的是_________________ ,与B图变化趋势一致的是______________ ,与 C图变化趋势一致的是_________________ 。
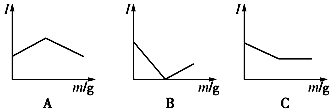
a.向Ba(OH)2溶液中逐滴加入等浓度的H2SO4溶液至过量
b.向醋酸溶液中逐滴加入等浓度的氨水至过量
c.向盐酸中逐滴加入等浓度的NaOH溶液至过量
(2)写出第(1)中,选项b所描述的离子反应方程式____________________ 。
(3)写出制备氢氧化铁胶体的化学反应方程式:_______________________ 。
在氢氧化铁胶体中加入足量的盐酸,能观察到的现象是:____________________ 。

a.向Ba(OH)2溶液中逐滴加入等浓度的H2SO4溶液至过量
b.向醋酸溶液中逐滴加入等浓度的氨水至过量
c.向盐酸中逐滴加入等浓度的NaOH溶液至过量
(2)写出第(1)中,选项b所描述的离子反应方程式
(3)写出制备氢氧化铁胶体的化学反应方程式:
在氢氧化铁胶体中加入足量的盐酸,能观察到的现象是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I:分别用单线桥、双线桥标出:2KClO3 2KCl+3O2↑中电子转移的方向和数目
2KCl+3O2↑中电子转移的方向和数目_______
II:导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是_______ (填序号)。
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
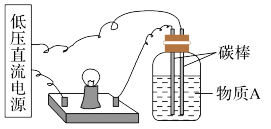
(2)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是_______ (填字母)。
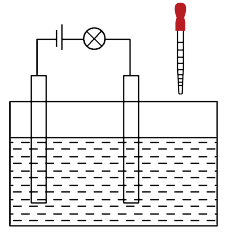
A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
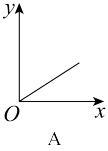
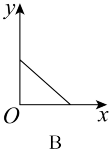
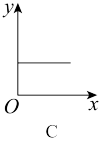
(3)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。若在(2)题图中,电解质溶液为Ca(OH)2溶液,向溶液中逐渐通入CO2.则:下列四个图中,_______ (填字母)能比较准确地反映出溶液的导电能力和通入CO2气体量的关系(x轴表示CO2通入的量,y轴表示导电能力)。
 2KCl+3O2↑中电子转移的方向和数目
2KCl+3O2↑中电子转移的方向和数目II:导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液

(2)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是

A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(3)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。若在(2)题图中,电解质溶液为Ca(OH)2溶液,向溶液中逐渐通入CO2.则:下列四个图中,




您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应、离子反应在生产生活中应用广泛。
(1) 和
和 都是大气污染物。利用氨水可以将
都是大气污染物。利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示:
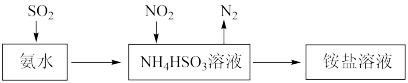
 被吸收的离子方程式是
被吸收的离子方程式是_____ 。
(2)用高能电子束激活烟气(主要成分是 等),会产生
等),会产生 等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是
等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是 、
、_____ (填离子符号)。

(3)SCR(选择性催化还原)工作原理

①尿素 水溶液热解为
水溶液热解为 和
和 ,该反应化学方程式
,该反应化学方程式_____
②反应器中 还原
还原 的化学方程式是
的化学方程式是_____
(4)NSR( 储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(
储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。
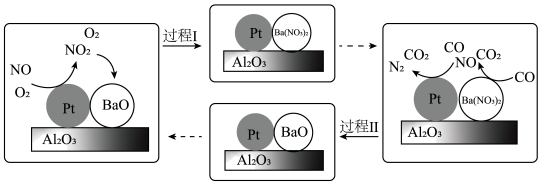
① 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比是
的反应中氧化剂与还原剂的粒子个数之比是_____ 。
②富燃条件下 表面反应的化学方程式是
表面反应的化学方程式是_____ 。
③若柴油中硫含量较高,在稀燃过程中, 吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因
吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因_____ 。
④研究 对
对 吸收氮氧化物的影响,一定温度下,测得气体中
吸收氮氧化物的影响,一定温度下,测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是_____ 。
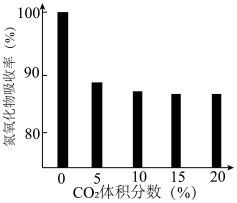
A.一定范围内,氮氧化物吸收率随 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面
B.当 体积分数达到
体积分数达到 时,氮氧化物吸收率依然
时,氮氧化物吸收率依然 体积分数
体积分数 较高,其原因可能是
较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
(1)
 和
和 都是大气污染物。利用氨水可以将
都是大气污染物。利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: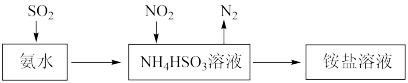
 被吸收的离子方程式是
被吸收的离子方程式是(2)用高能电子束激活烟气(主要成分是
 等),会产生
等),会产生 等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是
等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是 、
、
(3)SCR(选择性催化还原)工作原理

①尿素
 水溶液热解为
水溶液热解为 和
和 ,该反应化学方程式
,该反应化学方程式②反应器中
 还原
还原 的化学方程式是
的化学方程式是(4)NSR(
 储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(
储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。
①
 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比是
的反应中氧化剂与还原剂的粒子个数之比是②富燃条件下
 表面反应的化学方程式是
表面反应的化学方程式是③若柴油中硫含量较高,在稀燃过程中,
 吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因
吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因④研究
 对
对 吸收氮氧化物的影响,一定温度下,测得气体中
吸收氮氧化物的影响,一定温度下,测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随
 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面B.当
 体积分数达到
体积分数达到 时,氮氧化物吸收率依然
时,氮氧化物吸收率依然 体积分数
体积分数 较高,其原因可能是
较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列十种物质:①H2②铝 ③甲烷 ④CO2 ⑤H2SO4⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨盐酸 ⑩Al2(SO4)3
(1)上述物质中属于电解质的有:_____________________ 。(填序号)
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-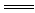 H2O,该反应的化学方程式为
H2O,该反应的化学方程式为_________________ 。
(3)⑩在水中的电离方程式为__________________ ,17.1g该物质溶于水配成250mL溶液,物质的量浓度为_______________ mol·L-1。
(4)⑨的浓溶液与二氧化锰发生反应的化学方程式为:4HCl(浓)+MnO2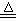 Cl2↑+MnCl2+2H2O,该反应的氧化剂是
Cl2↑+MnCl2+2H2O,该反应的氧化剂是___________ (填化学式),还原剂与氧化剂的物质的量之比是_________ 。写出该反应的离子方程式_____________________________ 。
(1)上述物质中属于电解质的有:
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-
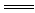 H2O,该反应的化学方程式为
H2O,该反应的化学方程式为(3)⑩在水中的电离方程式为
(4)⑨的浓溶液与二氧化锰发生反应的化学方程式为:4HCl(浓)+MnO2
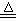 Cl2↑+MnCl2+2H2O,该反应的氧化剂是
Cl2↑+MnCl2+2H2O,该反应的氧化剂是
您最近一年使用:0次
【推荐1】完成下列问题
(1)下列反应中不涉及氧化还原反应的是___________ 。
a.蜡炬成灰 b.水滴石穿 c.食物腐败
(2)KMnO4 和浓盐酸一定条件反应会生成绿黄色的氯气,其变化可表述为___________KMnO4+___________HCl(浓)=___________MnCl2+___________KCl+___________Cl2↑+___________H2O
①请配平上述化学方程式并用单线桥表示出电子转移情况__________ 。
②若该反应有 316gKMnO4参加反应,则被氧化的HCl的质量为___________ g
(3)在反应8NH3+3Cl2=N2+6NH4Cl中,___________ 是还原剂, ___________ 元素被还原;被氧化的元素与被还原的元素的原子个数比为___________ ;
(4)某同学写出以下化学反应方程式(未配平):
①NH3+NO→HNO2+H2O,②NO+HNO3→N2O3+H2O,③N2O4+H2O→HNO3+HNO2,
在3个反应中一定不可能实现的是___________ (填序号)。
(5)亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。 误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列___________(填序号)反应中H2O2表现出的性质相同。
(6)ClO2可用于污水的杀菌和饮用水的净化。KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO ,此反应的离子方程式为
,此反应的离子方程式为___________ 。
(1)下列反应中不涉及氧化还原反应的是
a.蜡炬成灰 b.水滴石穿 c.食物腐败
(2)KMnO4 和浓盐酸一定条件反应会生成绿黄色的氯气,其变化可表述为___________KMnO4+___________HCl(浓)=___________MnCl2+___________KCl+___________Cl2↑+___________H2O
①请配平上述化学方程式并用单线桥表示出电子转移情况
②若该反应有 316gKMnO4参加反应,则被氧化的HCl的质量为
(3)在反应8NH3+3Cl2=N2+6NH4Cl中,
(4)某同学写出以下化学反应方程式(未配平):
①NH3+NO→HNO2+H2O,②NO+HNO3→N2O3+H2O,③N2O4+H2O→HNO3+HNO2,
在3个反应中一定不可能实现的是
(5)亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。 误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列___________(填序号)反应中H2O2表现出的性质相同。
A. |
B.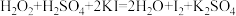 |
C. |
D.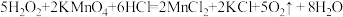 |
 ,此反应的离子方程式为
,此反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在反应5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,氧化剂是__________ ,还原剂是__________ ;氧化剂具有__________ 性;被氧化和被还原的原子数之比是__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
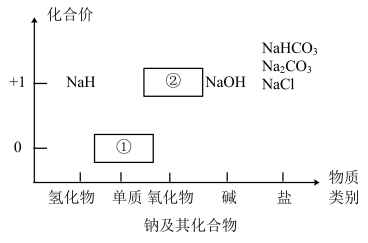
(1)物质①与水反应的离子方程式为_______ ,所以通常将其保存在_______ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目_______ 。
(3)从核心元素价态的视角看,NaH中H元素的化合价为_______ ,从H元素的价态分析,NaH常用作_______ (填“氧化剂”或“还原剂”)。
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
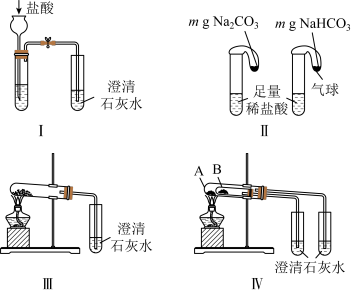
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是_______ (填装置序号)。
②图Ⅲ、Ⅳ中_______ 能更好说明二者的稳定性(填装置序号),写出Ⅳ中固体受热发生分解的化学方程式_______ 。

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目
(3)从核心元素价态的视角看,NaH中H元素的化合价为
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。

①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是
②图Ⅲ、Ⅳ中
您最近一年使用:0次

 晶体;②
晶体;② 固体;③
固体;③ 溶液;④熔融
溶液;④熔融 胶体的化学方程式:
胶体的化学方程式: 是一种酸式盐,试回答下列问题。
是一种酸式盐,试回答下列问题。 溶液反应的离子方程式
溶液反应的离子方程式 溶液混合,发生反应的离子方程式为
溶液混合,发生反应的离子方程式为

