人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
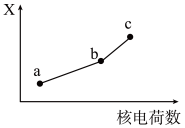
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
更新时间:2023-12-05 20:31:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)②的原子结构示意图是____ 。
(2)化学性质最不活泼的元素是_____ (填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是__________ 。(填离子符号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为_________ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有____ 。
(6)由元素⑧和⑨形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:______ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)②的原子结构示意图是
(2)化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
(6)由元素⑧和⑨形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A_________ ,B__________ ,C____________ ,D___________ ,E_________
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:______________________ 。
(3)写出A、B两元素的最高价氧化物的水化物相互反应的化学方程式:______________________ 。
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)_______________________ 。
(1)写出下列元素符号:A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A、B两元素的最高价氧化物的水化物相互反应的化学方程式:
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】X~R是元素周期表中的短周期元素,其性质或结构信息如下表:
请用化学用语回答下列问题:
(1)X在元素周期表中的位置是_________________________。
(2)元素W的离子结构示意图为_______________________。
(3)元素R的最高价氧化物的电子式为_________________。
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型为① ,② 。
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是 。(用离子方程式表示)
(6)W的氢氧化物是重要的基本化工原料。写出工业上制取该氢氧化物的离子反应方程式 。
| 元素 | X | Y | Z | W | R |
| 性质 信息 | 能形成+7价的化合物 | 日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子 | 焰色反应为黄色 | 位于第IVA,是形成化合物种类最多的元素 |
请用化学用语回答下列问题:
(1)X在元素周期表中的位置是_________________________。
(2)元素W的离子结构示意图为_______________________。
(3)元素R的最高价氧化物的电子式为_________________。
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型为① ,② 。
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是 。(用离子方程式表示)
(6)W的氢氧化物是重要的基本化工原料。写出工业上制取该氢氧化物的离子反应方程式 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】为纪念元素周期表诞生150周年,IUPAC等从世界范围征集优秀青年化学家提名,形成一张“青年化学家元素周期表”,向世界介绍118位优秀青年化学家,有8位中国青年化学家成为“N、Hg、U”等元素的代言人。回答下列问题:
(1)N在周期表中的位置是__ 。
(2)下列有关性质的比较,能用元素周期律解释的是__ 。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(3)非金属性:Cl>Br,用原子结构解释原因__ ,用一个离子方程式证明__ 。
(4)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为__ 。②X的氢化物的电子式__ 。
(1)N在周期表中的位置是
(2)下列有关性质的比较,能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(3)非金属性:Cl>Br,用原子结构解释原因
(4)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
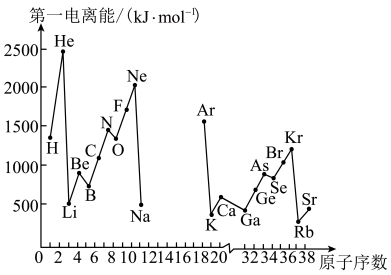
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为____ <Al<__ ;(填元素符号)
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是_____ 。
(3)上图中第一电离能最小的元素在周期表中的位置是第________ 周期________ 族;

(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)上图中第一电离能最小的元素在周期表中的位置是第
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
(1)①的元素符号是__________
(2)②和⑥两种元素的原子半径大小关系:_________ (填“>”或“<”);
(3)③和⑤两种元素的金属性强弱关系:________ (填“>”或“<”);
(4)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:__________ 。
| ⅠA | 0 | ||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | B | ① | ② | Ne | |||||
| 3 | ③ | ④ | ⑤ | Si | ⑥ | ||||
(1)①的元素符号是
(2)②和⑥两种元素的原子半径大小关系:
(3)③和⑤两种元素的金属性强弱关系:
(4)④的单质与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。在光照条件下,氯气和氢气反应过程如下:
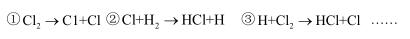
(1)写出氯元素的原子结构示意图________ 反应②中形成的化合物的电子式为_________ ;反应③中被破 坏的化学键属于________ 键。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是________________ 。
(3)与氯元素同周期且金属性最强的元素在周期表中的位置为________________ 。
(4)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是________________ 。
a.卤化银的颜色按 AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按 H—F、H—C1、H—Br、H—I 的顺序依次减小
c.卤化氢的还原性按 HF、HCl、HBr、HI 的顺序依次增强
d.卤素单质与氢气化合按 F2、C12、Br2、I2 的顺序由难变易
(5)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键_____ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:________________ 。
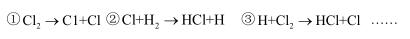
(1)写出氯元素的原子结构示意图
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(3)与氯元素同周期且金属性最强的元素在周期表中的位置为
(4)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a.卤化银的颜色按 AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按 H—F、H—C1、H—Br、H—I 的顺序依次减小
c.卤化氢的还原性按 HF、HCl、HBr、HI 的顺序依次增强
d.卤素单质与氢气化合按 F2、C12、Br2、I2 的顺序由难变易
(5)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键
②卤素单质键能大小与键长的关系为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮、磷、砷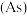 、锑
、锑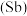 )、铋
)、铋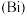 、镆
、镆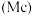 为元素周期表中原子序数依次增大的同族元素,回答下列问题:
为元素周期表中原子序数依次增大的同族元素,回答下列问题:
(1)砷在元素周期表中的位置_______ ,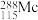 的中子数为
的中子数为_______ 。
(2)氨气和磷化物的热稳定性:
_______  (填“>”或“<”)。
(填“>”或“<”)。
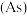 、锑
、锑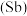 )、铋
)、铋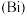 、镆
、镆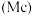 为元素周期表中原子序数依次增大的同族元素,回答下列问题:
为元素周期表中原子序数依次增大的同族元素,回答下列问题:(1)砷在元素周期表中的位置
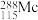 的中子数为
的中子数为(2)氨气和磷化物的热稳定性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】为纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。下图是扇形元素周期表的一部分,针对元素①~⑩按要求作答。
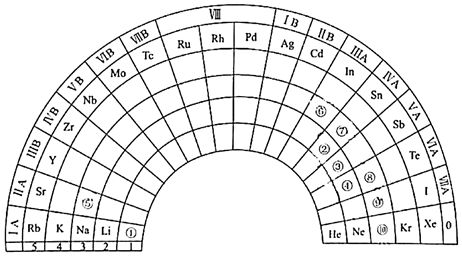
(1)⑩的原子结构示意图为___________________ 。
(2)①和②组成的最简单化合物的电子式为_______________ 。
(3)④和⑤的简单离子半径较大的是________ (填序号)。
(4)③的简单氢化物与其最高价氧化物对应水化物反应得到的盐的化学式为________________ 。
(5)某元素原子的M层电子数为K层电子数的两倍,则该元素是_________ (填序号)。
(6)把⑥投入烧碱溶液中发生反应的化学方程式为__________________ 。
(7)写出一个能证明⑧的非金属性小于⑨的离子方程式____________________ 。

(1)⑩的原子结构示意图为
(2)①和②组成的最简单化合物的电子式为
(3)④和⑤的简单离子半径较大的是
(4)③的简单氢化物与其最高价氧化物对应水化物反应得到的盐的化学式为
(5)某元素原子的M层电子数为K层电子数的两倍,则该元素是
(6)把⑥投入烧碱溶液中发生反应的化学方程式为
(7)写出一个能证明⑧的非金属性小于⑨的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)汞的原子结构示意图 ,汞在周期表中位于第
,汞在周期表中位于第__________ 周期。
(2) 、
、 、
、 分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是
分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是___________ 。
(3)下列有关性质的比较能用元素周期律解释的是_______ 。
a.酸性: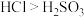
b.非金属性:
c.碱性: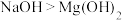
d.热稳定性:
(4)硒( )与硫位于同一主族,均是生命必需元素。下列推断正确的是
)与硫位于同一主族,均是生命必需元素。下列推断正确的是___________ 。
a.硒元素的最低负化合价为 价
价
b.二氧化硒( )具有还原性
)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为___________ 。
②X的氢化物的电子式___________ 。
 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)汞的原子结构示意图
 ,汞在周期表中位于第
,汞在周期表中位于第(2)
 、
、 、
、 分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是
分别为氮、氧、硫3种元素对应的氢化物,其中最稳定的是(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:
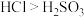
b.非金属性:

c.碱性:
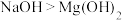
d.热稳定性:

(4)硒(
 )与硫位于同一主族,均是生命必需元素。下列推断正确的是
)与硫位于同一主族,均是生命必需元素。下列推断正确的是a.硒元素的最低负化合价为
 价
价b.二氧化硒(
 )具有还原性
)具有还原性c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①Y的元素符号为
②X的氢化物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。下表是元素周期表的一部分:
注意:用元素符号或化学式填空。
(1)①到⑩号元素中,所形成的氢化物最稳定的是___________ ,最高价氧化物对应的水化物酸性最强的是___________ 。③号元素在元素周期表中的位置是___________ 。
(2)实验室制备②的气态氢化物的化学方程式为___________ 。
(3)元素⑤的最高价氧化物对应水化物含有的化学键类型为:___________ (选填“离子键”“极性键”“非极性键”),其与⑦的最高价氧化物所对应的水化物能相互反应,反应的离子方程式是:___________ 。
(4)下列说法正确的是___________
A.碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
B.一定条件下,随着核电荷数的增加,卤素单质与H2化合越来越难
C.随着核电荷数的增加,卤族单质的氧化性逐渐增强
D.周期表七行七个周期,18列16族
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||||
| 过渡元素 | ⑩ |
注意:用元素符号或化学式填空。
(1)①到⑩号元素中,所形成的氢化物最稳定的是
(2)实验室制备②的气态氢化物的化学方程式为
(3)元素⑤的最高价氧化物对应水化物含有的化学键类型为:
(4)下列说法正确的是
A.碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
B.一定条件下,随着核电荷数的增加,卤素单质与H2化合越来越难
C.随着核电荷数的增加,卤族单质的氧化性逐渐增强
D.周期表七行七个周期,18列16族
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E五种元素的原子序数依次增大,其中A、B、C、D为短周期元素,且只有A、D为非金属元素。A的氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族,且原子序数相差8。
(1)E在元素周期表中的位置:____________ ,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________________________________ 。
(2)A的氢化物溶于水后的电离方程式为_________________________________ ;实验室制备A的氢化物的化学方程式为___________________________________ 。
(3)B单质在空气中燃烧后的产物为____________ ,产物中存在的化学键类型有_____ ,写出该产物和水反应的离子方程式:____________________________ 。
(1)E在元素周期表中的位置:
(2)A的氢化物溶于水后的电离方程式为
(3)B单质在空气中燃烧后的产物为
您最近一年使用:0次



