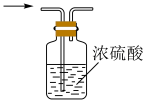
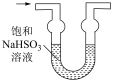
有一瓶无色澄清溶液,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 离子。现进行以下实验:
离子。现进行以下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入 溶液,使溶液由酸性变成碱性,无沉淀产生;
溶液,使溶液由酸性变成碱性,无沉淀产生;
③取少量②中的碱性溶液,滴加 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
(1)根据上述事实确定:该溶液中肯定存在的离子有______ ;肯定不存在的离子有______ ;可能存在的离子有______ 。
(2)写出②中发生反应的离子方程式______ 。
现有下列几种物质:① ;②
;② ;③
;③ ;④稀
;④稀 ;⑤
;⑤ ;⑥熔融
;⑥熔融 ;⑦汞;③
;⑦汞;③ ;⑨液氯;⑩氨水。请回答下列问题:
;⑨液氯;⑩氨水。请回答下列问题:
(3)以上物质属于电解质的是______ ,能导电的是______ 。(填序号)
(4)写出①与⑥的水溶液反应的离子反应方程式:______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 离子。现进行以下实验:
离子。现进行以下实验:①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入
 溶液,使溶液由酸性变成碱性,无沉淀产生;
溶液,使溶液由酸性变成碱性,无沉淀产生;③取少量②中的碱性溶液,滴加
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。(1)根据上述事实确定:该溶液中肯定存在的离子有
(2)写出②中发生反应的离子方程式
现有下列几种物质:①
 ;②
;② ;③
;③ ;④稀
;④稀 ;⑤
;⑤ ;⑥熔融
;⑥熔融 ;⑦汞;③
;⑦汞;③ ;⑨液氯;⑩氨水。请回答下列问题:
;⑨液氯;⑩氨水。请回答下列问题:(3)以上物质属于电解质的是
(4)写出①与⑥的水溶液反应的离子反应方程式:
更新时间:2023-11-13 14:42:56
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】请回答下列问题:
(1)现有下列物质,请用序号填空:
①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳
上述状态下可导电的是___________ 。属于强电解质的是___________ 。属于非电解质的是___________ 。
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体。
(3)NaHSO4 固体溶于水的电离方程式为___________ ;
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为___________ 。
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C___________ ,D ___________ ;
A与C反应的离子方程式___________ ;
A溶液中阴离子的检验方法___________ 。
(1)现有下列物质,请用序号填空:
①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳
上述状态下可导电的是
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用
(3)NaHSO4 固体溶于水的电离方程式为
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO
 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C
A与C反应的离子方程式
A溶液中阴离子的检验方法
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】图中A~K均为中学化学中常见的物质。A是金属单质、C为黄绿色气体单质。常温常压下C、D、F、G、K是气体,A、B、E的焰色试验同为黄色:J具有漂白作用。它们之间有如图转化关系。(反应中生成的部分产物已经略去)请回答下列问题:
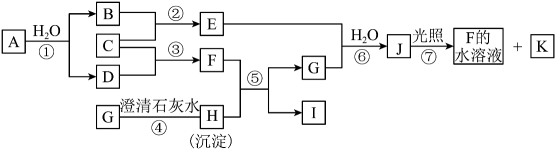
(1)E的电离方程式:
(2)气体C有毒性,不能直接排放到空气中,请写出实验室常用处理尾气C时发生的离子反应方程式
(3)图示物质A~K中,属于非电解质的为
(4)写出反应⑦的化学方程式
 气体K,转移的电子的物质的量为
气体K,转移的电子的物质的量为(5)写出反应⑤的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】Ⅰ.分类是研究物质组成及其变化的一种常用的科学方法。
现有以下物质:①液氯;②氢氧化铁胶体;③ 粉末;④熔融NaOH;⑤饱和食盐水。
粉末;④熔融NaOH;⑤饱和食盐水。
(1)在上述物质中,属于化合物的是______ (填标号,下同),属于电解质的是______ ,能导电的是______ 。
(2)写出①在水中发生反应的离子方程式____________ 。
Ⅱ.某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作步骤如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①配制0.10 mol⋅L稀盐酸和0.10 mol⋅LNaOH溶液;
②向一粒研碎后的药片(0.1 g)中加入20.00 mL蒸馏水;
③加入25.00 mL 0.10 mol/L稀盐酸;
④用0.10 mol/LNaOH溶液中和过量稀盐酸,记录所消耗NaOH溶液的体积。
请回答下列问题:
(3)若配制480 mL 0.10 mol⋅L NaOH溶液,则需用托盘天平称NaOH固体
NaOH溶液,则需用托盘天平称NaOH固体______ g。
(4)下列实验操作使所配制的稀盐酸物质的量浓度偏小的是______(填字母)。
(5)某同学4次测定所消耗NaOH溶液的体积如表。
根据这个同学的实验数据,计算这种药片中碳酸钙的质量分数______ (保留两位有效数字)。
现有以下物质:①液氯;②氢氧化铁胶体;③
 粉末;④熔融NaOH;⑤饱和食盐水。
粉末;④熔融NaOH;⑤饱和食盐水。(1)在上述物质中,属于化合物的是
(2)写出①在水中发生反应的离子方程式
Ⅱ.某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作步骤如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①配制0.10 mol⋅L稀盐酸和0.10 mol⋅LNaOH溶液;
②向一粒研碎后的药片(0.1 g)中加入20.00 mL蒸馏水;
③加入25.00 mL 0.10 mol/L稀盐酸;
④用0.10 mol/LNaOH溶液中和过量稀盐酸,记录所消耗NaOH溶液的体积。
请回答下列问题:
(3)若配制480 mL 0.10 mol⋅L
 NaOH溶液,则需用托盘天平称NaOH固体
NaOH溶液,则需用托盘天平称NaOH固体(4)下列实验操作使所配制的稀盐酸物质的量浓度偏小的是______(填字母)。
| A.用量筒量取浓盐酸时俯视刻度线 |
| B.容量瓶用蒸馏水洗涤后未干燥 |
| C.定容后摇匀、静置,发现液面下降,再加蒸馏水至刻度线 |
| D.定容时,俯视容量瓶刻度线 |
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V[NaOH(aq)]/mL | 13.0 | 12.9 | 13.1 | 13.8 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计实验和过程如下:如图所示连接好装置,向烧杯中加入25mLBa(OH)2溶液和2滴酚酞溶液,再匀速逐滴向烧杯中滴加H2SO4溶液,并轻轻振荡。

实验现象及分析:
(1)溶液颜色变化及原因:___ 。
(2)灯泡亮度变化及原因:___ 。
(3)溶液变浑浊的原因是:__ 。
(4)烧杯中溶液的酸碱度变化是:__ 。
实验结论:
(5)稀H2SO4与Ba(OH)2溶液反应的实质是:___ (用离子方程式表示)。

实验现象及分析:
(1)溶液颜色变化及原因:
(2)灯泡亮度变化及原因:
(3)溶液变浑浊的原因是:
(4)烧杯中溶液的酸碱度变化是:
实验结论:
(5)稀H2SO4与Ba(OH)2溶液反应的实质是:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某学习小组以Ba(OH)2、水、H2SO4为实验对象探究离子反应发生的条件。
(1)
Ba(OH)2与H2SO4在溶液中能发生___ 反应。
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加H2O后,灯泡变亮的原因是Ba(OH)2发生了___ 。
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因___ 。
(4)查阅有关物质溶解度数据如表:
比较溶液2、溶液3中c(SO )的大小:
)的大小:___ >___ 。
(5)下列图示能正确表示实验过程的是___ (填序号)。
a.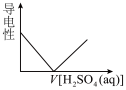 b.
b. c.
c.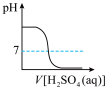 d.
d.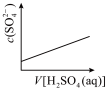
(6)实验2:用Na2SO4溶液替代稀H2SO4,重复实验进行对照。
①Na2SO4溶液的浓度是___ 。
②加入Na2SO4溶液过程中灯泡不熄灭,原因是___ 。
通过实验可知:离子反应发生的条件之一是生成沉淀。
(1)
| 实验1:向烧杯中依次加入下列试剂,记录灯泡变化 | |
 | ①Ba(OH)2粉末:灯泡不亮 ②加入蒸馏水:灯泡变亮 ③逐滴滴加0.1mol/LH2SO4,灯泡变化如下: 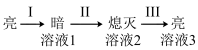 |
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加H2O后,灯泡变亮的原因是Ba(OH)2发生了
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因
(4)查阅有关物质溶解度数据如表:
| 物质 | Ba(OH)2 | BaSO4 |
| 溶解度/g | 5.6 | 0.00025 |
 )的大小:
)的大小:(5)下列图示能正确表示实验过程的是
a.
 b.
b. c.
c. d.
d.
(6)实验2:用Na2SO4溶液替代稀H2SO4,重复实验进行对照。
①Na2SO4溶液的浓度是
②加入Na2SO4溶液过程中灯泡不熄灭,原因是
通过实验可知:离子反应发生的条件之一是生成沉淀。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.现有中学化学中常见的八种物质:
①固体氢氧化钡 ②石墨碳棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥熔融氯化钠 ⑦蔗糖 ⑧碳酸钠粉末
请用序号填空:
(1)上述状态下可导电的是________ ,属于电解质的是_____________ 。
Ⅱ.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
①甲同学向1 mol·L−1氯化铁溶液中加入少量的NaOH溶液;
②乙同学直接加热饱和FeCl3溶液;
③丙同学向25 ml沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
(1)其中操作正确的同学是______ ;他的操作中涉及到的化学反应方程式为_______________________________________________________ 。
(2)证明有Fe(OH)3胶体生成的现象是________________________ 。
(3)丁同学将所制得的Fe(OH)3胶体进行下列实验:将Fe(OH)3胶体装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明________________________________ 。
①固体氢氧化钡 ②石墨碳棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥熔融氯化钠 ⑦蔗糖 ⑧碳酸钠粉末
请用序号填空:
(1)上述状态下可导电的是
Ⅱ.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
①甲同学向1 mol·L−1氯化铁溶液中加入少量的NaOH溶液;
②乙同学直接加热饱和FeCl3溶液;
③丙同学向25 ml沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的现象是
(3)丁同学将所制得的Fe(OH)3胶体进行下列实验:将Fe(OH)3胶体装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】用废铁屑制备磁性胶体粒子的工艺如下。

(1)废铁屑表面有油脂存在,其作用是:___________ 。
使用Na2CO3溶液(显碱性)浸泡废铁屑的目的:____________ 。
(2)Fe与稀硫酸反应的离子方程式:___________ 。
(3)加适量的H2O2是为了将部分Fe2+氧化为Fe3+,离子反应:___________ 。
(4)加入NaOH溶液后与溶液中的Fe2+、Fe3+反应,生成相应碱的离子方程式:___________ 、___________ 。
(5)通入N2是防止空气中的___________ 氧化___________ 。
(6)检验溶液A中含有的Fe3+,方法为:_________________ 。

(1)废铁屑表面有油脂存在,其作用是:
使用Na2CO3溶液(显碱性)浸泡废铁屑的目的:
(2)Fe与稀硫酸反应的离子方程式:
(3)加适量的H2O2是为了将部分Fe2+氧化为Fe3+,离子反应:
(4)加入NaOH溶液后与溶液中的Fe2+、Fe3+反应,生成相应碱的离子方程式:
(5)通入N2是防止空气中的
(6)检验溶液A中含有的Fe3+,方法为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】材料一:现有一包白色固体粉末,由Na2SO4、CaCO3、NaCl、BaCl2、CuSO4中的几种物质组成,为确定其成分,进行如下实验:
Ⅰ.取少量白色粉末,加入足量水,充分搅拌后过滤,得到白色沉淀和无色滤液;
Ⅱ.向Ⅰ滤出的沉淀中加入足量稀盐酸,沉淀部分溶解,并产生无色气体。
据此回答下列问题:
(1)原白色固体粉末中一定含有_______ ,可能含有_______ ,一定不含有_______ (填化学式)。
(2)实验Ⅰ中发生反应的离子方程式为_______ ,实验Ⅱ中发生反应的离子方程式为_______ 。
材料二:无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(3)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ 。
Ⅰ.取少量白色粉末,加入足量水,充分搅拌后过滤,得到白色沉淀和无色滤液;
Ⅱ.向Ⅰ滤出的沉淀中加入足量稀盐酸,沉淀部分溶解,并产生无色气体。
据此回答下列问题:
(1)原白色固体粉末中一定含有
(2)实验Ⅰ中发生反应的离子方程式为
材料二:无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(3)不做任何实验就可以肯定原溶液中不存在的离子是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学兴趣小组对 与
与 的产物进行了探究.
的产物进行了探究.
同学们经过讨论,提出了如下猜想:
猜想1:产物为 和
和
猜想2:产物为
甲同学设计如图所示实验装置(夹持装置已省略)制备 并进行实验探究,请回答下列问题:
并进行实验探究,请回答下列问题:__________ ;打开分液漏斗活塞,装置甲中发生反应的离子方程式为__________ ;使用70%的硫酸而不用98%的硫酸的原因是__________ .
(2)①甲同学用带火星的木条检验出丁中收集的气体为氧气,该同学认为猜想1正确,乙同学分析装置后推翻了甲同学的结论,乙同学的理由可能是__________ ,乙同学对实验装置进行了改进,在装置甲和装置乙之间添加了装置戊,装置戊可能是__________ (填标号).
②改进实验装置后,丙同学在乙处硬质玻璃管内淡黄色固体全部变成白色后,取适量反应后的白色固体a于试管i中,加入适量的稀硫酸,有气泡产生,将产生的气体通入适量酸性高锰酸钾溶液b中,溶液b褪色,说明固体a中含有__________ (填化学式),溶液b褪色的离子方程式为__________ ;另取适量固体a于试管ii中,加入足量的稀盐酸酸化,充分反应后,加入适量的 溶液,观察到有白色沉淀产生,该白色沉淀为
溶液,观察到有白色沉淀产生,该白色沉淀为__________ (填化学式)。
实验结论: 与
与 在常温时就能发生化学反应,生成
在常温时就能发生化学反应,生成__________ (填化学式)和 .
.
 与
与 的产物进行了探究.
的产物进行了探究.同学们经过讨论,提出了如下猜想:
猜想1:产物为
 和
和
猜想2:产物为

甲同学设计如图所示实验装置(夹持装置已省略)制备
 并进行实验探究,请回答下列问题:
并进行实验探究,请回答下列问题: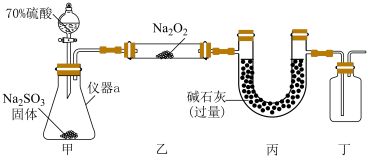
(2)①甲同学用带火星的木条检验出丁中收集的气体为氧气,该同学认为猜想1正确,乙同学分析装置后推翻了甲同学的结论,乙同学的理由可能是
|
|
|
|
A | B | C | D |
 溶液,观察到有白色沉淀产生,该白色沉淀为
溶液,观察到有白色沉淀产生,该白色沉淀为实验结论:
 与
与 在常温时就能发生化学反应,生成
在常温时就能发生化学反应,生成 .
.
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、 、
、 、I-、
、I-、 ,实验如下:
,实验如下:
由此判断:
(1)溶液中一定存在的离子是____________________________________________ ;溶液中肯定不存在的离子是______________________________________________ 。
(2)写出实验步骤(2)中所发生反应的离子方程式____________________________ 。
(3)写出实验步骤(5)中沉淀部分溶解的离子方程式____________________________ 。
(4)不能确定的离子是__________________________ ,为了进一步确定其是否存在,应该补充的实验是_____________________________________________________________ 。
 、
、 、I-、
、I-、 ,实验如下:
,实验如下:| 实验步骤 | 实验现象 |
| (1)用玻璃棒蘸取少量该溶液,点在pH试纸中部 | 试纸变为红色 |
| (2)取少量该溶液,加入Cu片和浓硫酸,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| (4)取(3)中反应后的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| (5)取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
(1)溶液中一定存在的离子是
(2)写出实验步骤(2)中所发生反应的离子方程式
(3)写出实验步骤(5)中沉淀部分溶解的离子方程式
(4)不能确定的离子是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象。
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、C的化学式:B_______ ;C _______ 。
(2)写出过量E滴入到C溶液中的离子反应方程式_______ 。
(3)在A溶液中加澄清石灰水,其离子方程式为_______ 。
(4)写出检验D中阴离子的方法_______ 。
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、 、 、 、 、 |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象。
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、C的化学式:B
(2)写出过量E滴入到C溶液中的离子反应方程式
(3)在A溶液中加澄清石灰水,其离子方程式为
(4)写出检验D中阴离子的方法
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某无色溶液中可能含有K+、Na+、 、Cl-、Cu2+中的一种或几种,为鉴别其中所含离子,现进行如下实验:
、Cl-、Cu2+中的一种或几种,为鉴别其中所含离子,现进行如下实验:
(1)原溶液中一定存在的离子是_____ (填离子符号,下同),一定不存在的离子是______ ,可能存在的离子是_________ 。
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是:__________________ 。
 、Cl-、Cu2+中的一种或几种,为鉴别其中所含离子,现进行如下实验:
、Cl-、Cu2+中的一种或几种,为鉴别其中所含离子,现进行如下实验:| 序号 | 实验操作及现象 |
| 步骤① | 取原溶液,进行焰色试验,显黄色,透过蓝色钴玻璃观察无紫色 |
| 步骤② | 取原溶液,向溶液中加入盐酸,有气体产生 |
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是:
您最近一年使用:0次