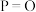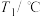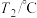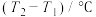Ⅰ.在载人航天器中,可以利用 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:
①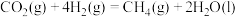

②
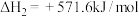
(1)请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式___________ 。
Ⅱ.将 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持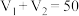 。
。
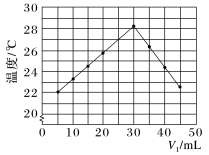
(2)下列叙述正确的是___________。
(3)中和反应的反应热的理论值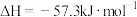 ,写出表示稀盐酸和
,写出表示稀盐酸和 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式___________ 。下列操作可能使测得的 偏大的是
偏大的是___________ (填序号)。
①室温低于 时进行实验
时进行实验
②分多次把 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
③实验时用环形铜丝搅拌棒代替搅拌器
(4)在做测定中和反应的反应热实验时,应使用仪器的正确组合是___________。
①天平 ②量筒 ③烧杯 ④滴定管 ⑤温度计 ⑥试管 ⑦酒精灯
 与
与 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,然后通过电解
等,然后通过电解 得到
得到 ,从而实现
,从而实现 的再生。已知:
的再生。已知:①
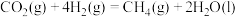

②

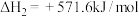
(1)请写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
Ⅱ.将
 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持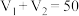 。
。
(2)下列叙述正确的是___________。
| A.该实验表明化学能可转化为热能 | B.做该实验时环境温度为 |
C. 溶液的浓度约为 溶液的浓度约为 | D.该实验表明有水生成的反应都是放热反应 |
(3)中和反应的反应热的理论值
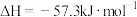 ,写出表示稀盐酸和
,写出表示稀盐酸和 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式 偏大的是
偏大的是①室温低于
 时进行实验
时进行实验②分多次把
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中③实验时用环形铜丝搅拌棒代替搅拌器
(4)在做测定中和反应的反应热实验时,应使用仪器的正确组合是___________。
①天平 ②量筒 ③烧杯 ④滴定管 ⑤温度计 ⑥试管 ⑦酒精灯
| A.①②④ | B.②③⑤ | C.②③④⑦ | D.全部 |
更新时间:2023-11-11 15:30:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.回答下列问题:
(1)“84”消毒液是一种以 为主要成分的高效消毒剂,
为主要成分的高效消毒剂, 溶液
溶液__________ 性(填“酸”“碱”或“中”),用离子方程式表示其原因__________ 。
(2)25℃时,pH均为3的醋酸和硫酸铝两种溶液中,由水电离出的 之比为
之比为__________ 。该温度下,若 的100体积某强酸溶液与
的100体积某强酸溶液与 的1体积某强碱溶液混合后溶液呈中性,则
的1体积某强碱溶液混合后溶液呈中性,则
__________ 。
Ⅱ.某实验小组用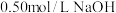 溶液和
溶液和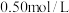 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。
配制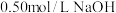 溶液
溶液
(3)若实验中大约要使用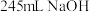 溶液,则至少需要称量
溶液,则至少需要称量 固体
固体__________ g。取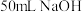 溶液和
溶液和 硫酸溶液进行实验,实验数据如下表。
硫酸溶液进行实验,实验数据如下表。
(4)请填写下表中的空白:
(5)近似认为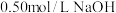 溶液和
溶液和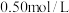 硫酸溶液的密度都是
硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 J/(g·℃)。则中和热
J/(g·℃)。则中和热
__________ (取小数点后一位)。
(6)上述实验结果的数值与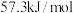 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是__________ (填字母)。
a.实验装置保温、隔热效果差
b.在量取 溶液的体积时仰视读数
溶液的体积时仰视读数
c.分多次把 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中
d.用铜棒代替玻璃搅拌棒
(1)“84”消毒液是一种以
 为主要成分的高效消毒剂,
为主要成分的高效消毒剂, 溶液
溶液(2)25℃时,pH均为3的醋酸和硫酸铝两种溶液中,由水电离出的
 之比为
之比为 的100体积某强酸溶液与
的100体积某强酸溶液与 的1体积某强碱溶液混合后溶液呈中性,则
的1体积某强碱溶液混合后溶液呈中性,则
Ⅱ.某实验小组用
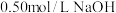 溶液和
溶液和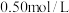 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。配制
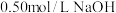 溶液
溶液(3)若实验中大约要使用
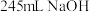 溶液,则至少需要称量
溶液,则至少需要称量 固体
固体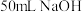 溶液和
溶液和 硫酸溶液进行实验,实验数据如下表。
硫酸溶液进行实验,实验数据如下表。(4)请填写下表中的空白:
温度实验次数 | 起始温度 | 终止温度 | 温度差平均值 | ||
|
| 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
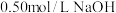 溶液和
溶液和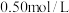 硫酸溶液的密度都是
硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 J/(g·℃)。则中和热
J/(g·℃)。则中和热
(6)上述实验结果的数值与
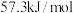 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是a.实验装置保温、隔热效果差
b.在量取
 溶液的体积时仰视读数
溶液的体积时仰视读数c.分多次把
 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中d.用铜棒代替玻璃搅拌棒
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,回答下列有关问题:
(1)用0.1mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出__________ kJ的能量。
(2)如图所示装置中,仪器A的名称是_______________ ,作用是___________________________ ;碎泡沫塑料的作用是__________________________________ 。
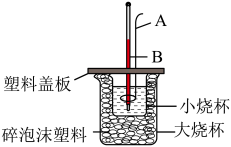
(3)通过实验测定的中和热的ΔH常常大于-57.3kJ/mol,其原因可能是______________ 。
(1)用0.1mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出
(2)如图所示装置中,仪器A的名称是

(3)通过实验测定的中和热的ΔH常常大于-57.3kJ/mol,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题:
(1)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。
①该反应的生成物能量总和__ (填“大于”、“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量___ (填“大于”、“小于”或“等于”)572 kJ。
(2)2.3g有机物C2H6O和一定量的氧气混合点燃,恰好完全燃烧,生成CO2和液态水,并放出68.35kJ热量,则该反应的热化学方程式是___ 。
(3)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1
H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是___ 。
(4)2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点
2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点___ (填“升高”还是“降低”),△H___ (填“变大”、“变小”或“不变”)。
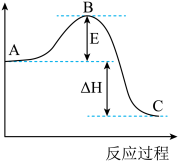
(5)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、___ 、量筒。量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是___ (填序号)。
A.50 mL0.50mol·L-1NaOH溶液
B.50 mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(1)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。
①该反应的生成物能量总和
②若2mol氢气完全燃烧生成水蒸气,则放出的热量
(2)2.3g有机物C2H6O和一定量的氧气混合点燃,恰好完全燃烧,生成CO2和液态水,并放出68.35kJ热量,则该反应的热化学方程式是
(3)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是
(4)2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点
2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点
(5)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
A.50 mL0.50mol·L-1NaOH溶液
B.50 mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】完成下列问题
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液测定计算中和反应的反应热。
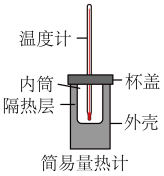
回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是_______ 。
②如改用0.0275molNaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将_______ (填“偏大”、“偏小”或“无影响”)。
(2)反应mA(g)+nB(g) pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
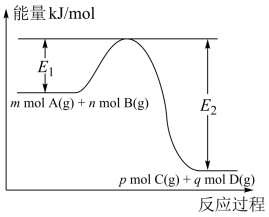
①该反应ΔH=_______ (用含E1、E2式子表示);
②在反应体系中加入催化剂,E1_______ (填“增大”、“减小”、“不变”),ΔH_______ (填“增大”、“减小”、“不变”)。
(3)依据事实,写出下列反应的热化学方程式:
①4g硫粉在O2中完全燃烧生成SO2气体,放出37kJ热量,写出表示硫燃烧热的热化学方程式为:_______ 。
②25℃101kPa时,氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水,放出2.444kJ的热量。请写出氢气和氧气反应生成1mol液态水时的热化方程式为:_______ 。
(4)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①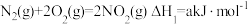
②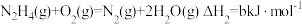
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:_______ 。
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液测定计算中和反应的反应热。

回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是
②如改用0.0275molNaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将
(2)反应mA(g)+nB(g)
 pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
①该反应ΔH=
②在反应体系中加入催化剂,E1
(3)依据事实,写出下列反应的热化学方程式:
①4g硫粉在O2中完全燃烧生成SO2气体,放出37kJ热量,写出表示硫燃烧热的热化学方程式为:
②25℃101kPa时,氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水,放出2.444kJ的热量。请写出氢气和氧气反应生成1mol液态水时的热化方程式为:
(4)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①
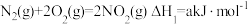
②
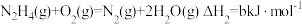
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是_______ (填写序号)。
(2)燃烧10gH2生成液态水,放出的热量为_______ 。
(3)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为_______ 。
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(4)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=_______ 。
①2H2(g)+O2(g)=2H2O(l) △H=-570kJ/mol
②2H2O(g)=2H2(g)+O2(g) △H=+483.6kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是
(2)燃烧10gH2生成液态水,放出的热量为
(3)已知:1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应,写出该中和热的热化学方程式为
Ⅱ.已知:工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)=CH3OH(g) ΔH1=-90.7kJ·mol-1 ①
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1 ②
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1 ③
(4)反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】中国长征系列火箭常用偏二甲肼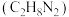 、液态氢等作为燃料,液态氧、四氧化二氮
、液态氢等作为燃料,液态氧、四氧化二氮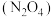 等作为助燃剂。火箭某一级发射使用的燃料是偏二甲肼
等作为助燃剂。火箭某一级发射使用的燃料是偏二甲肼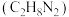 和四氧化二氮组合。
和四氧化二氮组合。
(1)已知:1.5g偏二甲肼(液态)完全燃烧生成液态水放出50kJ热量。则偏二甲肼的摩尔燃烧焓为______ ,请写出其中表示偏二甲肼燃烧摩尔焓的热化学方程式:__________________ 。
(2)运载火箭的第三级使用的推进剂是液氢和液氧。
已知下列在298K时的热化学方程式:
I.
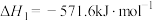
Ⅱ
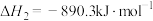
Ⅲ.
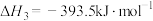
①已知
 ,试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:
,试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:__________________ 。
②如表所示是部分化学键的键能参数:
已知白磷的摩尔燃烧焓为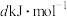 ,白磷及其完全燃烧的产物的结构如图所示,则表中x=
,白磷及其完全燃烧的产物的结构如图所示,则表中x=______ (用含a、b、c、d的代数式表示)。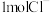 、
、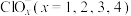 的能量(单位:kJ)相对大小如图所示。
的能量(单位:kJ)相对大小如图所示。______ (用离子符号表示)。
(4)取50mLNaOH溶液和30mL硫酸进行实验,实验数据如下表:
①温度差的平均值为______ ℃。
②近似认为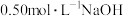 溶液和
溶液和 硫酸的密度都是
硫酸的密度都是 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容 。则测得的中和热
。则测得的中和热
______ (结果保留1位小数)。
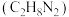 、液态氢等作为燃料,液态氧、四氧化二氮
、液态氢等作为燃料,液态氧、四氧化二氮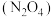 等作为助燃剂。火箭某一级发射使用的燃料是偏二甲肼
等作为助燃剂。火箭某一级发射使用的燃料是偏二甲肼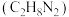 和四氧化二氮组合。
和四氧化二氮组合。(1)已知:1.5g偏二甲肼(液态)完全燃烧生成液态水放出50kJ热量。则偏二甲肼的摩尔燃烧焓为
(2)运载火箭的第三级使用的推进剂是液氢和液氧。
已知下列在298K时的热化学方程式:
I.

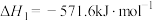
Ⅱ

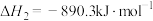
Ⅲ.

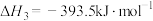
①已知

 ,试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:
,试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:②如表所示是部分化学键的键能参数:
化学键 | 键能 |
|
|
|
|
|
|
|
|
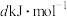 ,白磷及其完全燃烧的产物的结构如图所示,则表中x=
,白磷及其完全燃烧的产物的结构如图所示,则表中x=
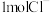 、
、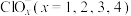 的能量(单位:kJ)相对大小如图所示。
的能量(单位:kJ)相对大小如图所示。
(4)取50mLNaOH溶液和30mL硫酸进行实验,实验数据如下表:
实验次数 | 起始温度 | 终止温度 | 温度差 | ||
|
| 平均值 | |||
1 | 26.6 | 26.6 | 26.6 | 29.1 | |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
②近似认为
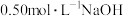 溶液和
溶液和 硫酸的密度都是
硫酸的密度都是 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容 。则测得的中和热
。则测得的中和热
您最近一年使用:0次

 /℃
/℃ /℃
/℃ /℃
/℃