某无色透明溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的几种。兴趣小组同学为确定其成分,进行如下实验:
中的几种。兴趣小组同学为确定其成分,进行如下实验:
①用pH试纸对溶液进行测试,结果表明溶液显酸性;
②取少量溶液于试管中,加入过量 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;
③取少量实验②中的滤液于试管中,加入 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
(1)测定溶液pH的操作是__________ 。
(2)该溶液中肯定含有的离子是__________ (填离子符号,下同),肯定不含有的离子是__________ ,可能含有的离子是__________ 。
(3)步骤②中发生反应的离子方程式为__________ 。
(4)若要进一步检验可能含有的离子是否存在,可采取的方法是__________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 中的几种。兴趣小组同学为确定其成分,进行如下实验:
中的几种。兴趣小组同学为确定其成分,进行如下实验:①用pH试纸对溶液进行测试,结果表明溶液显酸性;
②取少量溶液于试管中,加入过量
 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;③取少量实验②中的滤液于试管中,加入
 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。(1)测定溶液pH的操作是
(2)该溶液中肯定含有的离子是
(3)步骤②中发生反应的离子方程式为
(4)若要进一步检验可能含有的离子是否存在,可采取的方法是
更新时间:2023-12-22 09:37:11
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl-、OH-、NO3-六种离子,向试管A的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管A的溶液中所含的上述离子有________ 。
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为______ (填“A”或“B”)。
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是__________ (填化学式)。
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为____________ 、_______________ 。(不考虑氢氧化银的存在)
(5)若向由试管A溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量Ba(OH)2溶液,则发生反应的离子方程式为________________ 。
(1)试管A的溶液中所含的上述离子有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
(5)若向由试管A溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量Ba(OH)2溶液,则发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D四种可溶性盐,其阳离子分别是Na+、Ba2+、Fe3+、Ag+中的某一种,阴离子分别是Cl-、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为:A:___________ ;B:___________ ;C:___________ ;D:___________ 。
(2)写出下列反应的离子方程式:
①A+D→:___________ ;
②C+HCl→气体:________ 。
(3)已知Fe3+与 在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式
在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式______ ,当某溶液X中存在 时,X中不可能大量存在的离子有
时,X中不可能大量存在的离子有______ (选填序号)。
A. B.
B. C.H+ D.Fe3+
C.H+ D.Fe3+
 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断这四种盐的化学式分别为:A:
(2)写出下列反应的离子方程式:
①A+D→:
②C+HCl→气体:
(3)已知Fe3+与
 在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式
在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式 时,X中不可能大量存在的离子有
时,X中不可能大量存在的离子有A.
 B.
B. C.H+ D.Fe3+
C.H+ D.Fe3+
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 溶于稀硝酸。
溶于稀硝酸。
(1)写出实验②生成白色沉淀涉及的离子方程式:_______ 。
(2)实验③中的白色沉淀组成为_______ (写化学式)。
(3)根据上述实验现象可知,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,不能确定是否存在的离子是_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量
 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;③向第三份溶液中先加入
 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。已知:
 溶于稀硝酸。
溶于稀硝酸。(1)写出实验②生成白色沉淀涉及的离子方程式:
(2)实验③中的白色沉淀组成为
(3)根据上述实验现象可知,原溶液中一定存在的离子是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】实验室里需要纯净的氯化钠溶液,但手头只有混有硫酸钠的氯化钠。某学生设计了如下方案:

如果此方案正确,那么:
(1)写出碳酸钠在水中的电离方程式:___ ;
(2)操作①是否可改为加硝酸钡溶液?____ 。理由是____ 。
(3)进行操作①后,如何判断硫酸根离子已除尽,方法是___ 。
(4)操作②的目的是___ ,不先过滤再加碳酸钠溶液的原因是___ 。

如果此方案正确,那么:
(1)写出碳酸钠在水中的电离方程式:
(2)操作①是否可改为加硝酸钡溶液?
(3)进行操作①后,如何判断硫酸根离子已除尽,方法是
(4)操作②的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室有一瓶标签损坏的盐溶液,某同学为确定其组成,设计实验进行验证。
(1)实验步骤如下,请补全空白:
①用洁净的铂丝蘸取少许溶液,在酒精灯上灼烧,透过___ 观察,火焰呈紫色,说明溶液中含有___ 。
②取少量溶液于试管中,滴加NaOH溶液产生白色沉淀,继续滴加NaOH溶液,沉淀溶解。
③另取少量溶液于试管中,先滴加___ 酸化,再加入___ ,若有白色沉淀产生,则证明溶液中有SO 。
。
(2)步骤②的实验现象说明盐溶液中含有___ ,写出沉淀溶解时发生反应的离子方程式___ 。
(3)若该溶液的溶质只有一种,根据实验结果判断该溶质应为___ 。
(1)实验步骤如下,请补全空白:
①用洁净的铂丝蘸取少许溶液,在酒精灯上灼烧,透过
②取少量溶液于试管中,滴加NaOH溶液产生白色沉淀,继续滴加NaOH溶液,沉淀溶解。
③另取少量溶液于试管中,先滴加
 。
。(2)步骤②的实验现象说明盐溶液中含有
(3)若该溶液的溶质只有一种,根据实验结果判断该溶质应为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量 CaCl2、MgCl2、Na2SO4等杂质,实验室提供的试剂如下:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液。实验室提纯NaCl的流程如图:

(1)欲除去溶液I中的杂质,写出A所代表的多种试剂,按滴加顺序依次为 NaOH;_________ ;______ (填化学式)。
(2)操作a、b中均用到的玻璃仪器是烧杯和_____ (填仪器名称),操作c的名称为__________ 。
(3)如何对操作b所得到的沉淀进行洗涤:_____________________ 。
(4)经过操作b后,如何检验所得溶液中的 已除去:
已除去:______________ 。
(5)若上述流程中未进行操作b,即直接向溶液1中加盐酸到pH为4~5,过滤,得到沉淀X和溶液Y,则沉淀X为___ (写化学式)。

(1)欲除去溶液I中的杂质,写出A所代表的多种试剂,按滴加顺序依次为 NaOH;
(2)操作a、b中均用到的玻璃仪器是烧杯和
(3)如何对操作b所得到的沉淀进行洗涤:
(4)经过操作b后,如何检验所得溶液中的
 已除去:
已除去:(5)若上述流程中未进行操作b,即直接向溶液1中加盐酸到pH为4~5,过滤,得到沉淀X和溶液Y,则沉淀X为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
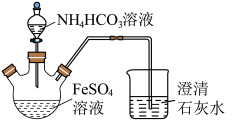
【推荐1】碳酸亚铁(FeCO3)难溶于水,常用于制取铁盐或补血剂。一种FeCO3的制备装置如图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得FeCO3沉淀。______________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:__________________ 。
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程_________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O
 =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是________ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有________ ,有关的离子方程式为____________ 。
(4)检验原溶液可能存在的阳离子的方法和结论是________
(5)原溶液可能大量共存的阴离子是________ (填字母序号)。
A.Cl- B.NO C.CO
C.CO D.OH-
D.OH-
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)检验原溶液可能存在的阳离子的方法和结论是
(5)原溶液可能大量共存的阴离子是
A.Cl- B.NO
 C.CO
C.CO D.OH-
D.OH-
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】为了将混有CaCl2、MgCl2、Na2SO4和难溶性杂质的粗盐进行提纯,某同学设计了如图实验方案:

请回答下列问题:
(1)操作①为___ 。
(2)操作②~④加入的试剂依次是___ 、___ 、___ 。
(3)写出过滤操作中所使用的玻璃仪器除了烧杯外,还需要___ 、___ 。
(4)简述判断SO 已除尽的方法
已除尽的方法___ 。
(5)工业上用电解精制的饱和食盐水的方法制取氯气,方程式为___ ,理论上每产生标准状况下5.6LCl2,转移电子的物质的量为___ 。

请回答下列问题:
(1)操作①为
(2)操作②~④加入的试剂依次是
(3)写出过滤操作中所使用的玻璃仪器除了烧杯外,还需要
(4)简述判断SO
 已除尽的方法
已除尽的方法(5)工业上用电解精制的饱和食盐水的方法制取氯气,方程式为
您最近一年使用:0次



