下列依据热化学方程式得出的结论正确的是
| A.已知C(s)+O2(g)=CO(g) ∆H=-akJmol-1,则1molC(s)完全燃烧放出的热大于akJ·mol-1 |
| B.已知SO2(g)+2H2S(g)=3S(s)+2H2O(l)常温下自发进行,则可推知一定∆H>0 |
| C.已知2H2(g)+O2(g)=2H2O(g) ∆H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ·mol-1 |
| D.已知C(石墨,s)=C(金刚石,s) ∆H>0,则金刚石比石墨稳定 |
更新时间:2024-01-03 12:51:15
|
相似题推荐
【推荐1】自由基是化学键断裂时产生的含未成对电子的中间体,活泼自由基与氧气的反应一直是科研人员的关注点,HNO自由基与O2反应过程的能量变化如图所示,下列说法不正确是


| A.三种中间产物中稳定顺序为:X<Y<Z |
| B.该历程中正反应最大的能垒为186.19kJ/mol |
| C.相同条件下Z转化为产物的速率:v(P1)>v(P2) |
| D.每生成1mol产物P2,反应吸收热量320.40kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科学家研究化合物M(s)催化CO2氢化机理。由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如图所示(已知1eV=1.6×10-19J,NA约为6.02×1023mol-1)。TS1、TS2均为过渡态。下列说法不正确 的是


| A.过渡态TS1比TS2更稳定 |
| B.过程TS1→P为化合物M生成化合物N的决速步骤 |
| C.化合物M催化CO2氢化反应过程中一定有Fe-O键的断裂 |
| D.该过程的热化学方程式为:M(s)+CO2(g)=N(s) ΔH=-1120.2kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】根据下列图示所得出的结论正确的是


A.图甲表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| B.图乙是金刚石与石墨分别氧化生成CO2的能量关系曲线,说明石墨转化为金刚石的反应的ΔH>0 |
| C.图丙表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率大于b点 |
| D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:101kPa时,1mol辛烷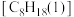 完全燃烧生成液态水时放出的热量为5518kJ;强酸和强碱在稀溶液中发生反应生成1mol液态水时放出的热量为57.3kJ,则下列热化学方程式书写正确的是
完全燃烧生成液态水时放出的热量为5518kJ;强酸和强碱在稀溶液中发生反应生成1mol液态水时放出的热量为57.3kJ,则下列热化学方程式书写正确的是
①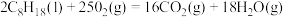
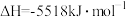
②
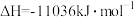
③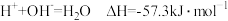
④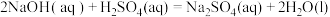
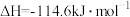
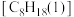 完全燃烧生成液态水时放出的热量为5518kJ;强酸和强碱在稀溶液中发生反应生成1mol液态水时放出的热量为57.3kJ,则下列热化学方程式书写正确的是
完全燃烧生成液态水时放出的热量为5518kJ;强酸和强碱在稀溶液中发生反应生成1mol液态水时放出的热量为57.3kJ,则下列热化学方程式书写正确的是①
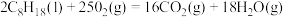
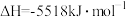
②

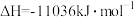
③
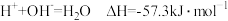
④
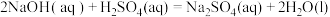
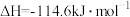
| A.①③ | B.②③ | C.②④ | D.只有② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列依据热化学方程式得出的结论正确的是
A.已知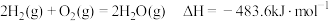 ,则氢气的燃烧热为 ,则氢气的燃烧热为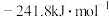 |
B.已知C(石墨,s)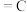 (金刚石,s) (金刚石,s)  ,则石墨比金刚石更稳定 ,则石墨比金刚石更稳定 |
C. 、 、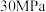 下,将 下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放热 ,放热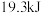 ,则其热化学方程式 ,则其热化学方程式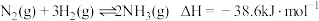 |
| D.中和热的测定实验中,氢氧化钠分批加入反应更充分,测定的中和热数值误差更小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】可以用图示法分析化学反应中的能量变化,下列说法不正确的是
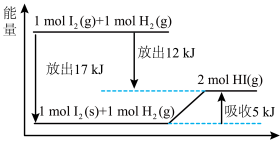

| A.2molI2(s)与过量H2(g)化合生成4molHI(g)时,需要吸收10kJ的能量 |
| B.1molI2(s)变为1molI2(g)时,需要吸收17kJ的能量 |
| C.2molHI(g)分解生成1molI2(g)与1molH2(g)时,需要吸收12kJ的能量 |
| D.2molHI(l)分解生成1molI2(s)与1molH2(g)时,需要放出5kJ的能量 |
您最近一年使用:0次
【推荐2】为研究反应 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程及图象如下:
和I-的混合溶液中加入Fe3+,过程及图象如下:
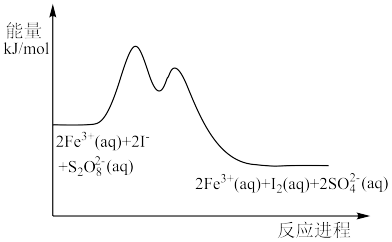
步骤①:2Fe3+(aq)+2I-(aq)=I2(aq)+2Fe2+(aq) ΔH1
步骤②:2Fe2+(aq)+ (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq) ΔH2
(aq) ΔH2
下列有关该反应的说法不正确的是
 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程及图象如下:
和I-的混合溶液中加入Fe3+,过程及图象如下:
步骤①:2Fe3+(aq)+2I-(aq)=I2(aq)+2Fe2+(aq) ΔH1
步骤②:2Fe2+(aq)+
 (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq) ΔH2
(aq) ΔH2下列有关该反应的说法不正确的是
| A.Fe3+是该反应的催化剂 |
| B.步骤②比步骤①快 |
| C.ΔH1<ΔH2 |
| D.步骤①和②均发生了氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是( )
| A.101kPa时,2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,则H2的燃烧热ΔH=-572kJ·mol-1 |
B.一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ 2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ |
| C.若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D.已知:2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH,该反应在一定条件下能自发,则下列关于该反应的ΔH、ΔS的判断,正确的是
2NH3(g) ΔH,该反应在一定条件下能自发,则下列关于该反应的ΔH、ΔS的判断,正确的是
 2NH3(g) ΔH,该反应在一定条件下能自发,则下列关于该反应的ΔH、ΔS的判断,正确的是
2NH3(g) ΔH,该反应在一定条件下能自发,则下列关于该反应的ΔH、ΔS的判断,正确的是| A.ΔH<0 ΔS>0 | B.ΔH<0 ΔS<0 |
| C.ΔH>0 ΔS<0 | D.ΔH>0 ΔS>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.Cl2溶于水得到的氯水能导电,但Cl2不是电解质,而是非电解质 |
| B.以铁作阳极,铂作阴极,电解饱和食盐水,可以制备烧碱 |
C.将1mol Cl2通入水中,HClO、Cl-、ClO-粒子数之和为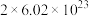 |
D.反应Al2O3(s)+3Cl2(g)+3C(s)═2AlCl3(g)+3CO(g)室温下不能自发进行,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:25℃、101kPa下:
I.2Na(s)+ O2(g)=Na2O(s) △H=-412kJ·mol-1
O2(g)=Na2O(s) △H=-412kJ·mol-1
II.2Na(s)+O2(g)=Na2O2(s) △H=-511kJ·mol-1
III.2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
IV.Na2O2(s)+CO2(g)=Na2CO3(g)+ O2(g) △H=-226kJ·mol-1
O2(g) △H=-226kJ·mol-1
下列说法正确的是
I.2Na(s)+
 O2(g)=Na2O(s) △H=-412kJ·mol-1
O2(g)=Na2O(s) △H=-412kJ·mol-1II.2Na(s)+O2(g)=Na2O2(s) △H=-511kJ·mol-1
III.2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
IV.Na2O2(s)+CO2(g)=Na2CO3(g)+
 O2(g) △H=-226kJ·mol-1
O2(g) △H=-226kJ·mol-1下列说法正确的是
| A.相同条件下,1mol[2Na(s)+O2(g)]的能量小于1mol[Na2O2(s)]的能量 |
| B.低温不利于CO与Na2O2自发生成碳酸钠 |
| C.反应I的活化能小于反应II的活化能 |
| D.Na2O不可能分解为Na2O2和Na |
您最近一年使用:0次


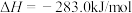
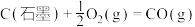 的ΔH,可由C(石墨)和CO的燃烧热计算
的ΔH,可由C(石墨)和CO的燃烧热计算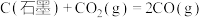 在任何温度下均不能自发进行
在任何温度下均不能自发进行

