化学从宏-微结合的视角研究物质的变化过程,并运用化学符号进行表征。
(1)观察下图的微观反应过程,写出该化学反应方程式___________ 。

(2)画出氧原子的结构示意图___________ ;氯离子的电子式___________ 。
(3)电解水时,通常向纯水中加入适量的 不参加反应),原因是
不参加反应),原因是___________ 。(请使用化学用语解释)
(4)某电解水实验开始时,向 纯水中溶解了
纯水中溶解了 此时溶液中
此时溶液中 和水分子的个数比是
和水分子的个数比是___________ ,该 溶液的物质的量浓度约为
溶液的物质的量浓度约为___________  。(保留2位有效数字,水和
。(保留2位有效数字,水和 溶液的密度近似为
溶液的密度近似为 )。
)。
(5)当实验进行到一段时间,两个电极共收集到的气体折合成标准状况约是 (不考虑气体溶解)。计算此时被电解的水的物质的量是
(不考虑气体溶解)。计算此时被电解的水的物质的量是___________ 。
(6)实际收集气体的外界条件并非标况。该条件下气体摩尔体积是 ,阿伏伽德罗常数的值是
,阿伏伽德罗常数的值是 ,当收集到氢气的体积是VL时,则同时收集到的氧气分子的个数是
,当收集到氢气的体积是VL时,则同时收集到的氧气分子的个数是___________ 。
(1)观察下图的微观反应过程,写出该化学反应方程式

(2)画出氧原子的结构示意图
(3)电解水时,通常向纯水中加入适量的
 不参加反应),原因是
不参加反应),原因是(4)某电解水实验开始时,向
 纯水中溶解了
纯水中溶解了 此时溶液中
此时溶液中 和水分子的个数比是
和水分子的个数比是 溶液的物质的量浓度约为
溶液的物质的量浓度约为 。(保留2位有效数字,水和
。(保留2位有效数字,水和 溶液的密度近似为
溶液的密度近似为 )。
)。(5)当实验进行到一段时间,两个电极共收集到的气体折合成标准状况约是
 (不考虑气体溶解)。计算此时被电解的水的物质的量是
(不考虑气体溶解)。计算此时被电解的水的物质的量是(6)实际收集气体的外界条件并非标况。该条件下气体摩尔体积是
 ,阿伏伽德罗常数的值是
,阿伏伽德罗常数的值是 ,当收集到氢气的体积是VL时,则同时收集到的氧气分子的个数是
,当收集到氢气的体积是VL时,则同时收集到的氧气分子的个数是
更新时间:2024-01-05 21:07:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钠元素在自然界中普遍存在。
(1)画出钠的原子结构示意图___________ ,根据原子结构示意图,钠具有___________ (填“氧化性”或“还原性”)
(2)钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.钠不断与水反应,直到反应完全;
E.生成的氢氧化钠使酚酞试液变红。
请在下发填写。描述的现象相对应的原因。
(3)写出钠与水反应的化学方程式:___________ 。
(4)金属钠着火时用___________进行灭火
(1)画出钠的原子结构示意图
(2)钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.钠不断与水反应,直到反应完全;
E.生成的氢氧化钠使酚酞试液变红。
请在下发填写。描述的现象相对应的原因。
| 实验现象 | 原因(填以上序号) |
| 钠浮在水面上 | |
| 熔成闪亮的小球 | |
| 小球向各个方向迅速游动,并发出“嘶嘶”的声音 | |
| 小球逐渐变小以后完全消失 | |
| 在反应后的溶液中滴入酚酞试液显红色 |
(3)写出钠与水反应的化学方程式:
(4)金属钠着火时用___________进行灭火
| A.水 | B.泡沫灭火器 | C.干粉灭火器 | D.干燥的沙土 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2020年12月17日凌晨,嫦娥五号圆满完成任务,携月壤凯旋归来。不同组分月壤中的Rb-Sr同位素组成差异是研究月球表面演化历史的依据,Ca9NaMg(PO4)7是新矿物“嫦娥石”的一种成分。
(1)Ca9NaMg(PO4)7属于___________ 。
A.酸式盐 B.磷酸盐 C.弱电解质 D.离子化合物
该晶体在熔融状态下的电离方程式为___________ 。
(2)87Sr、90Sr是锶元素两种核素,它们具有相同的___________。
(3)自然界中磷元素主要以磷酸盐的形式存在。磷的两种分子如下图所示:
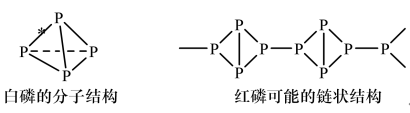
①图中用“*”标出的化学键类型为___________ ;红磷和白磷互为___________ 。
②6.2g的白磷全部转化成红磷,需要断开________ 根化学键。(用含阿伏加德罗常数NA的代数式表示)
③31P的质量数常被作为磷元素的近似相对原子质量。其中“近似”的含义不包括___________ 。
A.质子和中子的相对原子质量都接近1
B.元素的近似相对原子质量约等于质量
C.核外电子的质量太小,可忽略不计
D.磷的其他同位素的丰度太低,可忽略不计
(4)已知铷原子(Rb)的核电荷数为37,次外层电子数与其L层上所带电子数相等,其简单离子的带电性与钠离子相同,画出铷的原子结构示意图:___________ 。
(1)Ca9NaMg(PO4)7属于
A.酸式盐 B.磷酸盐 C.弱电解质 D.离子化合物
该晶体在熔融状态下的电离方程式为
(2)87Sr、90Sr是锶元素两种核素,它们具有相同的___________。
| A.质子数 | B.质量数 | C.中子数 | D.物理性质 |
(3)自然界中磷元素主要以磷酸盐的形式存在。磷的两种分子如下图所示:

①图中用“*”标出的化学键类型为
②6.2g的白磷全部转化成红磷,需要断开
③31P的质量数常被作为磷元素的近似相对原子质量。其中“近似”的含义不包括
A.质子和中子的相对原子质量都接近1
B.元素的近似相对原子质量约等于质量
C.核外电子的质量太小,可忽略不计
D.磷的其他同位素的丰度太低,可忽略不计
(4)已知铷原子(Rb)的核电荷数为37,次外层电子数与其L层上所带电子数相等,其简单离子的带电性与钠离子相同,画出铷的原子结构示意图:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】新型陶瓷材料氮化硅(Si3N4)可用于制作火箭发动机中燃料的喷嘴。氮化硅可由石英、焦炭在高温氮气流中制取。完成下列填空:
SiO2 +______C +_____N2 ______Si3N4 + ________CO
______Si3N4 + ________CO
(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目_____ 。
(2)反应中___________ 被还原,当氧化产物比还原产物多1mol时,反应中电子转移数为___________ 。
(3)在该反应体系中:所涉及物质属于单质的电子式为___________ ;所涉及元素中原子半径最大的原子的结构示意图为___________ 。
SiO2 +______C +_____N2
 ______Si3N4 + ________CO
______Si3N4 + ________CO(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目
(2)反应中
(3)在该反应体系中:所涉及物质属于单质的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D四种物质之间有下图所示的转化关系。已知A是气体单质,C是红棕色气体。

回答下列问题:
(1)A的电子式:_______ ,C的化学式:_______ 。
(2)在上图D→B的过程中,D表现出强_______ (填“氧化性”或“还原性”)。
(3)写出C→D转化的化学方程式:_______ 。

回答下列问题:
(1)A的电子式:
(2)在上图D→B的过程中,D表现出强
(3)写出C→D转化的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列9种微粒: 、
、 、
、 、
、 、
、 、
、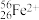 、
、 、
、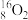 、
、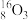 。按要求完成以下各题:
。按要求完成以下各题:
(1)互为同素异形体的微粒是_______ 。
(2)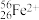 的中子数为
的中子数为_______ ,核外电子数为_______ 。
(3)形成上述9种微粒的核素有_______ 种,元素有_______ 种。
(4)写出下列物质的电子式:NH4Cl_______ ,N2_______ ,HClO_______ 。
(5)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是_______ ;只含有共价键的是_______ ;既含有离子键又含有共价键的是_______ ;含有非极性共价键的化合物是_______ ;不含化学键的是_______ ;属于电解质的是_______ ,属于非电解质的是_______
 、
、 、
、 、
、 、
、 、
、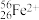 、
、 、
、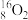 、
、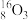 。按要求完成以下各题:
。按要求完成以下各题:(1)互为同素异形体的微粒是
(2)
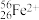 的中子数为
的中子数为(3)形成上述9种微粒的核素有
(4)写出下列物质的电子式:NH4Cl
(5)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)l0Be和9Be_____________ (填序号)。
a.是同一种原子 b.具有相同的中子数 c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:_________________________ 。
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是____________ (填序号)。
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
II.下表列出了①~⑩10种元素在周期表中的位置。
(1)上述元素中,金属性最强的是(填元素符号,下同)________ ,③④⑤三种元素的原子半径由大到小的顺序是____________ 。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________ (填化学式)
(3)元素⑥的氢化物的电子式为____________ ,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为_______________________________________ 。
(1)l0Be和9Be
a.是同一种原子 b.具有相同的中子数 c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
II.下表列出了①~⑩10种元素在周期表中的位置。
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑩ | |||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | |||
| 4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是
(3)元素⑥的氢化物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】向含有0.8mol的稀硝酸溶液中慢慢加入22.4g的铁粉。假设反应分为两个阶段。第一阶段为:Fe+HNO3→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段反应的离子方程式___________ 、___________ 。
(2)求这两个阶段反应中,加入铁粉的物质的量和溶液中铁元素存在的形式_________ 。
(3)在图中画出溶液中Fe2+、 离子的物质的量随加入铁粉的物质的量变化的关系图像
离子的物质的量随加入铁粉的物质的量变化的关系图像___________ (纵坐标是溶液中离子的物质的量)。

(1)写出这两个阶段反应的离子方程式
(2)求这两个阶段反应中,加入铁粉的物质的量和溶液中铁元素存在的形式
(3)在图中画出溶液中Fe2+、
 离子的物质的量随加入铁粉的物质的量变化的关系图像
离子的物质的量随加入铁粉的物质的量变化的关系图像
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)下列数量的各物质所含原子数按由大到小的顺序排列是________ 。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏伽德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为________ mol。
②该气体所含原子总数为________ 个。
③该气体在标准状况下的体积为________ L。
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________ mol·L-1。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏伽德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为
②该气体所含原子总数为
③该气体在标准状况下的体积为
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)若将反应Fe+H2SO4=FeSO4+H2↑设计成原电池,可用铜作该电池装置的_______ (填“正”或“负”)极,该极上发生的电极反应为_______ 。
(2)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从_______ (填“a”或“b”)口通入,该电极的电极反应为_______ 。

(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是_______ (填“正”或“负”)极,Ag2O发生_______ (填“氧化”或“还原”)反应。
②当电路通过1 mol电子时,负极消耗物质的质量是_______ g。
③在使用过程中,电解质溶液中KOH的物质的量_______ (填“增大”“减小”或“不变”)。
(1)若将反应Fe+H2SO4=FeSO4+H2↑设计成原电池,可用铜作该电池装置的
(2)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从

(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+H2O
Ag2O+H2O+2e-=2Ag+2OH-
总反应为Ag2O+Zn=ZnO+2Ag
①Zn是
②当电路通过1 mol电子时,负极消耗物质的质量是
③在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ、按要求写出方程式。
(1)碳酸钙和盐酸(写出离子方程式)__________________________________________
(2)Fe2(SO4)3(写出电离方程式)______________________________________________
(3)H+ + OH— = H2O(写出对应的化学方程式)__________________________________
Ⅱ、用单线桥 法表示下列反应电子转移的方向和数目_______ :
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
氧化剂和还原剂的物质的量之比为________ 。
(1)碳酸钙和盐酸(写出离子方程式)
(2)Fe2(SO4)3(写出电离方程式)
(3)H+ + OH— = H2O(写出对应的化学方程式)
Ⅱ、用
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸至过量,同时不断搅拌(如图所示)。
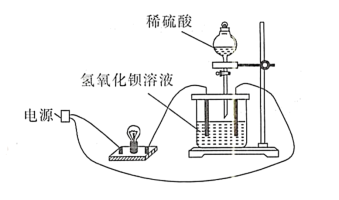
(1)主要实验现象:烧杯中___ ,小灯泡:___ 。
(2)烧杯中反应的离子方程式:___ 。
(3)下列图示能正确表示实验过程的是___ 。(填序号)
A. B.
B. C.
C.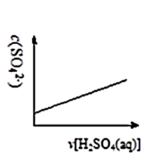

(1)主要实验现象:烧杯中
(2)烧杯中反应的离子方程式:
(3)下列图示能正确表示实验过程的是
A.
 B.
B. C.
C.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】今有10种物质:①Na;②稀硫酸;③固态醋酸;④ ;⑤石墨;⑥
;⑤石墨;⑥ ;⑦
;⑦ 胶体;⑧熔融
胶体;⑧熔融 ;⑨
;⑨ 固体;⑩NaCl溶液
固体;⑩NaCl溶液
(1)能导电的物质_______ 。(用序号填空,下同)
(2)电解质_______ ;非电解质_______ 。
(3)区分 的胶体和
的胶体和 溶液实验方法
溶液实验方法_______ ;实验室制备 胶体的原理
胶体的原理_______ 。(用化学方程式表示)
(4)将②逐滴加入到⑨的溶液中,测得混合溶液的导电能力随时间变化曲线如图所示;写出该过程发生的离子反应方程式_______ 。下列关于该图的有关说法不正确的是_______ 。

A.a时刻 溶液与稀硫酸恰好完全反应
溶液与稀硫酸恰好完全反应
B.AB段溶液的导电能力不断减弱,说明生成物不是电解质
C.B处溶液的导电能力约为0,说明溶液中几强没有自由移动的离子
 ;⑤石墨;⑥
;⑤石墨;⑥ ;⑦
;⑦ 胶体;⑧熔融
胶体;⑧熔融 ;⑨
;⑨ 固体;⑩NaCl溶液
固体;⑩NaCl溶液(1)能导电的物质
(2)电解质
(3)区分
 的胶体和
的胶体和 溶液实验方法
溶液实验方法 胶体的原理
胶体的原理(4)将②逐滴加入到⑨的溶液中,测得混合溶液的导电能力随时间变化曲线如图所示;写出该过程发生的离子反应方程式

A.a时刻
 溶液与稀硫酸恰好完全反应
溶液与稀硫酸恰好完全反应B.AB段溶液的导电能力不断减弱,说明生成物不是电解质
C.B处溶液的导电能力约为0,说明溶液中几强没有自由移动的离子
您最近一年使用:0次



