如图是饮用矿泉水标签的部分内容,阅读标签并计算。
(1)每瓶水最多含 的物质的量
的物质的量___________ 。
(2)镁离子浓度最大时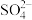 的物质的量浓度
的物质的量浓度___________ 。
| 饮用矿泉水 净含量: 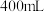 配料表:纯净水、硫酸镁、氯化钾 保质期:12个月 主要成分:水 钾离子 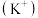 : :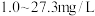 镁离子 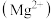 : :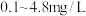 氯离子 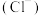 : :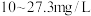 硫酸根离子  |
 的物质的量
的物质的量(2)镁离子浓度最大时
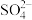 的物质的量浓度
的物质的量浓度
更新时间:2024-01-27 11:26:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)实验室常用浓盐酸与高锰酸钾发生反应快速制备少量氯气,该反应的化学方程式为: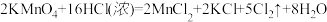 用双线桥法表示该反应过程中的电子转移情况
用双线桥法表示该反应过程中的电子转移情况______________________ ,该反应中氧化剂为____________ ,HCl的作用是______________________ 。
(2)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的离子方程式是_________________________________ 。
(3)已知在碱性溶液中可发生如下反应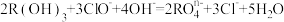 ,则
,则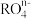 中R的化合价是
中R的化合价是________ 。
A.+3 B.+4 C.+5 D.+6
(4)填写下列空白:
①等物质的量的CO和CO2中:所含的分子数目之比为_______ ,相同条件下体积之比为_______ ,所含的原子总数目之比为_______ 。
②有下列物质:
a.硫酸 b.盐酸 c.氯气 d.硫酸钡 e.甲烷 f.铜 g.CH3COOH h.氯化氢 i.蔗糖 j.氨气 k.CO2 l.NaHCO3 m.Al(OH)3 n.NaOH溶液
其中属于非电解质的为_____________ (填序号,下同。),属于电解质的为____________ 。
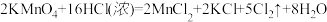 用双线桥法表示该反应过程中的电子转移情况
用双线桥法表示该反应过程中的电子转移情况(2)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的离子方程式是
(3)已知在碱性溶液中可发生如下反应
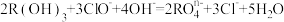 ,则
,则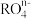 中R的化合价是
中R的化合价是A.+3 B.+4 C.+5 D.+6
(4)填写下列空白:
①等物质的量的CO和CO2中:所含的分子数目之比为
②有下列物质:
a.硫酸 b.盐酸 c.氯气 d.硫酸钡 e.甲烷 f.铜 g.CH3COOH h.氯化氢 i.蔗糖 j.氨气 k.CO2 l.NaHCO3 m.Al(OH)3 n.NaOH溶液
其中属于非电解质的为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)有以下几种物质:①铁 ②液态的HCl ③蔗糖 ④酒精 ⑤稀盐酸 ⑥H2SO4 ⑦KOH ⑧熔融的KNO3 ⑨O2⑩干冰。试回答(填序号):以上物质能导电的是_______ ,属于电解质的是_______
(2)写出下列反应的离子方程式:
碳酸钠溶液与足量盐酸:_______
澄清石灰水与足量盐酸:_______
(3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
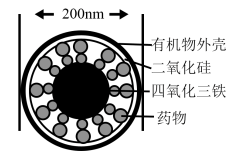
①“纳米药物分子运输车”分散于水中所得的分散系_______ (填“属于”或“不属于”)胶体。
②从元素组成的角度分析,CO2和Fe3O4可归为同一类物质,其类别属于化合物中的_______
(4)已知反应2F2+2H2O=4HF+O2请用双线桥表示出该反应的电子转移方向和数目_______
(5)计算:①1.5molH2SO4的质量是_______ g
②等质量的CO和CO2中氧原子个数之比为_______
(1)有以下几种物质:①铁 ②液态的HCl ③蔗糖 ④酒精 ⑤稀盐酸 ⑥H2SO4 ⑦KOH ⑧熔融的KNO3 ⑨O2⑩干冰。试回答(填序号):以上物质能导电的是
(2)写出下列反应的离子方程式:
碳酸钠溶液与足量盐酸:
澄清石灰水与足量盐酸:
(3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:

①“纳米药物分子运输车”分散于水中所得的分散系
②从元素组成的角度分析,CO2和Fe3O4可归为同一类物质,其类别属于化合物中的
(4)已知反应2F2+2H2O=4HF+O2请用双线桥表示出该反应的电子转移方向和数目
(5)计算:①1.5molH2SO4的质量是
②等质量的CO和CO2中氧原子个数之比为
您最近一年使用:0次
【推荐3】呼吸面具中的Na2O2可吸收CO2放出O2,若用超氧化钾(KO2)代替Na2O2也可以得到类似的产物,起到同样的作用。
(1)标准状况下,若有30mL的CO2气体通过盛有足量的KO2的装置充分反应后,逸出气体的体积为_______ mL;
(2)标准状况下,若一定量的CO2(过量),通过盛有7.24gKO2和Na2O2的均匀混合物的装置充分反应后,逸出的气体中O2体积为1568mL,则混合物中KO2和Na2O2的物质的量分别为:KO2_______ mol、Na2O2_______ mol;
(3)比较Na2O2和KO2中氧氧键的键能大小,并说明理由:_______ 。
(1)标准状况下,若有30mL的CO2气体通过盛有足量的KO2的装置充分反应后,逸出气体的体积为
(2)标准状况下,若一定量的CO2(过量),通过盛有7.24gKO2和Na2O2的均匀混合物的装置充分反应后,逸出的气体中O2体积为1568mL,则混合物中KO2和Na2O2的物质的量分别为:KO2
(3)比较Na2O2和KO2中氧氧键的键能大小,并说明理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】计算题
I.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量为_______ 。(写出计算过程,下同)
(2)反应后ZnCl2的物质的量浓度_______ 。
(3)生成H2的体积(标准状况)_______ 。
II.实验室用密度为 、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为_______ 。
I.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量为
(2)反应后ZnCl2的物质的量浓度
(3)生成H2的体积(标准状况)
II.实验室用密度为
 、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。(4)该浓盐酸中溶质的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学用10mol/L的浓盐酸配制250mL1mol/L的稀盐酸,并进行有关实验。请回答下列问题:
(1)需要量取浓盐酸__________ mL。
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒、还必须用到的仪器有__________ 、__________ 等。
(3)取所配制的稀盐酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为__________ 。
(1)需要量取浓盐酸
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒、还必须用到的仪器有
(3)取所配制的稀盐酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为
您最近一年使用:0次



