电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知: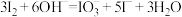 。下列说法不正确的是
。下列说法不正确的是

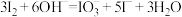 。下列说法不正确的是
。下列说法不正确的是
A.电解结束时,右侧溶液中含有 |
B.左侧发生的电极方程式: |
C.电解槽内发生反应的总化学方程式: |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式会改变 |
更新时间:2024-01-28 10:44:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】近年来,电化学法催化还原二氧化碳因其反应条件温和、能耗低绿色环保而备受研究者的青睐。将电解食盐水氧化生成次氯酸盐的阳极反应与电催化还原CO2的阴极反应相耦合,不仅实现低电位下高效电催化还原CO,还提高了电解反应的能源效率。下列说法正确的是


| A.阳极区可使用海水提供C1-,不影响电极反应 |
| B.阴极的电极反应式为CO2 + H2O +2e-= CO + 2OH - |
| C.反应生成次氯酸盐和CO,整个反应过程的原子利用率接近100% |
| D.若反应开始时,两电极区溶液质量相等,转移2 mol电子时,两电极区溶液质量差16 g(忽略气体溶解) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
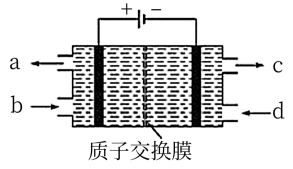
【推荐2】空气污染物NO通常用含Ce4+的溶液吸收,生成HNO2、 ,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是
,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是
 ,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是
,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是
| A.H+由右室进入左室 |
| B.Ce4+从电解槽的c口流出,且可循环使用 |
| C.若用甲烷燃料电池作为电源,当消耗33.6L甲烷时,理论上可转化2molHNO2 |
| D.阴极的电极反应式:2HNO2+6H++6e-=N2↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】将 电催化转化成燃料和化学品具有重要意义。甲酸可以作为氢载体直接用于甲酸燃料电池。某科学家在常温下用S-In催化剂电催化还原
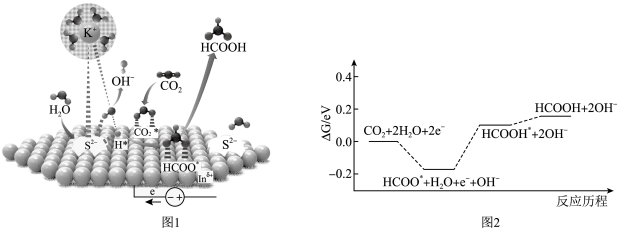
电催化转化成燃料和化学品具有重要意义。甲酸可以作为氢载体直接用于甲酸燃料电池。某科学家在常温下用S-In催化剂电催化还原 制甲酸的机理如图甲所示,反应历程如图乙所示,其中吸附在催化剂表面的原子用*标注。下列说法错误的是
制甲酸的机理如图甲所示,反应历程如图乙所示,其中吸附在催化剂表面的原子用*标注。下列说法错误的是
 电催化转化成燃料和化学品具有重要意义。甲酸可以作为氢载体直接用于甲酸燃料电池。某科学家在常温下用S-In催化剂电催化还原
电催化转化成燃料和化学品具有重要意义。甲酸可以作为氢载体直接用于甲酸燃料电池。某科学家在常温下用S-In催化剂电催化还原 制甲酸的机理如图甲所示,反应历程如图乙所示,其中吸附在催化剂表面的原子用*标注。下列说法错误的是
制甲酸的机理如图甲所示,反应历程如图乙所示,其中吸附在催化剂表面的原子用*标注。下列说法错误的是
| A.使用S-In催化剂,可以降低反应的活化能 |
B. 在催化剂表面 在催化剂表面 的催化作用下转化为 的催化作用下转化为 和 和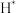 |
C.电催化还原 制甲酸的总反应式为 制甲酸的总反应式为 |
| D.电催化还原制备甲酸时,阳极电势比阴极低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】南开大学陈军院士团队研究了一种K-CO2可充电电池,该电池以KSn合金为电极材料, MWCNTs- COOH为电极催化剂,其工作原理示意图如下。研究表明,该电池的优势源于K和Sn的合金反应:K+Sn=KSn,原电池的电流效率(电路中通过的电子数与电池反应中转移的电子数之比)为80%。下列说法错误的是


| A.放电时,Y极的电极反应式为KSn−e−=K++Sn |
| B.放电时,K+由Y极向X极方向迁移 |
| C.放电时,外电路中每转移1 mol e−,消耗16.8 L(标准状况) CO2 |
| D.充电时,X极的电极反应式为2K2CO3+C−4e−=4K++3CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上以软锰矿(主要成分为MnO2,另含有少量FeCO3、Al2O3、SiO2)为原料制取金属锰的工艺流程如下:
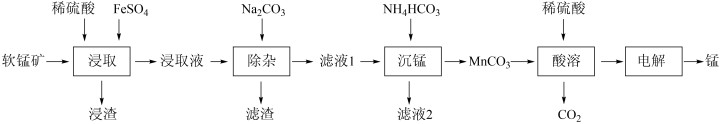
下列有关说法正确的是

下列有关说法正确的是
| A.浸取软锰矿时,加入FeSO4会引入杂质,因此是多余的 |
| B.若浸取液中无Fe2+存在,则加入的Na2CO3主要目的是除去Fe3+、Al3+。为除杂彻底,加入Na2CO3需过量,使溶液呈碱性 |
C.沉锰时的离子方程式为:Mn2++2 =MnCO3↓+H2O+CO2↑ =MnCO3↓+H2O+CO2↑ |
| D.电解时,锰元素在负极被氧化 |
您最近一年使用:0次

 FeO
FeO +3H2↑,其工作原理如图所示。下列叙述正确的是
+3H2↑,其工作原理如图所示。下列叙述正确的是


