(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是 。
(2)将2.4mol某金属投入某酸溶液中,恰好完全反应,并产生7.2g氢气,则此金属化合价为 。
(3)某同学为探究铜铁合金中铁的质量分数,先后进行了三次实验,实验数据如下:
①该合金中铁的质量分数是 %(结果精确到1%)。
②本实验中所加稀硫酸的溶质的质量分数为 %(结果精确到0.1%)。
(2)将2.4mol某金属投入某酸溶液中,恰好完全反应,并产生7.2g氢气,则此金属化合价为 。
(3)某同学为探究铜铁合金中铁的质量分数,先后进行了三次实验,实验数据如下:
| 实验次数 项目 | 第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 20 | 20 | 40 |
| 所加稀硫酸的质量/g | 100 | 120 | 80 |
| 生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
①该合金中铁的质量分数是 %(结果精确到1%)。
②本实验中所加稀硫酸的溶质的质量分数为 %(结果精确到0.1%)。
14-15高一上·广东广州·期末 查看更多[2]
更新时间:2014-06-23 14:48:01
|
【知识点】 氧化还原反应
相似题推荐
【推荐1】氧化还原反应在工农业生产、日常生活中具有广泛用途,下图物质转化中实现了循环,减少了有害物质向环境的排放,回答下列问题。

(1)Na2Cr2O7中Cr元素的化合价是___________ ,在上述转化中,Cr元素化合价不变的步骤是___________ (填序号)。
(2)下列物质中能实现反应①转化的是___________ 。(填字母)
a.KMnO4 b.HCl c.O2
所选物质参与反应①转化中,Na2Cr2O7发生___________ 反应(填“氧化”或“还原”),该反应有黄绿色气体生成,写出反应的化学方程式:___________ 。
(3)向Cr(OH)3中加入NaOH浓溶液可实现反应③,写出该反应的化学方程式:___________ 。
(4)反应④在碱性条件下发生,反应的离子方程式为: ,请将
,请将 所缺的物质补充完整并配平方程式
所缺的物质补充完整并配平方程式___________ 。

(1)Na2Cr2O7中Cr元素的化合价是
(2)下列物质中能实现反应①转化的是
a.KMnO4 b.HCl c.O2
所选物质参与反应①转化中,Na2Cr2O7发生
(3)向Cr(OH)3中加入NaOH浓溶液可实现反应③,写出该反应的化学方程式:
(4)反应④在碱性条件下发生,反应的离子方程式为:
 ,请将
,请将 所缺的物质补充完整并配平方程式
所缺的物质补充完整并配平方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在高中化学中是一类重要的反应类型。 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:
(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
(2)实验室迅速制备少量氯气可利用如下反应: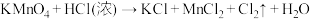 (未配平)。
(未配平)。
①上述反应中被还原的元素为_______ (填元素符号)。
②浓盐酸在反应中表现出的性质是:_______ 。
A.只有还原性B.还原性和酸性C.只有氧化性D.氧化性和酸性
③ 与
与 反应生成
反应生成 ,则
,则 发生
发生_______ 反应(填“氧化”或“还原”)。
(3) 溶液能与
溶液能与 反应制作印刷电路板。其制作原理可用
反应制作印刷电路板。其制作原理可用 表示。式中X的化学式为
表示。式中X的化学式为_______ 。
 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
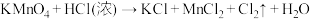 (未配平)。
(未配平)。①上述反应中被还原的元素为
②浓盐酸在反应中表现出的性质是:
A.只有还原性B.还原性和酸性C.只有氧化性D.氧化性和酸性
③
 与
与 反应生成
反应生成 ,则
,则 发生
发生(3)
 溶液能与
溶液能与 反应制作印刷电路板。其制作原理可用
反应制作印刷电路板。其制作原理可用 表示。式中X的化学式为
表示。式中X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】利用“价类二维图”可以从不同角度研究含铁物质的性质及其转化关系,图中甲~戊均含铁元素。回答下列问题:

(1)Na2FeO4是一种新型饮用水消毒剂。工业上常用NaClO、Fe(NO3)3、NaOH制备:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为______ 。
(2)打印机使用的墨粉中含有Fe3O4,下列关于Fe3O4的说法正确的是______ (填标号)。
(3)维生素C易溶于水,可将Fe3+转化为Fe2+被人体吸收。为检验转化产物Fe2+,设计如下实验:取适量Fe2(SO4)3溶液置于试管中,加入过量维生素C片振荡溶解后,滴加酸性高锰酸钾溶液,紫色褪去。该设计方案能否检验Fe2+并说明理由______ 。
(4)丁与烧碱溶液反应可生成乙,在空气中放置一段时间后乙转化为丙。乙转化为丙的现象为______ ,发生反应的化学方程式为______ 。
(5)若用丁溶液经一系列反应来制备Fe2O3。不考虑过程损失,若100mL丁溶液最终制得1.6gFe2O3,变质前丁溶液的物质的量浓度为______ 。

(1)Na2FeO4是一种新型饮用水消毒剂。工业上常用NaClO、Fe(NO3)3、NaOH制备:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为(2)打印机使用的墨粉中含有Fe3O4,下列关于Fe3O4的说法正确的是
| A.有磁性,是FeO与Fe2O3的混合物 |
| B.属于两性氧化物,与酸、碱都能反应 |
| C.Fe3O4与稀盐酸反应生成Fe2+与Fe3+物质的量之比为1:2 |
| D.Fe与水蒸气在高温下反应能生成Fe3O4 |
(4)丁与烧碱溶液反应可生成乙,在空气中放置一段时间后乙转化为丙。乙转化为丙的现象为
(5)若用丁溶液经一系列反应来制备Fe2O3。不考虑过程损失,若100mL丁溶液最终制得1.6gFe2O3,变质前丁溶液的物质的量浓度为
您最近一年使用:0次



