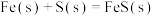载人飞船中通过如下过程实现 再生:
再生:
①
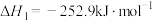
②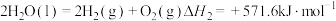
下列说法错误的是
 再生:
再生:①

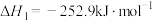
②
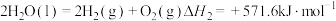
下列说法错误的是
A. 的燃烧热 的燃烧热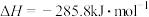 |
B.反应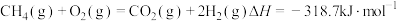 |
C.反应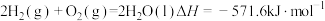 |
D.反应 |
更新时间:2024-02-04 20:15:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列依据热化学方程式得出的结论正确的是
| A.已知2SO2(g)+O2(g)=2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)=C(金刚石,s)ΔH>0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1,则任何酸碱中和反应的热效应均为57.3 kJ |
| D.在25℃、101kPa时,已知C(s)+O2(g)=CO2(g) ΔH,则C的燃烧热为-ΔH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.乙醇的燃烧热为ΔH=-akJ·mol-1,则乙醇燃烧的热化学方程式可表示为:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)ΔH=-akJ·mol-1 |
| B.稀硫酸与氢氧化钡溶液反应的中和热ΔH=-57.3kJ·mol-1 |
| C.S(g)+O2(g)=SO2(g)ΔH=-akJ·mol-1,S(s)+O2(g)=SO2(g)ΔH=-bkJ·mol-1,则a>b |
D.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)ΔH=-38.6kJ·mol-1 2NH3(g)ΔH=-38.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】 与
与 重整生成
重整生成 和CO的过程中主要发生下列反应:
和CO的过程中主要发生下列反应:

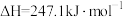

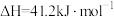
在恒压、反应物起始物质的量比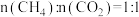 条件下,
条件下, 和
和 的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是

 与
与 重整生成
重整生成 和CO的过程中主要发生下列反应:
和CO的过程中主要发生下列反应:
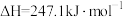

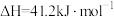
在恒压、反应物起始物质的量比
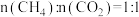 条件下,
条件下, 和
和 的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
A.曲线B表示 的平衡转化率随温度的变化 的平衡转化率随温度的变化 |
B.反应 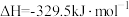 |
C.升高温度、减小压强均有利于提高 的平衡转化率 的平衡转化率 |
D.恒压、800K、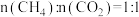 条件下,反应至 条件下,反应至 转化率达到X点的值,可通过改变 转化率达到X点的值,可通过改变 的量或使用高效催化剂等特定条件继续反应, 的量或使用高效催化剂等特定条件继续反应, 转化率能达到Y点的值 转化率能达到Y点的值 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列推论正确的是
A.C(s)+O2(g)=CO2(g) ΔH1;C(s)+ O2(g)=CO(g) ΔH2;则:ΔH1>ΔH2 O2(g)=CO(g) ΔH2;则:ΔH1>ΔH2 |
| B.已知4P(红磷,s)=P4(白磷,s)ΔH=+17kJ/mol,则白磷比红磷更稳定 |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4kJ·mol-1,则:含20gNaOH的稀溶液与足量稀盐酸完全反应,放出的热量为28.7kJ |
D.硫的燃烧热为315kJ/mol,表示硫的燃烧热的热化学方程式为:S(s)+ O2(g)=SO3(g) ΔH=-315kJ/mol O2(g)=SO3(g) ΔH=-315kJ/mol |
您最近一年使用:0次
【推荐3】碘与氢气反应的热化学方程式是
①I2(g) + H2(g) 2HI(g) △H=-9.48 kJ·mol-1
2HI(g) △H=-9.48 kJ·mol-1
②I2 (s) + H2 (g) 2HI(g) △H= +26.48 kJ·mol-1 下列说法正确的是
2HI(g) △H= +26.48 kJ·mol-1 下列说法正确的是
①I2(g) + H2(g)
 2HI(g) △H=-9.48 kJ·mol-1
2HI(g) △H=-9.48 kJ·mol-1②I2 (s) + H2 (g)
 2HI(g) △H= +26.48 kJ·mol-1 下列说法正确的是
2HI(g) △H= +26.48 kJ·mol-1 下列说法正确的是| A.①的产物比②的产物稳定 |
| B.I2(s) = I2(g) △H = +17.00 kJ·mol-1 |
| C.②的反应物总能量比①的反应物总能量低 |
| D.1mol I2(g)中通入 1 molH2 (g),发生反应时放热 9.48 kJ |
您最近一年使用:0次

 溶液反应:
溶液反应:
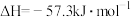
 的燃烧热为
的燃烧热为 ,则水分解的热化学方程式:
,则水分解的热化学方程式:

 的燃烧热为
的燃烧热为 ,则有
,则有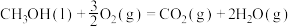

 时放出19.12kJ热量,则
时放出19.12kJ热量,则