1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
(1)元素 在元素周期表中的位置为第
在元素周期表中的位置为第_______ 周期第_______ 族。
(2)分别写出由第二周期元素与H元素形成的含10电子的一个分子和一个离子_______ 、_______ 。
(3)有以下几种粒子: 、
、 、
、 、
、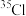 、
、 、
、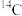 、
、 。其中含有
。其中含有_______ 种核素,互为同位素的有_______ 。由 、
、 、
、  与
与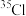 、
、  形成的氯化氢分子相对分子质量有
形成的氯化氢分子相对分子质量有_______ 种。
(4)以下说法正确的是_______。
(1)元素
 在元素周期表中的位置为第
在元素周期表中的位置为第(2)分别写出由第二周期元素与H元素形成的含10电子的一个分子和一个离子
(3)有以下几种粒子:
 、
、 、
、 、
、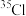 、
、 、
、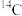 、
、 。其中含有
。其中含有 、
、 、
、  与
与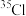 、
、  形成的氯化氢分子相对分子质量有
形成的氯化氢分子相对分子质量有(4)以下说法正确的是_______。
| A.碱金属单质和卤素单质随着核电荷数的增加,熔沸点依次升高,密度依次增大 |
| B.由于F、Cl、Br、I的非金属性依次减弱,可推出HF、HCl、HBr、HI的还原性及热稳定性依次减弱 |
| C.第85号元素砹At是核电荷数最大的卤素,其单质At2可能是一种有色固体,难溶于水易溶于有机溶剂 |
| D.在新制氯水中加入少量铁粉,发生2Fe+3Cl2=2FeCl3 |
更新时间:2024/02/02 11:11:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
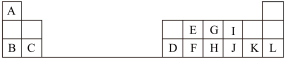
【推荐1】如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题。(除特别注明外,其他一律用化学式表示)___ 。
(2)元素E的最高价氧化物的电子式是____ 。
(3)某三原子分子有18个电子,该分子的空间构型为____ 。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序为____ 。
(5)H、J、K的最高价氧化物对应的水化物的酸性由强到弱的顺序为____ 。
(6)元素B的最高氧化物的水化物的电子式是___ ,其中含有的化学键为____ 。
(7)把C和D两元素的单质插入氢氧化钠溶液中形成原电池,则正极为____ (填元素名称),该原电池的负极电极反应式____ 。
(2)元素E的最高价氧化物的电子式是
(3)某三原子分子有18个电子,该分子的空间构型为
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序为
(5)H、J、K的最高价氧化物对应的水化物的酸性由强到弱的顺序为
(6)元素B的最高氧化物的水化物的电子式是
(7)把C和D两元素的单质插入氢氧化钠溶液中形成原电池,则正极为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:
(1)表中用于半导体材料的元素在周期表中的位置__________ 。
(2)③、④、⑧的原子半径最小是__________ (用元素符号回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是________ (用化学式回答)。
(4)②、③、④的气态氢化物,稳定性最强的是__________ (用结构式回答)。
(5)②和③按原子数1:2形成的化合物的电子式为____ ,该晶体气化的过程中克服的微粒间作用力为______ 。
(6)③和⑧形成的化合物属于__________ (填“离子化合物”或“共价化合物”),该晶体属于__________ 晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的离子方程式为:_____________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)③、④、⑧的原子半径最小是
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是
(4)②、③、④的气态氢化物,稳定性最强的是
(5)②和③按原子数1:2形成的化合物的电子式为
(6)③和⑧形成的化合物属于
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下面是元素周期表的一-部分,参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
(1)②⑦⑧的最高价含氧酸的酸任由强到弱的顺序是(填化学式)___ 。
(2)在①④⑤⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:___ 。
(3)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:__ 。
(4)②的简单气态氢化物与氧气组成燃料电池,用氢氧化钠做电解质溶液,写出其负极的电极反应式:___ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)②⑦⑧的最高价含氧酸的酸任由强到弱的顺序是(填化学式)
(2)在①④⑤⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(3)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(4)②的简单气态氢化物与氧气组成燃料电池,用氢氧化钠做电解质溶液,写出其负极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】我国科研团队成功研发“硅—石墨烯—锗晶体管”,代表着我国在这一尖端科技领域走在了世界的前列。
(1)碳元素在元素周期表中的位置是第___ 周期、第IVA族。
(2)硅元素最高价氧化物的化学式为___ 。
(3)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是___ (填字母)。
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
(1)碳元素在元素周期表中的位置是第
(2)硅元素最高价氧化物的化学式为
(3)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。如图是元素周期表的一部分,回答下列问题。
(1)周期表呈现的短周期元素中,次外层电子数等于其他电子层电子数之和的元素是_______ (写原子结构示意图);上述周期表呈现的元素中,金属性最强的元素在周期表中处于第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,写出Cl的最高价氧化物对应水化物的化学式_______ 。
(3)比较微粒半径大小:Al_______ F;
_______  (选填“>”或“<”)。
(选填“>”或“<”)。
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是_______ 。
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②原子数相同、价电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息见下表。
硼元素与Y、Q形成互为等电子体负离子: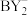 、
、 ,则m值为
,则m值为_______ 。
| B | C | N | O | F |
| Al | Si | P | S | Cl |
| Ga | Ge | As | Se | Br |
| In | Sn | Sb | Te | I |
(2)Sn的最高正价为
(3)比较微粒半径大小:Al

 (选填“>”或“<”)。
(选填“>”或“<”)。(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②原子数相同、价电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息见下表。
| Q | 与H可形成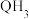 的10电子结构分子 的10电子结构分子 |
| Y | 带两个负电荷的负离子与氖原子结构相同 |
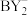 、
、 ,则m值为
,则m值为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为纪念 Dmitri Mendeleev(德米特里·门德列夫)发明的元素周期表诞生150周年。联合国大会室布2019年是“国际化学元素周期表年。以下是元素周期表的一部分
回答下列问题:
(1)在上表中用实线画出元素周期表的上边界_______ 。
(2)元素X原子核外有_______ 种能量不同的电子,元素Y原子最外层电子的轨道表示式为_______ ;26号元素Z的最外层有2个电子,其原结构示意可以表示为_______ 。
(3)比较元素的金属性:X_______ Y(填“>”或“<),从原子结构的角度说明理由:_______ 。
(4)下列曲线分别表示元素的某种性质(y)与核电荷数(Z)的关系:

①若“y表示元素周期表中第一列元素单质熔点,则对应曲线的编号是_______ 。
②若“y”表示同一短周期元素的原子半径,则对应曲线的编号是_______ 。
(5)氮(N)元素的气态氢化物的电子式为_______ ,假设NH 是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第_______ 族,其“单质”在常温常压下_______ (填“能”或“不能”)导电。
| X | Y | ||||||||||||||||
| Z | |||||||||||||||||
(1)在上表中用实线画出元素周期表的上边界
(2)元素X原子核外有
(3)比较元素的金属性:X
(4)下列曲线分别表示元素的某种性质(y)与核电荷数(Z)的关系:

①若“y表示元素周期表中第一列元素单质熔点,则对应曲线的编号是
②若“y”表示同一短周期元素的原子半径,则对应曲线的编号是
(5)氮(N)元素的气态氢化物的电子式为
 是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)自然界中存在的碘的稳定性核素是碘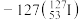 。某次核电站事故释放出的放射性物质中含有人工放射性核素碘
。某次核电站事故释放出的放射性物质中含有人工放射性核素碘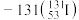 。碘
。碘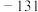 一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是
一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是______ (填序号)。
A. 和
和 原子核外的价电子排布不同
原子核外的价电子排布不同
B. 和
和 互为同位素
互为同位素
C. 原子的核外电子排布式中只有1个能级上未充满电子
原子的核外电子排布式中只有1个能级上未充满电子
D. 的中子数与质子数之差为74
的中子数与质子数之差为74
(2)有四种短周期元素,它们的结构、性质等信息如下表所示:
① 元素原子的核外电子排布式为
元素原子的核外电子排布式为______ 。
②离子半径:
______ (填“ ”或“
”或“ ”)
”) 。
。
③ 元素原子的核外电子排布图为
元素原子的核外电子排布图为______ ,其原子核外有______ 个未成对电子,能量最高的电子为______ 轨道上的电子,该轨道呈______ 形。
④写出 、
、 两元素的最高价氧化物对应的水化物反应的离子方程式:
两元素的最高价氧化物对应的水化物反应的离子方程式:______ 。
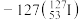 。某次核电站事故释放出的放射性物质中含有人工放射性核素碘
。某次核电站事故释放出的放射性物质中含有人工放射性核素碘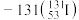 。碘
。碘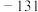 一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是
一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是A.
 和
和 原子核外的价电子排布不同
原子核外的价电子排布不同B.
 和
和 互为同位素
互为同位素C.
 原子的核外电子排布式中只有1个能级上未充满电子
原子的核外电子排布式中只有1个能级上未充满电子D.
 的中子数与质子数之差为74
的中子数与质子数之差为74(2)有四种短周期元素,它们的结构、性质等信息如下表所示:
| 元素 | 结构、性质等信息 |
| A | 是短周期元素中(除稀有气体外)第一电离能最小的元素,该元素单质的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时可用作制冷剂 |
| D | 原子核外电子共有17种不同的运动状态 |
①
 元素原子的核外电子排布式为
元素原子的核外电子排布式为②离子半径:

 ”或“
”或“ ”)
”) 。
。③
 元素原子的核外电子排布图为
元素原子的核外电子排布图为④写出
 、
、 两元素的最高价氧化物对应的水化物反应的离子方程式:
两元素的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答下列问题:
(1)写出漂白粉中有效成分的化学式___________ 。
(2)写出中子数为8的碳原子符号___________ 。
(3)镁离子的结构示意图___________ 。
(4)工业上用覆铜板制作印刷电路板,对应的离子方程式为___________ 。
(5)写出实验室制取氧气反应的化学方程式___________ 。
(1)写出漂白粉中有效成分的化学式
(2)写出中子数为8的碳原子符号
(3)镁离子的结构示意图
(4)工业上用覆铜板制作印刷电路板,对应的离子方程式为
(5)写出实验室制取氧气反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据要求回答下列相关问题:
(1)科学家进行科学探究时曾用48Ca轰击 Bk生成
Bk生成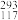 Uus和
Uus和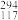 Uus下列说法错误的是
Uus下列说法错误的是___________ 。
A.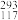 Uus和
Uus和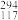 Uus互为同位素
Uus互为同位素
B.48Ca、 Bk表示两种核素
Bk表示两种核素
C.48Ca、 Bk、
Bk、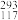 Uus和
Uus和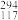 Uus属于四种元素
Uus属于四种元素
(2)下列关于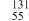 I和
I和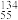 Cs和
Cs和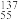 Cs的说法正确的是___________。
Cs的说法正确的是___________。
(3)碘原子核外电子层数有___________ 层,最外层电子数是___________ 。
(4)钚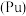 的质子数为94。
的质子数为94。
①用核素符号表示:钚-238、钚-239和钚-244分别是___________ 、___________ 、___________ 。
②钚 的中子数为
的中子数为___________ 。
(1)科学家进行科学探究时曾用48Ca轰击
 Bk生成
Bk生成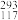 Uus和
Uus和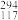 Uus下列说法错误的是
Uus下列说法错误的是A.
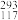 Uus和
Uus和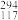 Uus互为同位素
Uus互为同位素B.48Ca、
 Bk表示两种核素
Bk表示两种核素C.48Ca、
 Bk、
Bk、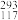 Uus和
Uus和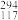 Uus属于四种元素
Uus属于四种元素(2)下列关于
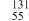 I和
I和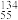 Cs和
Cs和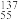 Cs的说法正确的是___________。
Cs的说法正确的是___________。A.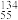 Cs和 Cs和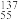 Cs的质子数相同,电子数不同 Cs的质子数相同,电子数不同 |
B.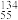 Cs和 Cs和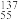 Cs的质量数相同,电子数不同 Cs的质量数相同,电子数不同 |
C.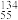 Cs和 Cs和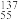 Cs的质子数相同,质量数不同 Cs的质子数相同,质量数不同 |
D.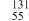 I和 I和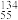 Cs和 Cs和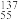 Cs的化学性质基本相同 Cs的化学性质基本相同 |
(4)钚
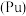 的质子数为94。
的质子数为94。①用核素符号表示:钚-238、钚-239和钚-244分别是
②钚
 的中子数为
的中子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请按要求填空:
(1)简单原子的原子结构如图:
①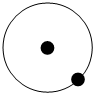 ②
② ③
③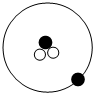
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
(2)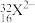 的质子数为
的质子数为___________ ,中子数为___________ ,电子数为___________ ,该元素在元素周期表中的位置是第___________ 周期___________ 族,该元素的最高价氧化物对应水化物的化学式是___________
(3)1828年,德国化学家维勒通过蒸发氰酸铵( )水溶液得到尿素[
)水溶液得到尿素[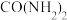 ]。
]。
①氰酸铵和尿素之间的关系是___________ (填标号)。
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为___________ 。
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为___________ 。
(1)简单原子的原子结构如图:
①
 ②
② ③
③
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
| A.①②③是三种不同的核素 | B.①②③具有相同的质量数 |
| C.①②③互为同位素 | D.①②③是三种化学性质不同的粒子 |
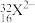 的质子数为
的质子数为(3)1828年,德国化学家维勒通过蒸发氰酸铵(
 )水溶液得到尿素[
)水溶液得到尿素[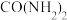 ]。
]。①氰酸铵和尿素之间的关系是
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为
您最近一年使用:0次

 、N
、N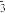 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等。已知N2H5+的形成过程类似于NH
等。已知N2H5+的形成过程类似于NH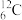 、
、 、
、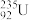 、
、 中共有
中共有

