“分类”的思想在化学学习及化学学科发展中起着重要作用。现有下列物质:
① 固体 ②熔融
固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤
③淀粉溶液 ④液态氯化氢 ⑤ 溶液 ⑥
溶液 ⑥ ⑦金属铜 ⑧
⑦金属铜 ⑧ ⑨酒精 ⑩
⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)②熔融 能导电,其电离方程式为
能导电,其电离方程式为___________ 。
(3)③淀粉溶液,⑤ 溶液二者如果混合,可采用
溶液二者如果混合,可采用___________ 方法分离。
(4)⑧ 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为___________ ,每当有 参与反应,转移电子数为
参与反应,转移电子数为___________ (设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
(5)已知⑨ (亚磷酸)与足量
(亚磷酸)与足量 溶液反应的化学方程式为
溶液反应的化学方程式为 ,
, 属于
属于___________ (填“正盐”或“酸式盐”)。
①
 固体 ②熔融
固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤
③淀粉溶液 ④液态氯化氢 ⑤ 溶液 ⑥
溶液 ⑥ ⑦金属铜 ⑧
⑦金属铜 ⑧ ⑨酒精 ⑩
⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是
(2)②熔融
 能导电,其电离方程式为
能导电,其电离方程式为(3)③淀粉溶液,⑤
 溶液二者如果混合,可采用
溶液二者如果混合,可采用(4)⑧
 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为 参与反应,转移电子数为
参与反应,转移电子数为 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。(5)已知⑨
 (亚磷酸)与足量
(亚磷酸)与足量 溶液反应的化学方程式为
溶液反应的化学方程式为 ,
, 属于
属于
更新时间:2024-02-18 08:31:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有甲、乙同学分别进行Fe(OH)3胶体的制备实验。
(1)甲同学:向一定量NaOH溶液中滴加少量FeCl3饱和溶液。甲同学的实验操作___ (填“能”或“不能”)制得Fe(OH)3胶体,其实验操作反应的离子方程式为___ 。
(2)乙同学:用蒸馏水和FeCl3饱和溶液制得了Fe(OH)3胶体。
①实验中所需仪器为___ (填选项字母)。
A.酒精灯 B.100 mL烧杯 C.玻璃棒 D.胶头滴管 E.三脚架 F.泥三角 G.石棉网
②实验步骤:向40 mL沸水中逐滴加入5~6滴FeCl3饱和溶液,___ ,停止加热。
③证明有Fe(OH)3胶体生成的实验操作是利用了胶体的___ 性质。
④制备Fe(OH)3胶体反应的化学方程式为___ 。
(1)甲同学:向一定量NaOH溶液中滴加少量FeCl3饱和溶液。甲同学的实验操作
(2)乙同学:用蒸馏水和FeCl3饱和溶液制得了Fe(OH)3胶体。
①实验中所需仪器为
A.酒精灯 B.100 mL烧杯 C.玻璃棒 D.胶头滴管 E.三脚架 F.泥三角 G.石棉网
②实验步骤:向40 mL沸水中逐滴加入5~6滴FeCl3饱和溶液,
③证明有Fe(OH)3胶体生成的实验操作是利用了胶体的
④制备Fe(OH)3胶体反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与人类生产、生活密切相关,按要求回答下列问题。
(1)现有以下六种物质:① 、②
、② 、③酒精、④
、③酒精、④ 、⑤稀硫酸。以上物质中属于电解质的是
、⑤稀硫酸。以上物质中属于电解质的是___________ (填序号,下同),可用___________ (填现象名称)区分 胶体和
胶体和 溶液。
溶液。
(2)钠的化合物中,可用作潜水艇中供氧剂的是___________ ,其与 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入___________(填字母)。
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是___________ (填化学式)。从物质类别来看,它属于___________ 类。
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备: (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目___________ 。
(1)现有以下六种物质:①
 、②
、② 、③酒精、④
、③酒精、④ 、⑤稀硫酸。以上物质中属于电解质的是
、⑤稀硫酸。以上物质中属于电解质的是 胶体和
胶体和 溶液。
溶液。(2)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(3)饮用水质量是关系人类健康的重要问题。暴雨过后,井水混浊无法饮用。为了能让井水变澄清,可向井水中投入___________(填字母)。
A. | B. | C. | D. |
(5)新型陶瓷氮化铝可用氧化铝高温还原法制备:
 (未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
(未配平),配平该化学反应方程式并用单线桥法标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)实验室中,制取Fe(OH)3胶体的操作是________ ,反应的化学方程式是_______ ,证明胶体已经制成的方法是_______ 。
(2)已知Fe(OH)3胶粒带正电荷。Al(OH)3胶粒也带正电荷,而H2SiO3胶粒带负电荷,则下列实验的现象分别是:
①Fe(OH)3胶体和Al(OH)3胶体混合:_______ ;
②Fe(OH)3胶体和H2SiO3胶体混合:_______ 。
(3)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体_______ (填“能”或“不能”)净水。
(1)实验室中,制取Fe(OH)3胶体的操作是
(2)已知Fe(OH)3胶粒带正电荷。Al(OH)3胶粒也带正电荷,而H2SiO3胶粒带负电荷,则下列实验的现象分别是:
①Fe(OH)3胶体和Al(OH)3胶体混合:
②Fe(OH)3胶体和H2SiO3胶体混合:
(3)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”,其具体流程如下,请回答下列问题:
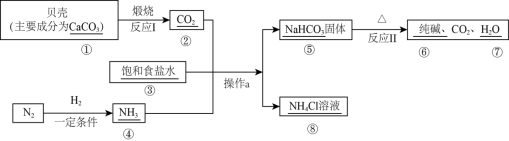
(1)图中涉及的①~⑧八种物质中,能导电的物质有_______ (填序号,下同),属于电解质的有_______ 。
(2)反应Ⅱ的化学方程式为_______ 。
(3)用离子方程式表示操作a制备NaHCO3的原理:_______ 。
(4)若向NaHCO3溶液中加入足量的Ba(OH)2,该反应的离子方程式为_______ 。
(5)若称取10.5g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02g。如果把剩余的固体全部加入到含0.2mol HCl的盐酸中充分反应。求反应后溶液中剩余的H+的物质的量_______ (忽略因水电离产生的H+)。

(1)图中涉及的①~⑧八种物质中,能导电的物质有
(2)反应Ⅱ的化学方程式为
(3)用离子方程式表示操作a制备NaHCO3的原理:
(4)若向NaHCO3溶液中加入足量的Ba(OH)2,该反应的离子方程式为
(5)若称取10.5g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02g。如果把剩余的固体全部加入到含0.2mol HCl的盐酸中充分反应。求反应后溶液中剩余的H+的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有下列八种物质:A.硫酸亚铁;B.稀硫酸;C.过氧化钠;D.水玻璃;E、烧碱溶液;F、浓氨水;G、氯化铵;H、硝酸钾。按要求回答问题:
⑴其中属于电解质的有________________________________ (用各物质的序号);
⑵物质的量浓度均为0.1mol·L-1的 D.F、G、H四种物质的溶液,按溶液pH由小到大排列的顺序为(将各物质的序号用“<”连接表示)_________________ ;
⑶在足量C中通入CO2气体,写出反应的化学方程式并标明电子得失情况;
____________________________________________________________________ ;
⑷将E逐滴滴入A的溶液中,请用简单的文字和离子方程式说明所发生的现象及该过程的化学原理____________________________________ ;
⑸将物质的量浓度均为0.02mol·L-1的 B.E等体积混合,所得溶液的pH=________ 。
⑴其中属于电解质的有
⑵物质的量浓度均为0.1mol·L-1的 D.F、G、H四种物质的溶液,按溶液pH由小到大排列的顺序为(将各物质的序号用“<”连接表示)
⑶在足量C中通入CO2气体,写出反应的化学方程式并标明电子得失情况;
⑷将E逐滴滴入A的溶液中,请用简单的文字和离子方程式说明所发生的现象及该过程的化学原理
⑸将物质的量浓度均为0.02mol·L-1的 B.E等体积混合,所得溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列十种物质(微粒):①氢氧化铁胶体 ②氯水 ③四氯化碳 ④CO2 ⑤CuSO4•5H2O ⑥漂白粉 ⑦0.2 mol·L-1 Ba(OH)2溶液 ⑧0.1 mol·L-1 Na2SO4溶液 ⑨溴水 ⑩KI。
(1)属于电解质的有________ 。
(2)将⑦⑧两溶液等体积混合,所得溶液中Na+的物质的量浓度约________ 。
(3)往往用________ 来证明①为胶体。
(4)实验室欲配制480 mL的⑧,下列说法正确的是________ 。
a.应选用480 mL容量瓶
b.需称量6.8 g Na2SO4固体
c.实验前,容量瓶需洗净并干燥
d.在其他操作正确情况下,定容时,俯视刻度线会导致所配溶液浓度偏大
(5)⑥在使用时需加水浸泡片刻,才能发挥更好的漂白效果,请用离子方程式表示相应的反应原理________ 。
(1)属于电解质的有
(2)将⑦⑧两溶液等体积混合,所得溶液中Na+的物质的量浓度约
(3)往往用
(4)实验室欲配制480 mL的⑧,下列说法正确的是
a.应选用480 mL容量瓶
b.需称量6.8 g Na2SO4固体
c.实验前,容量瓶需洗净并干燥
d.在其他操作正确情况下,定容时,俯视刻度线会导致所配溶液浓度偏大
(5)⑥在使用时需加水浸泡片刻,才能发挥更好的漂白效果,请用离子方程式表示相应的反应原理
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列物质: ①H2SO4 ②H2CO3 ③Ca(OH)2 ④NH3·H2O ⑤NaHCO3 ⑥BaSO4
(1)其中,属于强电解质的有___________ ,属于弱电解质的有___________ 。
(2)写出上述电解质的电离方程式___________ 。
(1)其中,属于强电解质的有
(2)写出上述电解质的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾、还强。工业上制取高铁酸钠的化学方程式是(未配平):Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O。
(1)高铁酸钠中,铁元素的化合价是____ ;上述制取铁酸钠的反应过程中,铁元素被____ (填“还原”或“氧化”)。
(2)高铁酸钠(Na2FeO4)是水处理过程中常用的新型净水剂,原因是Na2FeO4被还原为Fe3+,形成Fe(OH)3胶体,使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是____ nm,高铁酸钠在水溶液中的电离方程式是____ 。
(3)某同学配制了一瓶K2FeO4溶液,但标签丢失了,测定该瓶溶液物质的量浓度的实验步骤如下:
步骤1:准确量取VmL溶液加入锥形瓶中;
步骤2:在强碱溶液中,用过量CrO 与FeO
与FeO  反应生成Fe(OH)3和CrO
反应生成Fe(OH)3和CrO  ;
;
步骤3:加足量稀硫酸,使CrO 转化为Cr2O
转化为Cr2O ,CrO
,CrO 转化为Cr3+,Fe(OH)3转化为Fe3+;
转化为Cr3+,Fe(OH)3转化为Fe3+;
步骤4:加入二苯胺磺酸钠作指示剂,用cmol·L-1(NH4)2Fe(SO4)2溶液滴加至终点,消耗(NH4)2Fe(SO4)2标准溶液V1mL,此时Cr2O 恰好完全转化为Cr3+。
恰好完全转化为Cr3+。
①写出步骤四发生反应的离子方程式为____ 。
②原溶液中K2FeO4的物质的量浓度为____ (用含字母的代数式表示)。
Ⅱ.次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4:1,则氧化产物为____ (填化学式)。
②从分类来看,NaH2PO2属于____ 。
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法如下方程式,请配平方程式____ 。
P4+ Ba(OH)2+ H2O→ Ba(H2PO2)2+ PH3↑
(1)高铁酸钠中,铁元素的化合价是
(2)高铁酸钠(Na2FeO4)是水处理过程中常用的新型净水剂,原因是Na2FeO4被还原为Fe3+,形成Fe(OH)3胶体,使水中悬浮物沉聚,Fe(OH)3胶体微粒直径的范围是
(3)某同学配制了一瓶K2FeO4溶液,但标签丢失了,测定该瓶溶液物质的量浓度的实验步骤如下:
步骤1:准确量取VmL溶液加入锥形瓶中;
步骤2:在强碱溶液中,用过量CrO
 与FeO
与FeO  反应生成Fe(OH)3和CrO
反应生成Fe(OH)3和CrO  ;
;步骤3:加足量稀硫酸,使CrO
 转化为Cr2O
转化为Cr2O ,CrO
,CrO 转化为Cr3+,Fe(OH)3转化为Fe3+;
转化为Cr3+,Fe(OH)3转化为Fe3+;步骤4:加入二苯胺磺酸钠作指示剂,用cmol·L-1(NH4)2Fe(SO4)2溶液滴加至终点,消耗(NH4)2Fe(SO4)2标准溶液V1mL,此时Cr2O
 恰好完全转化为Cr3+。
恰好完全转化为Cr3+。①写出步骤四发生反应的离子方程式为
②原溶液中K2FeO4的物质的量浓度为
Ⅱ.次磷酸(H3PO2)是一种精细磷化工产品,是一元中强酸,具有较强还原性。
(4)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①利用H3PO2进行化学镀银,氧化剂(Ag+)与还原剂(H3PO2)的物质的量之比为4:1,则氧化产物为
②从分类来看,NaH2PO2属于
a.正盐 b.酸式盐 c.钠盐 d.氧化物
(5)H3PO2的工业制法如下方程式,请配平方程式
P4+ Ba(OH)2+ H2O→ Ba(H2PO2)2+ PH3↑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在下列物质中:①水 ②空气 ③铁 ④二氧化碳 ⑤H2SO4 ⑥NaOH溶液 ⑦氨水 ⑧氯化钠 ⑨蔗糖 ⑩NaHCO3
(1)属于电解质的是________________ 。
(2)属于混合物的是_________________ 。
(3)写出氨水中主要的电离方程式_______________ 。
(1)属于电解质的是
(2)属于混合物的是
(3)写出氨水中主要的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用2FeCl3+Cu=CuCl2+2X表示。
(1)上式中X的化学式为___________ 。
(2)在上述反应中,氧化剂为___________ ,氧化产物为___________ ,将两者的氧化性相比较,___________ 的氧化性更强。
(3)若有32 g铜被氧化,则参与反应的FeCl3的质量为___________ g。
(4)该反应的离子方程式为___________ 。
(5)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,___________ 的还原性最强;在Cu2+、Fe2+、Ag+中, ___________ 的氧化性最强。
(6)配平下列方程式:
①_____ _____NH3+___O2=____NO+______H2O
②____ __KMnO4+_____K2SO3+_______H2O=_____MnO2+_____K2SO4+_____KOH
(1)上式中X的化学式为
(2)在上述反应中,氧化剂为
(3)若有32 g铜被氧化,则参与反应的FeCl3的质量为
(4)该反应的离子方程式为
(5)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,
(6)配平下列方程式:
①
②
您最近一年使用:0次
【推荐2】Ⅰ.已知铜在常温下能被HNO3溶解。反应方程式为: 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目_______ 。
(2)若生成0.2mol的NO,则该过程中转移的电子是___________ mol。
(3)被还原的硝酸占参加反应硝酸的比例为___________ 。
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2,写出该化学方程式_________ 。
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
(2)若生成0.2mol的NO,则该过程中转移的电子是
(3)被还原的硝酸占参加反应硝酸的比例为
Ⅱ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2;已知该反应中H2O2只发生如下过程:H2O2→ O2,写出该化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式为_________ 。向反应后的溶液中通入少量CO2,反应的离子方程式为 _______________ 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为______________ (结果保留两位小数)。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___________________ ,反应中生成0.2mol HNO3,转移的电子数目为__________ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是__________ 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次



