N、Si、Al的化合物常用于制作新型无机非金属材料,如SiO2可用于制作光导纤维,AlN可用于制作耐高温材料,Al2O3可用于制作生物陶瓷。
(1)光导纤维应避免与碱性物质接触,推测SiO2属于______ 氧化物。
(2)用氯化铝和氮气经气相反应可以制得AlN。AlN中N元素的化合价为______ 。
(3)用铝土矿(主要成分为Al2O3)冶炼铝时,常用碱液浸取。写出Al2O3与NaOH溶液反应的化学方程式______ 。
(1)光导纤维应避免与碱性物质接触,推测SiO2属于
(2)用氯化铝和氮气经气相反应可以制得AlN。AlN中N元素的化合价为
(3)用铝土矿(主要成分为Al2O3)冶炼铝时,常用碱液浸取。写出Al2O3与NaOH溶液反应的化学方程式
23-24高一下·全国·课前预习 查看更多[1]
(已下线)5.3.2新型无机非金属材料
更新时间:2024-02-28 14:49:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学是一门实用性很强的科学,请根据题意填空:
(1)运输浓硫酸和浓硝酸常用铝罐车,试解释其原因:______ 。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是_____ (填化学式)。
(3)常用的打火机中充有丁烷, 的一氯代物有
的一氯代物有______ 种,分子式为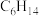 的长链(无支链)有机物的名称为
的长链(无支链)有机物的名称为____ 。
(4)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___ (填“放热”或“吸热”)的化学变化或物理变化。
(5)异戊二烯(结构简式为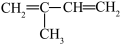 ),为无色易挥发液体,主要用于生产橡胶,还可用于制造农药、医药、香料及黏结剂等。在一定条件下存在以下转化关系:
),为无色易挥发液体,主要用于生产橡胶,还可用于制造农药、医药、香料及黏结剂等。在一定条件下存在以下转化关系:

①C→D的反应类型为______ ,反应条件为______ 。
②有机物E(分子式为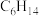 )是C的同系物,则有机物E的结构有
)是C的同系物,则有机物E的结构有_______ 种。
③在催化剂作用下,异戊二烯可发生加聚反应,写出加聚反应生成的产物可能的结构简式:_______ (任写一种)。
(1)运输浓硫酸和浓硝酸常用铝罐车,试解释其原因:
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)常用的打火机中充有丁烷,
 的一氯代物有
的一氯代物有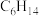 的长链(无支链)有机物的名称为
的长链(无支链)有机物的名称为(4)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(5)异戊二烯(结构简式为
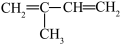 ),为无色易挥发液体,主要用于生产橡胶,还可用于制造农药、医药、香料及黏结剂等。在一定条件下存在以下转化关系:
),为无色易挥发液体,主要用于生产橡胶,还可用于制造农药、医药、香料及黏结剂等。在一定条件下存在以下转化关系:
①C→D的反应类型为
②有机物E(分子式为
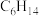 )是C的同系物,则有机物E的结构有
)是C的同系物,则有机物E的结构有③在催化剂作用下,异戊二烯可发生加聚反应,写出加聚反应生成的产物可能的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是______ (填化学式,下同),光导纤维的主要成分是_____ 。
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为_______ 。
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:_______ 。
(4)高纯度单晶硅可以按下列方法制备:SiO2 Si(粗)
Si(粗) SiHCl3
SiHCl3  Si(纯)
Si(纯)
写出步骤①的化学方程式:______ 。
步骤②的产物中, 大约占85%,还有
大约占85%,还有 、
、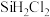 、
、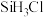 等,有关物质的沸点数据如下表,提纯
等,有关物质的沸点数据如下表,提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和________ 。
(1)可用于制作计算机芯片和太阳能电池的是
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
(4)高纯度单晶硅可以按下列方法制备:SiO2
 Si(粗)
Si(粗) SiHCl3
SiHCl3  Si(纯)
Si(纯)写出步骤①的化学方程式:
步骤②的产物中,
 大约占85%,还有
大约占85%,还有 、
、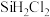 、
、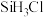 等,有关物质的沸点数据如下表,提纯
等,有关物质的沸点数据如下表,提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和物质 | Si |
|
|
|
| HCl |
|
沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学与人类生活、生产密切相关。请根据题意填空:
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填“SiO2”或“Na2SiO3”);
(2)衡量一个国家石油发展水平标志的物质是___________ (填“C2H4”或“C2H5OH”)
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成该反应的化学方程式:2CO+2NO 2CO2+___________。
2CO2+___________。___________
(4)常用作保护气的物质是___________ (填“N2”或“NH3”)
(5)检验某溶液中是否含SO ,先加盐酸,再加
,先加盐酸,再加___________ (填“BaCl2”或“NaCl”)溶液;
(6)要使AlCl3溶液中的Al3+全部沉淀,应加入过量的___________ (填“氨水”或“氢氧化钠溶液”)。
(1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(2)衡量一个国家石油发展水平标志的物质是
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成该反应的化学方程式:2CO+2NO
 2CO2+___________。
2CO2+___________。(4)常用作保护气的物质是
(5)检验某溶液中是否含SO
 ,先加盐酸,再加
,先加盐酸,再加(6)要使AlCl3溶液中的Al3+全部沉淀,应加入过量的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】W、X、Y、Z是原子序数依次增大的四种短周期元素。W的气态氢化物能使紫色石蕊溶液变蓝,W和X两种元素的最高价氧化物的水化物均能与Y的氢氧化物发生反应,W、X、Y、Z的最外层电子数之和为16。
(1) W单质的电子式是___________ 。
(2) 请用化学用语解释W的气态氢化物能使紫色石蕊溶液变蓝的原因:_________ 。
(3) Ga元素与Y在同一主族,Ga在元素周期表中的位置是_________ 。
(4) X的最高价氧化物的水化物与Y的氧化物发生反应的离子方程式是_________ 。
(5) WZ3易水解生成一种碱性气体和一种具有漂白性的物质。写出该水解反应的化学方程式_________ 。
(6) 已知Q与Z是位于相邻周期的同主族元素。某温度下,两种元素的气态单质与H2发生化合反应生成气态氢化物的平衡常数分别为KQ=5.6×107,KZ=9.7×1012。Q的元素符号是______ ,理 由 是_____________________ 。
(1) W单质的电子式是
(2) 请用化学用语解释W的气态氢化物能使紫色石蕊溶液变蓝的原因:
(3) Ga元素与Y在同一主族,Ga在元素周期表中的位置是
(4) X的最高价氧化物的水化物与Y的氧化物发生反应的离子方程式是
(5) WZ3易水解生成一种碱性气体和一种具有漂白性的物质。写出该水解反应的化学方程式
(6) 已知Q与Z是位于相邻周期的同主族元素。某温度下,两种元素的气态单质与H2发生化合反应生成气态氢化物的平衡常数分别为KQ=5.6×107,KZ=9.7×1012。Q的元素符号是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜、铬、锰均为过渡元素,其单质及化合物在工业、科技和生产中有着广泛的应用。
(1)Cu2S可用作制防污涂料、污水处理剂、催化剂等。
①灼烧Cu2S时,铜的焰色为___________ (填序号)。
A.黄色 B.洋红色 C.紫色 D.绿色
②用CuS、Cu2S处理酸性废水中的 时发生的反应如下:
时发生的反应如下:
I.CuS+ +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2O
II.Cu2S+ +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2O
当消耗的CuS、Cu2S的物质的量相同时,两者去除 的物质的量比为
的物质的量比为___________ 。
(2)Cr2O3可用于冶金,也可用作陶瓷、耐火材料、颜料业原料及有机合成催化剂等。
①Cr2O3与Al2O3性质类似,具有两性,写出Cr2O3与NaOH溶液反应的离子方程式:___________ 。
②用碳还原重铬酸钾可制备Cr2O3,同时生成一种可燃性有毒气体,当该反应中碳与重铬酸钾的化学计量数比为2:1时,氧化产物的化学式为___________ 。
(3)锰酸钾可用作皮革、纤维漂白剂以及杀菌剂、羊毛的媒染剂等。
①金属锰与熔融碱在氧化剂作用下生成锰酸钾,反应为2Mn+4KOH(熔融)+3O2=2K2MnO4+2H2O,若生成98.5 g K2MnO4,则消耗标准状况下O2的体积为___________ 。
②在KOH溶液的环境中高锰酸钾溶液与亚硫酸钠反应可以制得锰酸钾,写出该反应的离子方程式___________ 。
(1)Cu2S可用作制防污涂料、污水处理剂、催化剂等。
①灼烧Cu2S时,铜的焰色为
A.黄色 B.洋红色 C.紫色 D.绿色
②用CuS、Cu2S处理酸性废水中的
 时发生的反应如下:
时发生的反应如下:I.CuS+
 +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2OII.Cu2S+
 +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2O当消耗的CuS、Cu2S的物质的量相同时,两者去除
 的物质的量比为
的物质的量比为(2)Cr2O3可用于冶金,也可用作陶瓷、耐火材料、颜料业原料及有机合成催化剂等。
①Cr2O3与Al2O3性质类似,具有两性,写出Cr2O3与NaOH溶液反应的离子方程式:
②用碳还原重铬酸钾可制备Cr2O3,同时生成一种可燃性有毒气体,当该反应中碳与重铬酸钾的化学计量数比为2:1时,氧化产物的化学式为
(3)锰酸钾可用作皮革、纤维漂白剂以及杀菌剂、羊毛的媒染剂等。
①金属锰与熔融碱在氧化剂作用下生成锰酸钾,反应为2Mn+4KOH(熔融)+3O2=2K2MnO4+2H2O,若生成98.5 g K2MnO4,则消耗标准状况下O2的体积为
②在KOH溶液的环境中高锰酸钾溶液与亚硫酸钠反应可以制得锰酸钾,写出该反应的离子方程式
您最近一年使用:0次




