海水中盐的开发利用
(1)海水中溶解和悬浮着大量的_____ 和_____ 。海水中含量最多的_____ 两种元素,加上Cl、Na、Mg、S、Ca、K、Br、C、Sr、B、F元素,其总含量超过99%,其他元素为_____ 。虽然海水中元素的种类很多,总储量_____ ,但许多元素的富集程度却_____ 。
(2)海水制盐从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸等的化工原料。
①氯碱工业:电解饱和食盐水,可生产氢氧化钠、氢气和氯气。
化学反应方程式:_____ 。
②制钠和氯气:_____ 。
③制盐酸:_____ 。
④制漂白剂(84消毒液):_____ 。
⑤制纯碱:_____ ;_____ 。
(1)海水中溶解和悬浮着大量的
(2)海水制盐从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸等的化工原料。
①氯碱工业:电解饱和食盐水,可生产氢氧化钠、氢气和氯气。
化学反应方程式:
②制钠和氯气:
③制盐酸:
④制漂白剂(84消毒液):
⑤制纯碱:
23-24高一下·全国·课前预习 查看更多[1]
(已下线)8.1自然资源的开发利用
更新时间:2024-02-29 15:19:18
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式是__ (填“游离态”或“化合态”)。
②氯碱工业是重要的化学工业之一,写出该反应原理的离子方程式:__ 。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①铁和铝是两种常见的金属材料,在空气中铝比铁耐腐蚀的原因是__ 。
②新型陶瓷氮化铝可用氧化铝高温还原法制备,化学方程式如下,请配平该化学反应方程式并标出电子转移方向和数目。_________
Al2O3+C+N2 AlN+CO
AlN+CO
(3)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。
①写出二氧化硫与足量NaOH溶液反应的离子方程式:__ 。
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强。写出这一过程的化学方程式:__ 。
(1)海水中蕴含的元素有80多种。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式是
②氯碱工业是重要的化学工业之一,写出该反应原理的离子方程式:
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①铁和铝是两种常见的金属材料,在空气中铝比铁耐腐蚀的原因是
②新型陶瓷氮化铝可用氧化铝高温还原法制备,化学方程式如下,请配平该化学反应方程式并标出电子转移方向和数目。
Al2O3+C+N2
 AlN+CO
AlN+CO(3)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。
①写出二氧化硫与足量NaOH溶液反应的离子方程式:
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强。写出这一过程的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】海洋约占地球表面积的_______ ,海水约占地球上总水量的_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是___ (填序号)。
A.Cl2 B.淡水 C.烧碱 D.粗盐
(2)如图是从海水中提取镁的简单流程。___ ,Mg(OH)2转化为MgCl2的离子方程式是___ 。
②由无水MgCl2制取Mg的化学方程式是___ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
干海带 海带灰
海带灰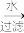 滤液
滤液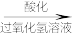
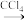
 I2
I2
①灼烧海带时所用的主要仪器名称是___ 。
②向酸化的滤液中加H2O2溶液,写出该反应的离子方程式:___ 。
③反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈___ 。
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.粗盐
(2)如图是从海水中提取镁的简单流程。

②由无水MgCl2制取Mg的化学方程式是
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
干海带
 海带灰
海带灰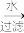 滤液
滤液
 I2
I2①灼烧海带时所用的主要仪器名称是
②向酸化的滤液中加H2O2溶液,写出该反应的离子方程式:
③反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】从海水中可提取多种化工原料,下图是工业上对海水的几项综合利用的示意图。试回答下列问题:
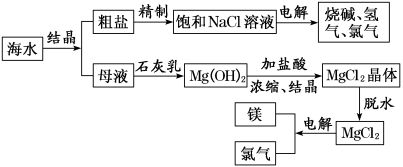
(1)写出用海滩上的贝壳制Ca(OH)2的化学方程式:_______ ;_______ 。
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?_______ 。
(3)电解无水MgCl2可制取镁和氯气,其中副产品氯气和粉末状熟石灰可制得漂白粉,制漂白粉的化学方程式为_______ 。
(4)用海滩上的贝壳制Ca(OH)2,而不从异地山中开凿石灰石制取,主要考虑到_______ 问题。
(5)从经济效益角度看,该化工厂厂址应选在_______ 。

(1)写出用海滩上的贝壳制Ca(OH)2的化学方程式:
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?
(3)电解无水MgCl2可制取镁和氯气,其中副产品氯气和粉末状熟石灰可制得漂白粉,制漂白粉的化学方程式为
(4)用海滩上的贝壳制Ca(OH)2,而不从异地山中开凿石灰石制取,主要考虑到
(5)从经济效益角度看,该化工厂厂址应选在
您最近一年使用:0次

 ;
;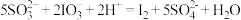 ;
; 溶液
溶液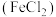 ,方法:
,方法: 酸性溶液
酸性溶液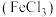 ,方法:
,方法: 和
和 :
: 溶液
溶液 溶液
溶液 溶液
溶液


