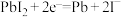微生物燃料电池能在较低的有机负荷下将化学能转化为电能,可用于有机污染的生物修复,其反应原理如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是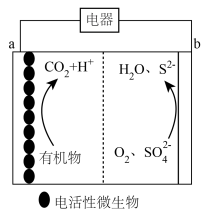
| A.a极是电池负极 |
B.电子从 极经电解质溶液流向 极经电解质溶液流向 极 极 |
C. 向 向 极移动 极移动 |
D.若“有机物”是甲烷,则a极每产生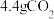 ,转移电子数为 ,转移电子数为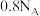 |
更新时间:2024-02-24 08:56:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】通过膜电池可除去废水中的乙酸钠和对氯苯酚(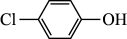 ),其原理如图所示,下列说法错误的是
),其原理如图所示,下列说法错误的是

 ),其原理如图所示,下列说法错误的是
),其原理如图所示,下列说法错误的是
| A.环境温度对该电池会有影响 |
| B.该电池工作时,外电路中的电流由b极流向a极 |
C. 、 、 均能与氯化铁溶液发生显色反应 均能与氯化铁溶液发生显色反应 |
D.每消耗 ,电路中通过的电子数为8NA ,电路中通过的电子数为8NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是
| A.该电池Zn为负极,ZnO为正极,MnO2为催化剂 |
| B.导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| C.该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH- |
| D.电池工作时正极发生氧化反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】对于反应Zn+H2SO4=ZnSO4+H2↑,1 mol Zn反应时放出Q kJ热量。下列叙述不正确的是( )
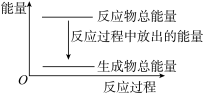

| A.反应过程中的能量关系可用如图表示 | B.滴入少许CuSO4溶液后反应速率减小 |
| C.若将该反应设计成原电池,则锌为负极 | D.理论上当转移4 mol电子时放出2QkJ热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
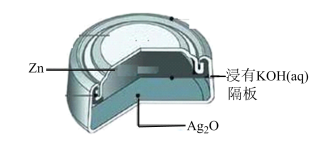
【推荐2】电子表中电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+H2O+Zn=Zn(OH)2+2Ag。下列说法不正确的是
| A.锌是负极,氧化银是正极 |
| B.正极反应式为:Ag2O+2e-+H2O=2Ag+2OH- |
| C.溶液中OH-向负极移动,K+向正极移动 |
| D.随着电极反应的不断进行,电解质溶液的pH会减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一种微生物燃料电池如图所示,下列关于该电池说法正确的是
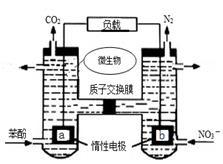

| A.a电极发生还原反应,做原电池的正极 |
| B.b电极反应式为:2NO3-+10e-+12H+=N2↑+6H2O |
| C.H+由右室通过质子交换膜进入左室 |
| D.标准状况下,电路中产生6moLCO2同时产生22.4L的N2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学电源在日常生活和高科技领域中都有广泛应用。
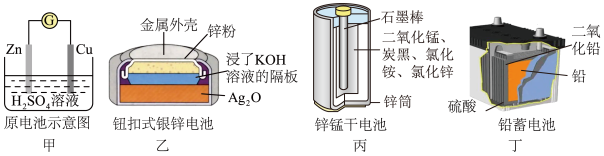
其中图乙、丙、丁三个电池的总电极反应方程式如下:
图乙:Zn+Ag2O+H2O═Zn(OH)2+2Ag
图丙:Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+MnO(OH)
图丁:PbO2+Pb+2H2SO4═2PbSO4+2H2O
下列说法不正确的是( )

其中图乙、丙、丁三个电池的总电极反应方程式如下:
图乙:Zn+Ag2O+H2O═Zn(OH)2+2Ag
图丙:Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+MnO(OH)
图丁:PbO2+Pb+2H2SO4═2PbSO4+2H2O
下列说法不正确的是( )
| A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加 |
| B.乙:正极的电极反应式为Ag2O+2e﹣+H2O═2Ag+2OH﹣ |
| C.丙:锌筒作负极,发生氧化反应,锌筒会变薄 |
| D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降 |
您最近一年使用:0次

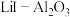 固体为电解质传递离子,其基本结构示意图如图,电池总反应可表示为
固体为电解质传递离子,其基本结构示意图如图,电池总反应可表示为 。下列说法正确的是
。下列说法正确的是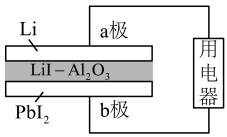
 由a极通过固体电解质传递到b极
由a极通过固体电解质传递到b极