现有以下物质:
①NaOH溶液 ②液氨 ③BaCO3固体 ④NaHSO4溶液 ⑤Fe(OH)3胶体
⑥铜 ⑦CO2 ⑧醋酸(CH3COOH) ⑨饱和NaHCO3溶液
(1)上述物质中属于电解质的是________ (英字号,下同),能导电的是________ 。
(2)写出④和⑨反应的离子方程式________ 。
(3)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为________ 。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是________ 。
①NaOH溶液 ②液氨 ③BaCO3固体 ④NaHSO4溶液 ⑤Fe(OH)3胶体
⑥铜 ⑦CO2 ⑧醋酸(CH3COOH) ⑨饱和NaHCO3溶液
(1)上述物质中属于电解质的是
(2)写出④和⑨反应的离子方程式
(3)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
更新时间:2024-03-19 14:15:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化
(1)写出碳酸氢钠在水中的电离方程式:________ ;
(2)除去FeSO4溶液中的少量CuSO4时发生的离子方程式:________ ;
(3)已知硼酸(H3BO3)的电离方程式可表示为:H3BO3+H2O B(OH)
B(OH) +H+,请写出硼酸与NaOH反应的离子方程式:
+H+,请写出硼酸与NaOH反应的离子方程式:________ ;
Ⅱ.过滤、结晶、蒸馏、萃取分液、渗析等是物质分离提纯的常用实验操作
(4)除去蛋白质溶液里混有的(NH4)2SO4的实验操作是________ ;
(5)已知硫酸镁和硼酸的溶解度曲线如图,为了分别获取硫酸镁晶体和硼酸晶体,做如下操作:

ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.将浓缩液加入到高压釜(确保水在200℃不沸腾)中,升温至200℃结晶,________ 分离出硫酸镁,分离后再将母液降温结晶,分离得到硼酸晶体。
Ⅲ.物质的量是联系宏观和微观的桥梁:
(6)一定质量的CH4中含有的原子总数为N,若阿伏伽德罗常数用NA表示,则CH4的物质的量是________ mol
(7)由CO、CO2两气体组成的混合气体12.8g,标准状况下的体积为8.96L。则CO、CO2的物质的量之比为________ 。
(1)写出碳酸氢钠在水中的电离方程式:
(2)除去FeSO4溶液中的少量CuSO4时发生的离子方程式:
(3)已知硼酸(H3BO3)的电离方程式可表示为:H3BO3+H2O
 B(OH)
B(OH) +H+,请写出硼酸与NaOH反应的离子方程式:
+H+,请写出硼酸与NaOH反应的离子方程式:Ⅱ.过滤、结晶、蒸馏、萃取分液、渗析等是物质分离提纯的常用实验操作
(4)除去蛋白质溶液里混有的(NH4)2SO4的实验操作是
(5)已知硫酸镁和硼酸的溶解度曲线如图,为了分别获取硫酸镁晶体和硼酸晶体,做如下操作:

ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.将浓缩液加入到高压釜(确保水在200℃不沸腾)中,升温至200℃结晶,
Ⅲ.物质的量是联系宏观和微观的桥梁:
(6)一定质量的CH4中含有的原子总数为N,若阿伏伽德罗常数用NA表示,则CH4的物质的量是
(7)由CO、CO2两气体组成的混合气体12.8g,标准状况下的体积为8.96L。则CO、CO2的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】随着科学技术的发展,许多新材料、新技术广泛应用于各个领域。
I.图1是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
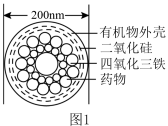
(1)“纳米药物分子车”分散于水中所得的分散系__________ (填“属于”或“不属于”)胶体。
(2)“纳米药物分子车”的外壳属于有机物。①酒精②蔗糖③冰醋酸中这三种有机物中,属于电解质的是__________ (填序号)。
(3)从元素组成的角度分析, 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的__________ 。
Ⅱ.无土栽培技术的成功推广,营养液的准确配制是重要环节。某 营养液中含有
营养液中含有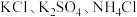 三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中
三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中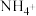 的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
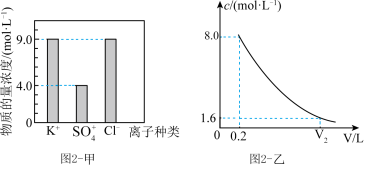
(4)该营养液中 的物质的量浓度为
的物质的量浓度为__________ 。
(5)写出一种与 含相同电子数的分子的化学式
含相同电子数的分子的化学式______________ ;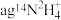 含有的中子的物质的量为
含有的中子的物质的量为__________ 。
Ⅲ.近年来,我国储氢材料的研制取得重大发展。其中电弧法合成储氢碳纳米管时,常伴有大量碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,其反应原理如下:
_____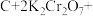 _____
_____ (稀)
(稀) ____
____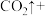 _____
_____ _____
_____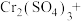 _____
_____
回答下列问题:
(6)完成上述反应的配平_________ 。
(7)某学生欲配制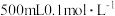 的稀硫酸,用量筒量取需要的浓硫酸,则需量取
的稀硫酸,用量筒量取需要的浓硫酸,则需量取 的浓硫酸
的浓硫酸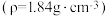 的体积为
的体积为__________ 。
(8)标准状况下,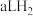 和
和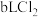 的混合气体,经强光充分照射后,所得气体恰好使含
的混合气体,经强光充分照射后,所得气体恰好使含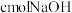 的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是____________________ 。
I.图1是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:

(1)“纳米药物分子车”分散于水中所得的分散系
(2)“纳米药物分子车”的外壳属于有机物。①酒精②蔗糖③冰醋酸中这三种有机物中,属于电解质的是
(3)从元素组成的角度分析,
 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的Ⅱ.无土栽培技术的成功推广,营养液的准确配制是重要环节。某
 营养液中含有
营养液中含有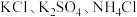 三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中
三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中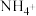 的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
(4)该营养液中
 的物质的量浓度为
的物质的量浓度为(5)写出一种与
 含相同电子数的分子的化学式
含相同电子数的分子的化学式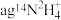 含有的中子的物质的量为
含有的中子的物质的量为Ⅲ.近年来,我国储氢材料的研制取得重大发展。其中电弧法合成储氢碳纳米管时,常伴有大量碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,其反应原理如下:
_____
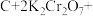 _____
_____ (稀)
(稀) ____
____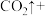 _____
_____ _____
_____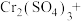 _____
_____
回答下列问题:
(6)完成上述反应的配平
(7)某学生欲配制
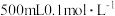 的稀硫酸,用量筒量取需要的浓硫酸,则需量取
的稀硫酸,用量筒量取需要的浓硫酸,则需量取 的浓硫酸
的浓硫酸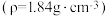 的体积为
的体积为(8)标准状况下,
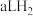 和
和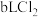 的混合气体,经强光充分照射后,所得气体恰好使含
的混合气体,经强光充分照射后,所得气体恰好使含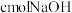 的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】人们根据分散质粒子的大小,把分散系分为溶液、胶体和浊液等。
(1)淀粉溶液是一种胶体,它区别于其它分散系的本质特征是_______ 。
(2)现有淀粉和 的混合液,装在半透膜袋中,浸泡在蒸馏水中(如图)。
的混合液,装在半透膜袋中,浸泡在蒸馏水中(如图)。

一段时间后,从烧杯中移走半透膜,然后取烧杯中的液体于甲、乙两支试管中,向甲试管中滴加碘水,溶液是否变为蓝色_______ (填“是”或“否”);向乙试管中滴加氯化钡溶液,现象是_______ 。由以上实验可得出的结论是_______ 。
(3)把装有橘红色的硫化锑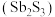 胶体的U型管,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫
胶体的U型管,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫_______ ,解释阳极附近橘红色加深的原因_______ 。
(1)淀粉溶液是一种胶体,它区别于其它分散系的本质特征是
(2)现有淀粉和
 的混合液,装在半透膜袋中,浸泡在蒸馏水中(如图)。
的混合液,装在半透膜袋中,浸泡在蒸馏水中(如图)。
一段时间后,从烧杯中移走半透膜,然后取烧杯中的液体于甲、乙两支试管中,向甲试管中滴加碘水,溶液是否变为蓝色
(3)把装有橘红色的硫化锑
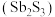 胶体的U型管,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫
胶体的U型管,插入电极后通直流电,发现阳极附近橘红色加深,这种现象叫
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列物质中,属于电解质的是___________ (填序号,下同),属于非电解质的是___________ ,属于强电解质的是___________ ,属于弱电解质的是___________ ,既不是电解质也不是非电解质的是___________ 。
①H2SO4;②氯气;③BaSO4;④乙醇;⑤铜;⑥H2CO3;⑦氯化氢;⑧CH3COOH; ⑨NH3;⑩CO2;⑪NaHCO3
①H2SO4;②氯气;③BaSO4;④乙醇;⑤铜;⑥H2CO3;⑦氯化氢;⑧CH3COOH; ⑨NH3;⑩CO2;⑪NaHCO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“咯酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有①吸收性抗酸药,如NaHCO3等。②非吸收性抗酸药,如CaCO3、MgO、Al(OH)3等。
(1)上述所举抗酸药中有___________ 个是电解质。
(2)CaCO3作抗酸药时发生反应的离子方程式为___________ 。
(3)___________ (填“可以”或“不可以”)服用BaCO3来治疗胃酸过多,理由是___________ 。
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为___________ 。
(1)上述所举抗酸药中有
(2)CaCO3作抗酸药时发生反应的离子方程式为
(3)
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列小题。
(1)以下为中学化学中常见的几种物质:①无水酒精,② 晶体,③铁丝,④氨水,⑤液态
晶体,③铁丝,④氨水,⑤液态 ,⑥
,⑥ 溶液,⑦
溶液,⑦ ,⑧熔融的
,⑧熔融的 ,⑨空气,⑩
,⑨空气,⑩ 固体。属于电解质的是
固体。属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)按要求写出下列方程式:
① 在水溶液中的电离方程式:
在水溶液中的电离方程式:___________ ;
② 通入足量澄清石灰水中发生反应的离子方程式
通入足量澄清石灰水中发生反应的离子方程式___________ ;
③向 溶液中滴加过量
溶液中滴加过量 溶液后发生反应的离子方程式:
溶液后发生反应的离子方程式:___________ 。
(1)以下为中学化学中常见的几种物质:①无水酒精,②
 晶体,③铁丝,④氨水,⑤液态
晶体,③铁丝,④氨水,⑤液态 ,⑥
,⑥ 溶液,⑦
溶液,⑦ ,⑧熔融的
,⑧熔融的 ,⑨空气,⑩
,⑨空气,⑩ 固体。属于电解质的是
固体。属于电解质的是(2)按要求写出下列方程式:
①
 在水溶液中的电离方程式:
在水溶液中的电离方程式:②
 通入足量澄清石灰水中发生反应的离子方程式
通入足量澄清石灰水中发生反应的离子方程式③向
 溶液中滴加过量
溶液中滴加过量 溶液后发生反应的离子方程式:
溶液后发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
Ⅰ.现有以下物质:①氮气 ②CO2 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的KNO3 ⑨NaHSO4溶液,请回答下列问题:
(1)以上物质中能导电的是_______ (填序号,下同)。
(2)以上物质中属于电解质的是_______ 。
(3)以上物质中属于非电解质的是_______ 。
Ⅱ.有下列几种物质:Na2SO3、Na2SO4、KIO3、K2SO4 、I2 等组成一个氧化还原反应。
(4)将化学方程式补全并进行配平_______ :
_____KIO3 + _____Na2SO3 + __________ —— _____Na2SO4 + _____K2SO4 + _____I2 + _____H2O
(5)在该反应中,还原剂是_______ (填化学式,下同),还原产物是_______ 。
Ⅲ.是“84”消毒液的有效成分,请回答下列问题:
(6)NaClO中Cl元素的化合价是_______ 价。
(7)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液而发生氯气中毒事件。用离子方程式表示原因:_______ 。
Ⅰ.现有以下物质:①氮气 ②CO2 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的KNO3 ⑨NaHSO4溶液,请回答下列问题:
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
Ⅱ.有下列几种物质:Na2SO3、Na2SO4、KIO3、K2SO4 、I2 等组成一个氧化还原反应。
(4)将化学方程式补全并进行配平
_____KIO3 + _____Na2SO3 + __________ —— _____Na2SO4 + _____K2SO4 + _____I2 + _____H2O
(5)在该反应中,还原剂是
Ⅲ.是“84”消毒液的有效成分,请回答下列问题:
(6)NaClO中Cl元素的化合价是
(7)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液而发生氯气中毒事件。用离子方程式表示原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可替代的。现有以下几种物质:①水银②熔融的烧碱③干冰④澄清石灰水⑤蔗糖⑥氢氧化钡⑦冰醋酸(纯净的醋酸),请按要求作答。
(1)上述物质中能导电的是_____ (填序号,下同),属于电解质的是_____ ,属于碱的是_____ 。
(2)⑥在水中的电离方程式为_____
(3)将过量③加入到④中反应的离子方程式为_____ 。
(4)向⑥的溶液中逐滴加入 溶液至中性,反应的离子方程式为
溶液至中性,反应的离子方程式为_____
(1)上述物质中能导电的是
(2)⑥在水中的电离方程式为
(3)将过量③加入到④中反应的离子方程式为
(4)向⑥的溶液中逐滴加入
 溶液至中性,反应的离子方程式为
溶液至中性,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】重铬酸钾( )具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识,回答下列问题:
)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识,回答下列问题:
(1) 中Cr的化合价为
中Cr的化合价为_______ 价,属于_______ (填“酸”、“碱”或“盐”)。
(2)当铬酸洗液变绿[溶液中 转化成
转化成 ]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入
]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入 粉末氧化,滤去
粉末氧化,滤去 后可实现铬酸洗液的再生,其中加入
后可实现铬酸洗液的再生,其中加入 粉末氧化时发生反应的离子方程式为
粉末氧化时发生反应的离子方程式为_______ (用单线桥法标明电子转移的方向和数目);滤去 时,可采用过滤操作,过滤需要用到的玻璃仪器有
时,可采用过滤操作,过滤需要用到的玻璃仪器有_______ 。
(3)当铬酸洗液变黑失效时,可在酸性条件下加入铁屑将残留的 转化成
转化成 ,铁屑自身转化成
,铁屑自身转化成 ,再用石灰石将铬元素转化成
,再用石灰石将铬元素转化成 沉淀,其中铁屑将
沉淀,其中铁屑将 转化成
转化成 的离子方程式为
的离子方程式为_______ ;若黑色铬酸洗液中 的浓度为
的浓度为 ,则处理
,则处理 该黑色铬酸洗液时,所需的铁屑的质量为
该黑色铬酸洗液时,所需的铁屑的质量为_______  。
。
(4)酸性 溶液还可以用来测定铁矿石中铁(以+2价形式存在,铁的含量为
溶液还可以用来测定铁矿石中铁(以+2价形式存在,铁的含量为 )的含量,称取铁矿石试样(含
)的含量,称取铁矿石试样(含 ,设其他物质不与
,设其他物质不与 反应)
反应) ,若加入的酸性
,若加入的酸性 溶液的体积为xmL,则
溶液的体积为xmL,则 的浓度为
的浓度为_______  。
。
 )具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识,回答下列问题:
)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识,回答下列问题:(1)
 中Cr的化合价为
中Cr的化合价为(2)当铬酸洗液变绿[溶液中
 转化成
转化成 ]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入
]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入 粉末氧化,滤去
粉末氧化,滤去 后可实现铬酸洗液的再生,其中加入
后可实现铬酸洗液的再生,其中加入 粉末氧化时发生反应的离子方程式为
粉末氧化时发生反应的离子方程式为 时,可采用过滤操作,过滤需要用到的玻璃仪器有
时,可采用过滤操作,过滤需要用到的玻璃仪器有(3)当铬酸洗液变黑失效时,可在酸性条件下加入铁屑将残留的
 转化成
转化成 ,铁屑自身转化成
,铁屑自身转化成 ,再用石灰石将铬元素转化成
,再用石灰石将铬元素转化成 沉淀,其中铁屑将
沉淀,其中铁屑将 转化成
转化成 的离子方程式为
的离子方程式为 的浓度为
的浓度为 ,则处理
,则处理 该黑色铬酸洗液时,所需的铁屑的质量为
该黑色铬酸洗液时,所需的铁屑的质量为 。
。(4)酸性
 溶液还可以用来测定铁矿石中铁(以+2价形式存在,铁的含量为
溶液还可以用来测定铁矿石中铁(以+2价形式存在,铁的含量为 )的含量,称取铁矿石试样(含
)的含量,称取铁矿石试样(含 ,设其他物质不与
,设其他物质不与 反应)
反应) ,若加入的酸性
,若加入的酸性 溶液的体积为xmL,则
溶液的体积为xmL,则 的浓度为
的浓度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下面是有关钠及其化合物性质的探究实验。
(1)金属钠的密度比水___ (填“大”或“小”),实验室中金属钠通常保存在___ 中,取一小块金属钠投入水中,写出该反应的离子方程式___ 。
(2)取Na2O2固体放入试管中,加适量水,有气体放出,写出该反应的离子方程式___ ,继续向上述试管中滴入1〜2滴酚酞溶液,可观察到的现象是___ 。
(1)金属钠的密度比水
(2)取Na2O2固体放入试管中,加适量水,有气体放出,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)BiCl3的水解产物中有BiOCl生成。
①写出BiCl3水解反应的方程式:_________________________ 。
②医药上将BiOCl称为次氯酸铋,该名称____________ (填“正确”或“不正确”)。
③如何配制BiCl3溶液?_________________________________ 。
(2)将pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
①若生成的盐中只有一种离子水解,该离子水解的离子方程式为_____________________ 。
②简述该混合液呈碱性的原因______________________ 。
①写出BiCl3水解反应的方程式:
②医药上将BiOCl称为次氯酸铋,该名称
③如何配制BiCl3溶液?
(2)将pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
①若生成的盐中只有一种离子水解,该离子水解的离子方程式为
②简述该混合液呈碱性的原因
您最近一年使用:0次



