根据原电池的工作原理分析判断(填写“正极”或“负极”)。
(1)由组成原电池的电极材料判断。一般是活动性较强的金属为_______ 极,活动性较弱的金属或能导电的非金属为_______ 极。
(2)根据电流方向或电子流动方向判断。电流由_______ 极流向_______ 极;电子由_______ 极流向_______ 极。
(3)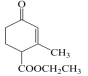 中含有的官能团名称是
中含有的官能团名称是_______ ,_______ ,_______ 。
(1)由组成原电池的电极材料判断。一般是活动性较强的金属为
(2)根据电流方向或电子流动方向判断。电流由
(3)
 中含有的官能团名称是
中含有的官能团名称是
更新时间:2024-03-22 07:51:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】空军通信卫星电源是以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2为原料的燃料电池,电极材料均采用Pt,其工作原理如图所示。回答下列问题:

(1)该燃料电池能量转化的主要形式是__ ,外电路中电子的流动方向为___ (填标号)。
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为___ 。
(3)图中离子交换膜为___ (填“阴”或“阳”)离子交换膜,电池工作时,Na+往___ (填“电极a”或“电极b”)方向迁移。
(4)每生成0.01molOH-,转移的电子数为__ NA,需要H2O2溶液(质量分数2%)的质量为___ g。
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为___ 。

(1)该燃料电池能量转化的主要形式是
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为
(3)图中离子交换膜为
(4)每生成0.01molOH-,转移的电子数为
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一种熔融碳酸盐燃料电池的原理示意图如下。
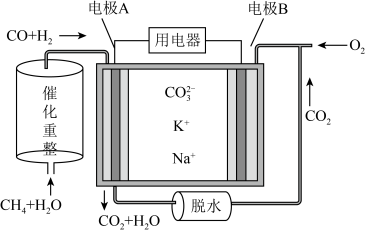
请回答下列有关该电池的问题:
(1)反应 ,每消耗1mol
,每消耗1mol  理论上转移的电子数目为
理论上转移的电子数目为_______ 。
(2)电池工作时, 向电极
向电极_______ (填“A”或“B”)移动。
(3)电极A上 参与的电极反应为
参与的电极反应为_______ 。
(4)电极B上发生的电极反应为_______ 。

请回答下列有关该电池的问题:
(1)反应
 ,每消耗1mol
,每消耗1mol  理论上转移的电子数目为
理论上转移的电子数目为(2)电池工作时,
 向电极
向电极(3)电极A上
 参与的电极反应为
参与的电极反应为(4)电极B上发生的电极反应为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流表。原电池工作时电子是从_____ 到______ (填锌片或银片),锌片电极上发生的是_______________ 反应(“氧化”或“还原”)。电极反应式为_________________________________ ,锌片上观察到的现象为___________
(2)银片上发生的是____________ 反应(“氧化”或“还原”),电极反应式是__________ ,银片上观察到的现象是______________________ 溶液中的C(H+)____________ (填“增大”或“减小”)。
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为________ L(标准状况);导线中通过的电子数为______ 。
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以__________ (写名称)为电解质溶液,铁为______ 极,电极反应式为_______ ,
(2)在该原电池中,选__________ (写名称)作正极,电极反应式是__________________________
(3)画出装置图,标出正、负极材料及电解质溶液名称____________________ 。
(2)银片上发生的是
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以
(2)在该原电池中,选
(3)画出装置图,标出正、负极材料及电解质溶液名称
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
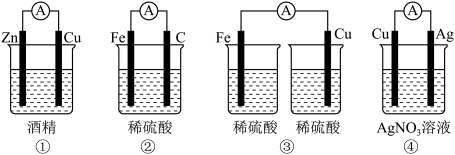
(1)如图装置中属于原电池的是____ (填序号)。
(2)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图1所示。
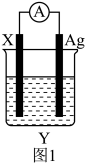
①电极X的材料是____ 。
②X电极的电极反应式为____ ;Ag电极上发生的是___ (填“氧化”或“还原”)反应。
③当有2.8 g铁溶解时,Ag电极增重____ g。
(3)以甲烷为燃料的新型电池得到广泛的研究,如图2是目前研究较多的一类燃料电池的工作原理示意图。
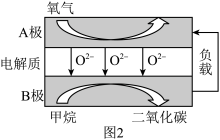
①A极为电池极____ (填“正”或“负”)。
②B极的电极反应式为____ ;若消耗标准状况下的CH411.2 L,则电路中转移____ mol电子。
(1)如图装置中属于原电池的是

(2)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图1所示。

①电极X的材料是
②X电极的电极反应式为
③当有2.8 g铁溶解时,Ag电极增重
(3)以甲烷为燃料的新型电池得到广泛的研究,如图2是目前研究较多的一类燃料电池的工作原理示意图。

①A极为电池极
②B极的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】燃料电池是利用燃料与氧气反应从而将化学能转化为电能的装置。
(1)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
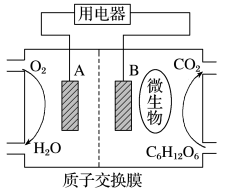
①A为生物燃料电池的_______ (填“正”或“负”)极。
②正极反应式为_______ 。
③放电过程中, 由
由_______ 极区向_______ 极区迁移(填“正”或“负”)。
④在电池反应中,每消耗 氧气,理论上生成标准状况下二氧化碳的体积是
氧气,理论上生成标准状况下二氧化碳的体积是_______ 。
(2)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇一氧化钠,其中 可以在固体介质
可以在固体介质 中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。
中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。

①工作时, 由电极
由电极_______ 向电极_______ 移动(填“a”或b”);
②电子由电极_______ 通过传感器流向电极_______ (填“a”或b”)。
(1)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①A为生物燃料电池的
②正极反应式为
③放电过程中,
 由
由④在电池反应中,每消耗
 氧气,理论上生成标准状况下二氧化碳的体积是
氧气,理论上生成标准状况下二氧化碳的体积是(2)一氧化碳无色无味有毒,世界各国每年均有不少人因一氧化碳中毒而失去生命。一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇一氧化钠,其中
 可以在固体介质
可以在固体介质 中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。
中自由移动。传感器中通过的电流越大,尾气中一氧化碳的含量越高。
①工作时,
 由电极
由电极②电子由电极
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:Cd+2NiO(OH)+2H2O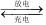 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是___________ ,负极的反应式是___________ 。放电时负极附近的溶液的碱性________ (填“不变”、“变大”或“变小”)。
(2)一种熔融碳酸盐燃料电池原理示意如图所示:

电池工作时,外电路上电流的方向应从电极________ (填A或B)流向用电器。内电路中,CO32-向电极___________ (填A或B)移动,电极A上CO参与的电极反应为___________ 。
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲醇(CH3OH)和氧气构成燃料电池,则通入甲醇的电极是原电池的____ 极,该极的电极反应式是____________ ,通入氧气的电极是原电池的____ 极,电极反应式是___________________ 。如果消耗甲醇160 g,假设化学能完全转化为电能,则转移电子的数目为_______________ (用NA表示)。
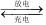 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是(2)一种熔融碳酸盐燃料电池原理示意如图所示:

电池工作时,外电路上电流的方向应从电极
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲醇(CH3OH)和氧气构成燃料电池,则通入甲醇的电极是原电池的
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有机化合物是构成生命的基础物质,因此。对有机化合物的结构、性质、制备以及应用的研究显得尤为重要。根据要求回答下列问题:
A. B.
B.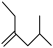 C.
C.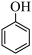 D.
D.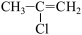 E.
E.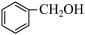 F.
F.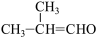
(1)用系统命名法命名A物质:_____ ,A的一氯代物有_____ 种。
(2)B物质的分子式为_____ ,按官能团分类,B所属的类别是_____ 。
(3)在C中加入足量的浓溴水,观察到的现象是_____ 。
(4)D能发生加聚反应,其产物的结构简式为_____ 。
(5)写出E在浓硫酸作催化剂并加热到140℃时发生的化学反应方程式:_____ 。
(6)检验F中官能团可以选择银氨溶液,写出银氨溶液的配制方法_____
A.
 B.
B. C.
C. D.
D.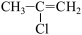 E.
E.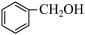 F.
F.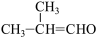
(1)用系统命名法命名A物质:
(2)B物质的分子式为
(3)在C中加入足量的浓溴水,观察到的现象是
(4)D能发生加聚反应,其产物的结构简式为
(5)写出E在浓硫酸作催化剂并加热到140℃时发生的化学反应方程式:
(6)检验F中官能团可以选择银氨溶液,写出银氨溶液的配制方法
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列有机物的名称。
(1)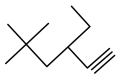 :
:__________
(2)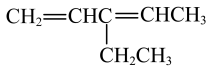 :
:__________
(3)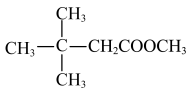 :
:__________
(4)CH2=CHCH2Cl:__________
(5)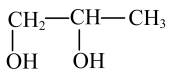 :
:__________
(6)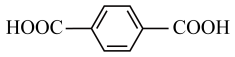 :
:__________
(7)CH3OCH3:__________
(8) :
:__________
(1)
 :
:(2)
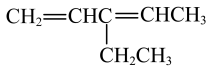 :
:(3)
 :
:(4)CH2=CHCH2Cl:
(5)
 :
:(6)
 :
:(7)CH3OCH3:
(8)
 :
:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种有机物,A、B属于烃类物质,C、D都是烃的衍生物。A是含氢质量分数最大的有机物,分子结构为正四面体;B的球棍模型为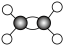 ;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为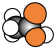 ,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
(1)A的电子式是___________ ,C中官能团的名称是___________ 。
(2)B的结构简式是___________ ,该物质发生加聚反应的化学方程式为___________ 。
(3)C与D在一定条件下反应生成一种有香味的物质,写出其化学方程式___________ 。
(4)下列说法正确的是___________ (填序号),
①B与其加聚反应产物组成元素及其原子个数比相同
②A与B都属于烃类,二者互为同系物
③C和D中都有—OH,其水溶液都显酸性
 ;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为 ,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:(1)A的电子式是
(2)B的结构简式是
(3)C与D在一定条件下反应生成一种有香味的物质,写出其化学方程式
(4)下列说法正确的是
①B与其加聚反应产物组成元素及其原子个数比相同
②A与B都属于烃类,二者互为同系物
③C和D中都有—OH,其水溶液都显酸性
您最近半年使用:0次



