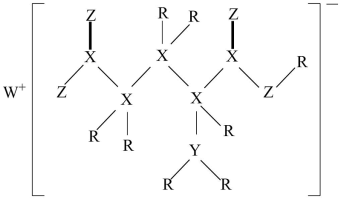
已知W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Z位于同一主族,X、Y位于同一周期,W元素原子的核外电子数与其周期序数相等,X的常见单质液态时是淡蓝色,常温下,Y的常见单质是一种有颜色的气体。下列有关说法正确的是
A.简单离子半径: |
B.最简单氢化物的熔、沸点: |
| C.Y的最高价氧化物对应的水化物为强酸 |
| D.由W、X、Z形成的三元化合物只含有离子键 |
更新时间:2024-03-31 21:55:57
|
相似题推荐
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,其中仅Z为金属元素,X、W为同一主族元素。甲、乙、丙均为含Y元素的化合物,其中甲、丙中的X、W均为最高价。x、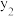 、w分别为X、Y、W的单质。其转化关系如图所示,下列判断正确的是
、w分别为X、Y、W的单质。其转化关系如图所示,下列判断正确的是

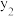 、w分别为X、Y、W的单质。其转化关系如图所示,下列判断正确的是
、w分别为X、Y、W的单质。其转化关系如图所示,下列判断正确的是
| A.反应①属于氧化还原反应,反应②属于非氧化还原反应 |
| B.Z的最高价氧化物对应的水化物可能为强碱 |
| C.一定条件下,x与甲反应可生成乙 |
| D.反应②可以证明X的非金属性强于W |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】下列有关实验的描述正确的是
选项 | 操作 | 实验目的 |
A | 沿玻璃棒将蒸馏水缓慢倒入盛有浓硫酸的烧杯中,边加边搅拌 | 稀释浓硫酸 |
B | 测定相同浓度的Na2SO4和Na2SiO3溶液的pH值 | 比较硫和硅的非金属性强弱 |
C | 将铁的氧化物溶于过量稀盐酸中,再滴加几滴紫红色KMnO4溶液 | 判断某铁的氧化物是否含有Fe2+ |
D | 向2 mL 0.1 mol·L–1 NaOH溶液中滴加足量0.1mol·L–1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1 mol·L–1 FeCl3溶液,出现红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是p能级的两倍,Z和M位于同一主族,由上述五种元素形成的化合物可作离子导体,结构如图所示。下列说法错误的是
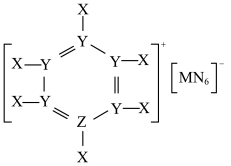

| A.原子半径:M>Y>Z>X |
| B.非金属性:M>N,Y>Z |
| C.氢化物沸点:Z>N>M>Y |
| D.同周期中第一电离能小于Z的元素有5种 |
您最近半年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】某公司研发出了一种新型除草剂,其结构如下图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M与Z同主族,W是地壳中含量最多的元素。下列叙述错误的是


| A.简单原子半径:M>Z>W |
| B.氧化物对应水化物的酸性:Z强于M |
| C.X与Y组成的最简单化合物的稳定性大于Z与X组成的化合物的稳定性 |
| D.X、Z、W三种元素既可组成共价化合物又可组成离子化合物 |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是
| 元素代号 | X | Y | Z | W | R |
| 原子半径/pm | 160 | 143 | 70 | 66 | 53 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 | +1 |
| A.元素X的最高价氧化物对应水化物的碱性比Y的强 |
| B.化合物XW、ZW中化学键类型相同 |
| C.元素Z的简单气态氢化物的热稳定性比W的强 |
| D.Z、W、R三种元素既可组成共价化合物,也可组成离子化合物 |
您最近半年使用:0次
多选题
|
较难
(0.4)
【推荐3】X、Y、Z、G、W 为原子序数依次增大的 5 种短周期元素。X 的质子数与电子层数相同,Y、Z、G 同周期且相邻,W 原子核外电子数是 G 原子最外层电子数的 2 倍。Z 与其同主族的短周期元素可形成常见气体甲。X、Y、G 三种元素形成六核化合物乙。下列说法正确的是
| A.化合物乙中只有共价键 |
| B.甲可与 Z 和 X 形成的某种化合物反应生成强酸 |
| C.W 的氧化物只能与碱反应,不能与任何酸反应 |
| D.X 分别与 Y、Z、G、W 形成的气态化合物中,稳定性最好的是 XG |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为14,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的2倍。下列说法不正确的是
| A.Y的氧化物既可与强酸反应又可与强碱反应,并可用来制作耐火材料 |
| B.X的氢化物是分子晶体,因其分子间存在氢键,所以该晶体更稳定 |
| C.X和Z的最高价氧化物对应的水化物的浓溶液都是具有强氧化性的酸 |
| D.X氢化物的水溶液与X最高价氧化物对应的水化物的水溶液不能相互反应 |
您最近半年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】X、Y、Z、W是原子序数依次增大的短周期主族元素,Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和比为5:4。下列说法正确的是
| A.原子半径:r(W)>r(Z) >r(Y) >r(X) |
| B.Z的简单气态氢化物的热稳定性比Y的强 |
| C.由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应 |
| D.由X、Y、Z三种元素组成的化合物可以是酸、碱或盐 |
您最近半年使用:0次
多选题
|
较难
(0.4)
【推荐1】甲、乙、丙、丁都是短周期元素,其中甲、丁在周期表中的相对位置如下表,甲原子最外层电子数是其内层电子数的2倍,乙单质在空气中燃烧发出黄色火焰,丙是地壳中含量最高的金属元素。下列判断正确的是


| A.原子半径:丙>丁 |
| B.甲与丁的核外电子数相差10 |
| C.氢氧化物碱性:乙>丙 |
| D.甲、乙的最高价氧化物均是共价化合物 |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】X、Y、Z、W 是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法错误的是
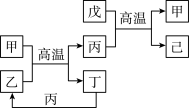

| A.W的原子序数是 Z 的两倍,金属性强于Z |
| B.W元素在周期表中的位置是第四周期VIII族 |
| C.己属于两性氧化物 |
| D.等物质的量的甲和戊完全溶于稀硝酸,消耗的HNO3的量相等 |
您最近半年使用:0次