下列事实对应的方程式不正确的是
A.用氨水吸收烟气中少量的 : :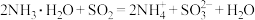 |
B.浓硝酸保存于棕色试剂瓶中的原因: |
C.AgCl沉淀溶于氨水: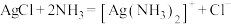 |
D.白醋可除去水壶中的水垢: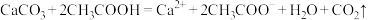 |
更新时间:2024-03-29 18:34:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列指定反应的离子方程式正确的是
A.双氧水使酸性KMnO4溶液褪色:2MnO +5H2O2=2Mn2++5O2↑+6OH-+2H2O +5H2O2=2Mn2++5O2↑+6OH-+2H2O |
B.过量的铁粉溶于稀硝酸:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
C.用Na2S2O3溶液吸收水中的Cl2:4Cl2+S2O +5H2O=10H++2SO +5H2O=10H++2SO +8Cl- +8Cl- |
D.向NaAlO2溶液中通入过量CO2:2AlO +CO2+3H2O=2Al(OH)3↓+CO +CO2+3H2O=2Al(OH)3↓+CO |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写正确的是
| A.NaClO溶液和FeCl2溶液混合:2ClO-+Fe2++2H2O=Fe(OH)2↓+2HClO |
B.苯酚浊液与纯碱溶液混合后变澄清:2C6H5OH+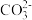 =2C6H5O-+CO2↑+H2O =2C6H5O-+CO2↑+H2O |
C.用过量氨水吸收工业尾气中的SO2:2NH3∙H2O+SO2=2 + + +H2O +H2O |
D.用铜制作电极电解CuSO4溶液:2Cu2++2H2O 2Cu↓+O2↑+4H+ 2Cu↓+O2↑+4H+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列物质敞口露置于空气中,质量基本不变的是
| A.氢氧化钠 | B.氯化钠 | C.浓盐酸 | D.浓硫酸 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的个数是
①CO2、NO2、P2O5均为酸性氧化物
②熔融状态下,H3CCOOH、NaOH、MgCl2均能导电
③芒硝的风化、浓硝酸久置变黄均为化学变化
④漂白粉、水玻璃、铝热剂均为混合物
⑤C60、碳纳米管、石墨烯互为同素异形体
⑥盐酸、亚硫酸、氯气分别为强电解质、弱电解质和非电解质
⑦金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
⑧硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
⑨因为胶粒比溶液中溶质粒子大,所以胶体可以用渗析的方法进行提纯
⑩胶体区别于其他分散系的本质特征是丁达尔效应
①CO2、NO2、P2O5均为酸性氧化物
②熔融状态下,H3CCOOH、NaOH、MgCl2均能导电
③芒硝的风化、浓硝酸久置变黄均为化学变化
④漂白粉、水玻璃、铝热剂均为混合物
⑤C60、碳纳米管、石墨烯互为同素异形体
⑥盐酸、亚硫酸、氯气分别为强电解质、弱电解质和非电解质
⑦金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
⑧硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
⑨因为胶粒比溶液中溶质粒子大,所以胶体可以用渗析的方法进行提纯
⑩胶体区别于其他分散系的本质特征是丁达尔效应
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近半年使用:0次
【推荐1】配合物Na2[Fe(CN)5(NO)]可用于离子检验,下列说法错误的是
| A.此配合物中存在离子键、配位键、极性键 |
| B.配离子为[Fe(CN)5(NO)]2-,中心离子为Fe3+,配位数为6 |
| C.1 mol配合物中σ键数目为10NA |
| D.该配合物为离子化合物,1 mol该配合物含有阴、阳离子的总数为3NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】研究笼形包合物结构和性质具有重要意义,化学式为Ni(CN)x•Zn(NH3)y•zC6H6的笼形包合物四方晶胞结构如图所示(H原子未画出)。每个苯环只有一半属于该晶胞,晶胞参数为a=b≠c,α=β=γ=90°。晶胞中N原子均参与形成配位键。下列说法不正确的是
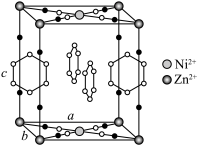

| A.基态Ni原子的价电子排布式为3d84s2 |
| B.Ni2+与Zn2+的配位数之比为2:3 |
| C.x:y:z=2:1:1 |
| D.晶胞中有d轨道参与杂化的金属离子是Zn2+ |
您最近半年使用:0次

 =BaSO4↓
=BaSO4↓ +Ca2++2OH-=CaCO3↓+
+Ca2++2OH-=CaCO3↓+ +2H2O
+2H2O


