原电池是一种能将化学能直接转化为电能的装置。
Ⅰ.下图是一种简易氢氧燃料电池装置。___________ ;正极的电极反应式是___________ 。
(2)能够证实该装置产生电流的现象是___________ 。
(3)如用KOH代替稀硫酸,则负极的电极反应式是___________ ;正极的电极反应式是___________ 。
Ⅱ.下图是另一种原电池装置。___________ 。
(5)正极的电极反应式是___________ 。
(6)下列叙述正确的是___________ (填字母)。
a. 在Cu表面被还原,产生气泡 b.电流从Zn片经导线流向Cu片
在Cu表面被还原,产生气泡 b.电流从Zn片经导线流向Cu片
c.电子从Zn片经导线流向Cu片 d.Zn和Cu的都是电极材料,也都参与电极反应
Ⅲ.某小组同学应用以下思路,将反应 设计成原电池装置。
设计成原电池装置。
(7)填空:①是(填物质的化学式,下同)___________ ,③是___________ 。⑤是___________ 。
(8)从以下选项中选出做负极材料的是(选填字母,下同)___________ ,最适合做正极材料的是___________ 。
a.Fe b.Cu c.石墨 d.Zn
Ⅰ.下图是一种简易氢氧燃料电池装置。
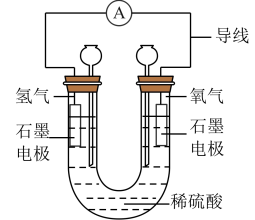
(2)能够证实该装置产生电流的现象是
(3)如用KOH代替稀硫酸,则负极的电极反应式是
Ⅱ.下图是另一种原电池装置。
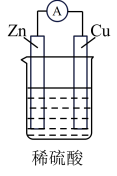
(5)正极的电极反应式是
(6)下列叙述正确的是
a.
 在Cu表面被还原,产生气泡 b.电流从Zn片经导线流向Cu片
在Cu表面被还原,产生气泡 b.电流从Zn片经导线流向Cu片c.电子从Zn片经导线流向Cu片 d.Zn和Cu的都是电极材料,也都参与电极反应
Ⅲ.某小组同学应用以下思路,将反应
 设计成原电池装置。
设计成原电池装置。反应: | |
| 确定负极 | 确定负极反应物① |
| 确定负极材料② | |
| 确定正极 | 确定正极反应物③ |
| 确定正极材料④ | |
| 确定离子导体 | ⑤ |
| 确定电子导体 | ⑥ |
(7)填空:①是(填物质的化学式,下同)
(8)从以下选项中选出做负极材料的是(选填字母,下同)
a.Fe b.Cu c.石墨 d.Zn
更新时间:2024-04-13 15:46:14
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】某同学为了探究原电池产生电流的过程,设计了如图所示实验。
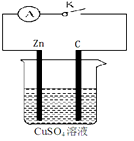
(1)打开K,观察到的现象为___________________________________________________ ,
(2)关闭K,观察到的现象是___________________________________________________ ,
此电池的负极的电极反应式为__________________________________________________ ,
总反应式为_________________________________________________ 。
(3)关闭K,溶液中阳离子向________________ (填Zn或C)极运动,
外电路中,电子流动方向是________________________ 。

(1)打开K,观察到的现象为
(2)关闭K,观察到的现象是
此电池的负极的电极反应式为
总反应式为
(3)关闭K,溶液中阳离子向
外电路中,电子流动方向是
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为___________ 。电池工作一段时间后需要充电,充电过程中H2SO4的浓度___________ (填“增大”、“减小”或“不变”)。
(2)某学习小组依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计成原电池,则负极发生的电极反应式为___________ ;当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应转移的电子数目是___________ 。
(3)燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为___________ (填物质名称),电解质溶液中的OH-移向___________ 极(填”负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:___________ 。
若该燃料电池为甲烷燃料电池。已知电池的总反应为CH4+2O2+2OH-=CO +3H2O。
+3H2O。
③下列有关说法正确的是___________ (填字母代号)。
A.燃料电池将电能转变为化学能
B.负极的电极反应式为CH4+10OH--8e-=CO +7H2O
+7H2O
C.正极的电极反应式为O2+4H++4e-=2H2O
D.通入甲烷的电极发生还原反应
④当消耗甲烷33.6L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为___________ mol。
(1)铅蓄电池在放电时发生的电池反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为
(2)某学习小组依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计成原电池,则负极发生的电极反应式为
(3)燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
②写出此氢氧燃料电池工作时,负极的电极反应式:
若该燃料电池为甲烷燃料电池。已知电池的总反应为CH4+2O2+2OH-=CO
 +3H2O。
+3H2O。③下列有关说法正确的是
A.燃料电池将电能转变为化学能
B.负极的电极反应式为CH4+10OH--8e-=CO
 +7H2O
+7H2OC.正极的电极反应式为O2+4H++4e-=2H2O
D.通入甲烷的电极发生还原反应
④当消耗甲烷33.6L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】电化学装置可实现化学能与电能的直接转化,是助力实现“30、60”双碳目标的一种重要路径。回答下列问题:
(1)①盐桥是电池发展史上一项重要技术突破,极大地提高了化学能→电能的转化效率,同时使电流更加稳定。若图1装置能形成铜锌原电池,则甲烧杯盛装:_______ [填ZnSO4(aq)或CuSO4(aq)];盐桥中装的是含有琼脂的KCl饱和溶液。
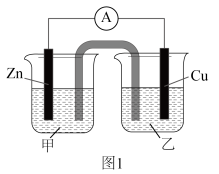
②将图1右池中的Cu电极材料换成_______ ,电解质溶液换成_______ ,可实现Zn+2Fe3+=Zn2++2Fe2+中能量直接转化为电能。
(2)电解池在工业及生产中广泛应用,其原理如图2和图3所示。
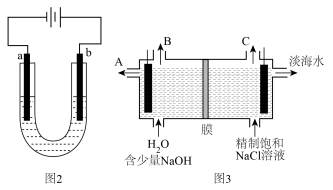
①电镀时,b电极应为_______ (选填“待镀金属”或“镀层金属”);精炼铜时,Cu2+的浓度变化是_______ (填“增大”,“不变”,“减小”)。
②图3氯碱工业中,选择的离子交换膜是_______ ,离子交换膜右侧电极产物是_______ ,左侧电极上发生的电极反应式为_______ 。
(3)二甲醚(CH3OCH3)燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质Ni的原理如图所示(反应中Ⅱ室NaCl溶液浓度变大)。
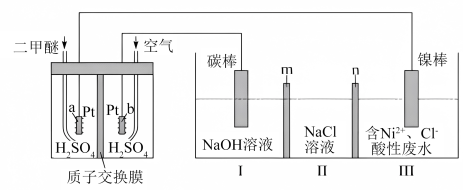
①a电极反应式为_______ ,发生_______ 反应。
②写出镍棒电极上发生的电极反应式为_______ 。m,n是否可以选择同种交换膜_______ (填“是”或“否”)请说明原因:_______ 。
(1)①盐桥是电池发展史上一项重要技术突破,极大地提高了化学能→电能的转化效率,同时使电流更加稳定。若图1装置能形成铜锌原电池,则甲烧杯盛装:

②将图1右池中的Cu电极材料换成
(2)电解池在工业及生产中广泛应用,其原理如图2和图3所示。

①电镀时,b电极应为
②图3氯碱工业中,选择的离子交换膜是
(3)二甲醚(CH3OCH3)燃料电池具有启动快、效率高等优点,以该电池为电源电解处理含镍废水并回收单质Ni的原理如图所示(反应中Ⅱ室NaCl溶液浓度变大)。

①a电极反应式为
②写出镍棒电极上发生的电极反应式为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:Cd+2NiO(OH)十2H2O 2 Ni(OH)2+ Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。正极的反应式是
2 Ni(OH)2+ Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。正极的反应式是____________________ ,负极的反应式是_________________ 。
(2)一种熔融碳酸盐燃料电池原理示意如图: 电池工作时,外电路上电流的方向应从电极___ (“填A或B”)流向用电器。内电路中,CO32-向电极_____ (“填A或B”)移动,电极A上CO参与的电极反应为______________________ 。
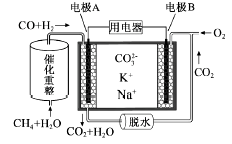
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的电极是原电池的____ 极,该极的电极反应式是____________________ ,电池工作时的总反应的离子方程式是__________________ 。如果消耗甲烷160g,假设化学能完全转化为电能,则转移电子的数目为___________ (用NA表示),需要消耗标准状况下氧气的体积为_______ L。
 2 Ni(OH)2+ Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。正极的反应式是
2 Ni(OH)2+ Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。正极的反应式是(2)一种熔融碳酸盐燃料电池原理示意如图: 电池工作时,外电路上电流的方向应从电极

(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的电极是原电池的
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】燃料电池在工业生产中有重要用途,肼燃料电池产物对环境无污染,能量高,有广泛的应用前景,其工作原理如图所示。回答下列问题
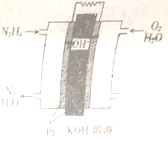
(1)该燃料电池中,负极通入的气体是_________ ,正极通入的气体是_________ .
(2)电池工作时,OH-向_____ 极移动,负极的电极反应式为_________ .
(3)肼在工业上常以氨和次氯酸钠为原料制得,其反应的化学方程式为2NH3+NaClO═N2H4+NaCl+H2O,该反应中每生成1molN2H4时,转移电子的物质的量为______ 。

(1)该燃料电池中,负极通入的气体是
(2)电池工作时,OH-向
(3)肼在工业上常以氨和次氯酸钠为原料制得,其反应的化学方程式为2NH3+NaClO═N2H4+NaCl+H2O,该反应中每生成1molN2H4时,转移电子的物质的量为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
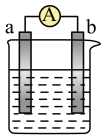
【推荐3】(1)下图是某化学兴趣小组探究化学能转变为电能的装置,若依据氧化还原反应: Cu+2Fe3+= Cu2++2Fe2+设计原电池,电极a为石墨、则电极b为电池的______ 极,发生的电极反应式为:___________ ,电极a上发生的电极反应为_____ (填“氧化”或“还原"反应。
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为某种甲烷燃料电池示意图,工作时电子流向如图所示。
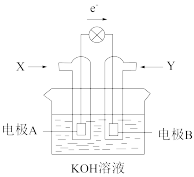
写出电极A的电极方程式________________ ,电极A附近pH如何变化?______________ (填“变大”或“变小”)。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4- SOCl2。电池的总反应可表示为:4Li+2SOCl= 4LiCl+S+ SO2。已知SOCl2会与水反应有刺激性气味的气体生成:SOCl2+ H2O=2HCl↑+ SO2↑。电池的负极材料为_________ ; 电池正极发生的电极反应式为_________ ;组装该电池必须在无水、无氧的条件下进行,原因是______________ 。

(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为某种甲烷燃料电池示意图,工作时电子流向如图所示。

写出电极A的电极方程式
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4- SOCl2。电池的总反应可表示为:4Li+2SOCl= 4LiCl+S+ SO2。已知SOCl2会与水反应有刺激性气味的气体生成:SOCl2+ H2O=2HCl↑+ SO2↑。电池的负极材料为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐1】燃料电池具有安全、高效的特点,请按要求回答下列问题。
I.新型甲醇(CH3OH)和O2燃料电池,装置如图a所示:
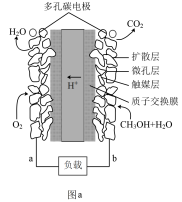
(1)b处的多孔碳电极是________ (填“正极”或“负极”);发生的电极反应式为_______ 。
Ⅱ.某兴趣小组的同学利用甲醇燃料电池探究氯碱工业原理等相关电化学问题,装置如图b所示,其中乙装置中X为离子交换膜。
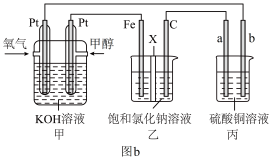
(2)乙中X是___________ (填“阳”或“阴”)离子交换膜。
(3)利用丙装置进行粗铜的电解精炼,则要求粗铜板是图中电极___________ (填图中的字母)。电解一段时间后,CuSO4溶液物质的量浓度___________ (填“增大”“减小”或“不变”)。
Ⅲ.乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。

(4)①N电极上的电极反应式为___________ 。
②若有2molH+通过质子交换膜并完全参与了反应,则该装置中生成的乙醛酸为___________ mol。
I.新型甲醇(CH3OH)和O2燃料电池,装置如图a所示:

(1)b处的多孔碳电极是
Ⅱ.某兴趣小组的同学利用甲醇燃料电池探究氯碱工业原理等相关电化学问题,装置如图b所示,其中乙装置中X为离子交换膜。

(2)乙中X是
(3)利用丙装置进行粗铜的电解精炼,则要求粗铜板是图中电极
Ⅲ.乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示。该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。

(4)①N电极上的电极反应式为
②若有2molH+通过质子交换膜并完全参与了反应,则该装置中生成的乙醛酸为
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】1887年,英国人赫勒森发明了最早的干电池,如今干电池已经发展成为一个庞大的家族,种类达100多种。应用广泛的是Zn—MnO2干电池,其电解质溶液是ZnCl2—NH4Cl混合溶液。电池工作一段时间后,电池内存在7种物质:NH3、Mn2O3、ZnCl2、MnO2、NH4Cl、Zn和H2O。请回答下列问题
(1)该电池的负极材料是__ ;电池工作时,电子流向__ (填“正极”或“负极”,下同);放电时NH4+向___ 移动。
(2)该氧化还原反应的化学方程式为__ ,发生还原反应的物质是__ ,被氧化的元素是__ 。若有17.4g氧化剂参与反应,则电子转移数目为__ NA(NA表示阿伏加 德罗常数的值)。
(3)普通锌锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是___ 。
(4)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是__ 。欲除去Cu2+,最好选用下列试剂中的__ (填序号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(1)该电池的负极材料是
(2)该氧化还原反应的化学方程式为
(3)普通锌锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是
(4)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
a.NaOH b.Zn c.Fe d.NH3·H2O
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】一个完整的氧化还原反应的方程式可以拆开,写成两个“半反应式”,一个是氧化反应式,另一个是还原反应式。如2Fe3++Cu=2Fe2++Cu2+的拆写结果是:氧化反应为Cu-2e-=Cu2+,还原反应为2Fe3++2e-=2Fe2+,原电池的电极反应式也可利用此方法书写。请回答下列问题:
(1)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池 ,其电极分别是Ag2O和Zn,电解质溶液为KOH,电池总反应为Ag2O+Zn=2Ag+ZnO,据此判断Ag2O是____ 极,电极反应式为______________ ;Zn是 ____ 极,电极反应式为 _____________ 。放电时,电解质溶液中OH-移向________ 极。
(2)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则该原电池负极的电极反应式为______________________ ,正极的电极反应式为_______________________ 若电池工作过程中有5.6L O2(标准状况下)参于反应,则转移电子的物质的量为__________ 。
(1)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池 ,其电极分别是Ag2O和Zn,电解质溶液为KOH,电池总反应为Ag2O+Zn=2Ag+ZnO,据此判断Ag2O是
(2)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则该原电池负极的电极反应式为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐1】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知E(N-N)=akJ/mol,E(N≡N)=b kJ/mol,E(N-H)=c kJ/mol,E(H-O)=d kJ/mol,E(O=O)=e kJ/mol,则:N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=_____________ kJ·mol-1
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图1所示,则通入a气体的电极名称为______________ ,通入b气体的电极反应式为 _____________ 。(质子交换膜只允许H+通过)
(3)在一定温度和催化剂作用下,CH4和CO2可直接生成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图2所示,则该反应的最佳温度控制在_____ 左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难容物),将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为___________________ 。
(4)CH4还原法是处理NOX气体的一种方法。已知一定条件下CH4与NOX反应转化为N2和CO2,若标准状况下8.96L CH4可处理22.4L NOX,则X值为______ 。
(1)已知E(N-N)=akJ/mol,E(N≡N)=b kJ/mol,E(N-H)=c kJ/mol,E(H-O)=d kJ/mol,E(O=O)=e kJ/mol,则:N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图1所示,则通入a气体的电极名称为

(3)在一定温度和催化剂作用下,CH4和CO2可直接生成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图2所示,则该反应的最佳温度控制在
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难容物),将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
(4)CH4还原法是处理NOX气体的一种方法。已知一定条件下CH4与NOX反应转化为N2和CO2,若标准状况下8.96L CH4可处理22.4L NOX,则X值为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】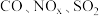 都是大气污染物,可利用化学反应原理给予消除。
都是大气污染物,可利用化学反应原理给予消除。
(1)在一定条件下利用反应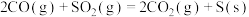 消除
消除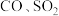 ,并获得硫黄。已知:①
,并获得硫黄。已知:①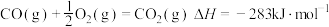 ,②
,②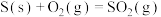
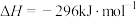 ,则
,则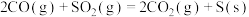

___________ 。
(2)利用CO还原NO的反应可消除汽车尾气引起的污染并获得电能,其简易装置如下图所示,(Na+交换膜两侧为等体积等浓度的 溶液):
溶液):
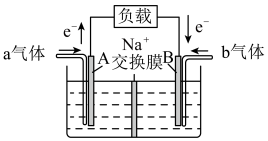
①电极A的电极反应式为___________ 。
②工作一段时间后,若B极区与A极区相差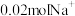 时,外电路中转移电子的物质的量是
时,外电路中转移电子的物质的量是___________ mol。
(3)利用下图所示的电化学装置可消除雾霾中的 、
、 。
。

①该装置中电子的流向是___________ (填“ ”或“
”或“ ”)。
”)。
②电极B的电极反应式为___________ 。
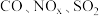 都是大气污染物,可利用化学反应原理给予消除。
都是大气污染物,可利用化学反应原理给予消除。(1)在一定条件下利用反应
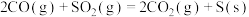 消除
消除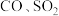 ,并获得硫黄。已知:①
,并获得硫黄。已知:①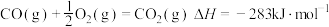 ,②
,②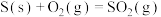
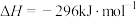 ,则
,则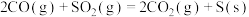

(2)利用CO还原NO的反应可消除汽车尾气引起的污染并获得电能,其简易装置如下图所示,(Na+交换膜两侧为等体积等浓度的
 溶液):
溶液):
①电极A的电极反应式为
②工作一段时间后,若B极区与A极区相差
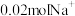 时,外电路中转移电子的物质的量是
时,外电路中转移电子的物质的量是(3)利用下图所示的电化学装置可消除雾霾中的
 、
、 。
。
①该装置中电子的流向是
 ”或“
”或“ ”)。
”)。②电极B的电极反应式为
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
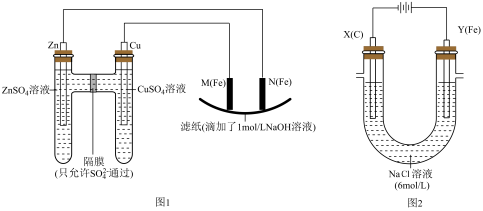
请回答:
Ⅰ.用如图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,能替代Cu做电极的是_________ (填字母序号).
(2)M极发生反应的电极反应式为_________ ;
(3)实验过程中,SO
_________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有_________ ,写出产生此现象的反应方程式:_________ ;
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH_________ (填“增大”、“减小”或“不变”);
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O 和 4OH--4e-═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少_________ g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料, 电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为_________ 。

请回答:
Ⅰ.用如图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,能替代Cu做电极的是
| A.铝 | B.石墨 | C.镁 | D.铂 |
(3)实验过程中,SO

Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O 和 4OH--4e-═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(6)在碱性锌电池中,用高铁酸钾作为正极材料, 电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为
您最近半年使用:0次



