华铁粉的主要成分为醋酸亚铁,可清热解毒,凉血消肿。以粗氯化铁(含少量 )为原料制备华铁粉的流程如下:
)为原料制备华铁粉的流程如下:
 )为原料制备华铁粉的流程如下:
)为原料制备华铁粉的流程如下: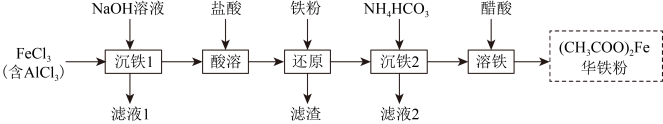
A.“沉铁1”中可用氨水替代 溶液 溶液 |
B.“还原”时加入铁粉的目的是将 转化成 转化成 |
C.滤液2的主要成分是 |
D.“溶铁”的离子方程式为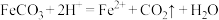 |
更新时间:2024-04-17 13:05:54
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】下列离子方程式正确的是
| A.向含1molFeBr2的溶液中通入1molCl2:2Fe2+ + 2Br- + 2Cl2=Br2 + 4Cl- + 2Fe3+ |
| B.向AlCl3溶液中加入过量氨水:Al3+ + 4OH- =AlO2- + 2H2O |
| C.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2+ + OH- + H+ +SO42-=BaSO4↓ + H2O |
| D.向澄清石灰水中加入过量的Ca(HCO3)2溶液:Ca2+ + OH- + HCO3-=CaCO3↓ + H2O |
您最近半年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】下列说法错误是
A.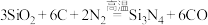 该反应中氧化剂和还原剂个数比为3∶1 该反应中氧化剂和还原剂个数比为3∶1 |
B.已知在碱性溶液中可发生反应: ,则 ,则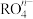 中R的化合价是+6 中R的化合价是+6 |
C.已知 , ,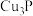 中 中 显+1价,则1个 显+1价,则1个 参与反应时,整个反应转移1个电子 参与反应时,整个反应转移1个电子 |
D.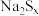 在碱性条件下可被 在碱性条件下可被 氧化为 氧化为 ,而 ,而 被还原为 被还原为 ,若反应中 ,若反应中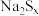 与 与 的个数比为1∶16,则x值为5 的个数比为1∶16,则x值为5 |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】某无色溶液中可能含有Mg2+、NH 、K+、Al3+、SO
、K+、Al3+、SO 、CO
、CO 、Cl-等离子。现进行如下实验:
、Cl-等离子。现进行如下实验:
①取10 mL该溶液于试管中,滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到6.99 g白色沉淀;
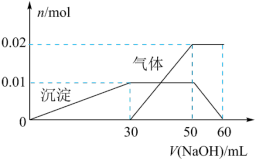
②另取10 mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示。
下列说法不符合事实的是
 、K+、Al3+、SO
、K+、Al3+、SO 、CO
、CO 、Cl-等离子。现进行如下实验:
、Cl-等离子。现进行如下实验:①取10 mL该溶液于试管中,滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到6.99 g白色沉淀;
②另取10 mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示。
下列说法不符合事实的是

| A.根据图中数据计算实验中使用的NaOH溶液的浓度为1 mol·L-1 |
| B.根据信息分析该溶液中焰色反应呈紫色的离子的物质的量浓度为1 mol·L-1 |
C.该溶液中NH 、Al3+、SO 、Al3+、SO 三种离子的物质的量之比为2∶1∶3 三种离子的物质的量之比为2∶1∶3 |
D.另取一定量该溶液滴加一定量Ba(OH)2溶液,能使Al3+和SO 同时完全沉淀 同时完全沉淀 |
您最近半年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】某些化学知识用数轴表示能体现出形象直观、简明易记的特点。下列用数轴表示不合理的是
| A | 铁和稀硝酸反应 | 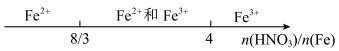 |
| B | 向烧碱溶液通入SO2后的产物 | 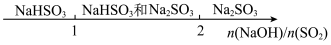 |
| C | Na与O2加热反应的产物 | 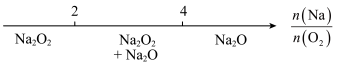 |
| D | 向NaOH溶液中滴加AlCl3溶液,铝元素的存在形式 | 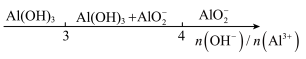 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
【推荐3】在MgCl2和AlCl3的混合溶液中,Cl-的物质的量为0.7 mol。向该溶液中逐渐加入100 mL 8 mol/L的KOH溶液,使之充分反应。反应前,若Al3+的物质的量与混合溶液中离子总物质的量的比值为x 。(不考虑Mg2+和Al3+水解及水电离对离子数目的影响),以下叙述正确的是
| A.x的取值范围是0<x≤0.25 |
| B.无论x为何值,当加入87.5 mL的KOH时,溶液中的阳离子恰好完全沉淀 |
| C.当100 mL KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的值为0.2 |
D.若反应前Al3+的物质的量为a mol,则a=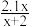 |
您最近半年使用:0次

 +Ba2++2OH-=BaSO4↓+Fe(OH)2↓
+Ba2++2OH-=BaSO4↓+Fe(OH)2↓ + Fe3++2
+ Fe3++2

