硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。____________ 。
(2)X与Y能发生反应,还原剂与氧化剂的物质的量之比为______ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是____________ 。
(4)硫酸是用途广泛的化工原料,可作脱水剂,吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸为原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即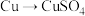
方案乙:由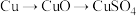
①方案甲中铜和浓硫酸反应的化学方程式是____________ 。该反应体现了浓硫酸的____________ 。
②这两种方案,你认为哪一种方案更合理?______ ,理由是____________ 。

(2)X与Y能发生反应,还原剂与氧化剂的物质的量之比为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)硫酸是用途广泛的化工原料,可作脱水剂,吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸为原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
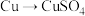
方案乙:由
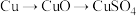
①方案甲中铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
更新时间:2024-05-04 10:38:09
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】反应 可用于氯气管道的检漏。
可用于氯气管道的检漏。
(1)该反应中作还原剂的物质是_______ (填化学式),氯元素的化合价_______ (填“升高”或“降低”);
(2)反应中每生成1mol ,消耗
,消耗 的物质的量是
的物质的量是_______ mol,同时转移电子的物质的量是_______ mol。
 可用于氯气管道的检漏。
可用于氯气管道的检漏。(1)该反应中作还原剂的物质是
(2)反应中每生成1mol
 ,消耗
,消耗 的物质的量是
的物质的量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是_______。
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_______ ,工艺师常用_______ (填物质名称)来雕刻玻璃。
(3)Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是_______ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)工业上常利用反应2C+SiO2 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是_______ (填化学式,下同),氧化剂是_______ 。
(1)下列物质不属于硅酸盐的是_______。
| A.陶瓷 | B.玻璃 | C.水泥 | D.生石灰 |
(3)Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)工业上常利用反应2C+SiO2
 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
您最近一年使用:0次
【推荐3】氧化还原反应是中学化学的重要内容。回答下列问题:
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为 。该反应中氧化剂为
。该反应中氧化剂为_______ ,还原产物为_______ 。
(2)用单线桥法表示电子转移的方向和数目:________
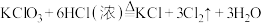
被氧化和被还原的氯原子的个数之比为_______ 。
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:__________
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为
 。该反应中氧化剂为
。该反应中氧化剂为(2)用单线桥法表示电子转移的方向和数目:
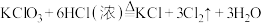
被氧化和被还原的氯原子的个数之比为
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4,向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(4)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(5)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液,选择合适试剂,并安排合理的顺序_______ (填序号)。

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4,向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:
(4)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(5)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液,选择合适试剂,并安排合理的顺序
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硫酸工业中热能的合理利用及三废处理
硫酸生产过程中的三个反应都是_____ ,为了充分利用这些热量,在生产过程中,沸腾炉外设置____ 回收高温废热,把__ 和转化器合为一体,将二氧化硫转化为三氧化硫时放出的热量及时导出用来__ 。
(1)废气:硫酸工业的尾气中含有的有毒气体是___ ,用___ 处理尾气的化学方程式分别为:_______________________ 、_________________________ 、_________________ 。
(2)废水:没有被污染的冷却水可以被____ ;若排出的是酸性废水,一般使用石灰乳等中和处理,反应的离子方程式为_____ 。
(3)废渣:以硫铁矿为原料生产硫酸,废渣的主要成分是____ 、硫化亚铁及少量有害物质。用废渣可以炼制的金属是____ 。
硫酸生产过程中的三个反应都是
(1)废气:硫酸工业的尾气中含有的有毒气体是
(2)废水:没有被污染的冷却水可以被
(3)废渣:以硫铁矿为原料生产硫酸,废渣的主要成分是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如图是自然界中不同价态硫元索之间的转化关系图,按要求回答问题:

(1)写出图中两种物质混合生成S,且S既是氧化产物又是还原产物的化学方程式____________________ 。
(2)工业生产硫酸的方法之一是:
①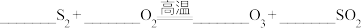 ,配平该反应方程式
,配平该反应方程式____________ ;
②__________________ ,写出该反应的方程式;
③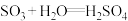 。
。
(3) 可用于焊接钢轨,写出该反应的化学方程式
可用于焊接钢轨,写出该反应的化学方程式___________________ 。
(4)硫酸是重要的化工原料,写出加热时铜和浓硫酸反应的化学方程式:____________________________ ,生成标准状况下 的还原性气体,转移的电子数为
的还原性气体,转移的电子数为_________________ 。

(1)写出图中两种物质混合生成S,且S既是氧化产物又是还原产物的化学方程式
(2)工业生产硫酸的方法之一是:
①
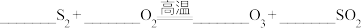 ,配平该反应方程式
,配平该反应方程式②
③
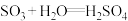 。
。(3)
 可用于焊接钢轨,写出该反应的化学方程式
可用于焊接钢轨,写出该反应的化学方程式(4)硫酸是重要的化工原料,写出加热时铜和浓硫酸反应的化学方程式:
 的还原性气体,转移的电子数为
的还原性气体,转移的电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现据“三大酸”与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,该反应的离子方程式为_ 。
(2)在一定体积的18mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol,则浓硫酸的实际体积__ (填“大于”“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可向其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__ 。
(3)根据如图操作及现象推断酸X为__ (填序号)。
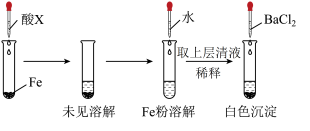
A.浓盐酸 B.浓硫酸 C.浓硝酸
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,该反应的离子方程式为
(2)在一定体积的18mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol,则浓硫酸的实际体积
(3)根据如图操作及现象推断酸X为

A.浓盐酸 B.浓硫酸 C.浓硝酸
您最近一年使用:0次





