一种用于心脏起搏器的微量电池具有能量大、寿命长等优点,其工作原理如图所示。下列说法正确的是
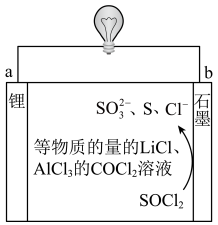
| A.b极为负极 |
B.该电池总反应的化学方程式为 |
C.外电路通过每 电子,理论上生成 电子,理论上生成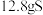 |
D.溶液中 移向b极 移向b极 |
更新时间:2024-05-24 22:52:58
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】2016年7月美国康奈尔大学的研究人员瓦迪·阿尔·萨达特和林登·阿彻在发表于《科学进展》(ScienceAdvances)上的一篇论文中,描述了一种能够捕捉二氧化碳的电化学电池的设计方案。其简易结构如下图。下列说法错误的是
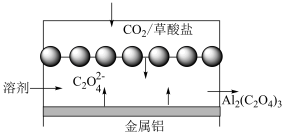

| A.金属铝作为还原剂参与负极的氧化反应 |
B.该装置除了吸收 之外还可得到化工产品 之外还可得到化工产品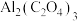 |
C.该装置每消耗27kg的金属铝,可以吸收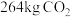 |
D.该装置的正极反应方程式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
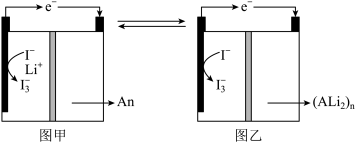
【推荐2】一种新型的“电池的正极采用含有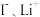 的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用
的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用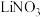 溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含
溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含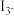 的溶液呈棕黄色,下列有关判断正确的是
的溶液呈棕黄色,下列有关判断正确的是
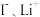 的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用
的水溶液,负极采用固体有机聚合物[用An, (Ali)n表示],电解质溶液采用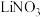 溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含
溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知含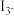 的溶液呈棕黄色,下列有关判断正确的是
的溶液呈棕黄色,下列有关判断正确的是
| A.图甲是原电池工作原理图,图乙是电池充电原理图 |
| B.放电时,正极液态电解质溶液的颜色变浅 |
C.放电时, 从右向左通过聚合物离子交换膜 从右向左通过聚合物离子交换膜 |
D.放电时,负极的电极反应式为: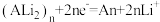 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据氧化还原反应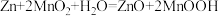 ,设计原电池,下列有关说法中正确的是
,设计原电池,下列有关说法中正确的是
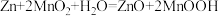 ,设计原电池,下列有关说法中正确的是
,设计原电池,下列有关说法中正确的是A. 在电池的正极发生氧化反应 在电池的正极发生氧化反应 |
| B.电流方向是从锌极流出并经过用电器流向二氧化锰电极 |
C.Zn极上发生的电极反应为 |
| D.电解质溶液可能是稀硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3。Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用该原理处理污水,设计装置如图所示。下列说法正确的是
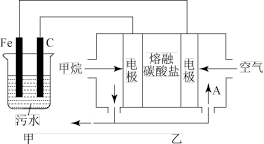

| A.为了增加污水的导电能力,应向污水中加入适量的H2SO4溶液 |
| B.甲装置中Fe电极的反应为Fe-3e-=Fe3+ |
| C.当乙装置中有1.6gCH4参加反应,则C电极理论上生成气体体积为4.48L |
| D.为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
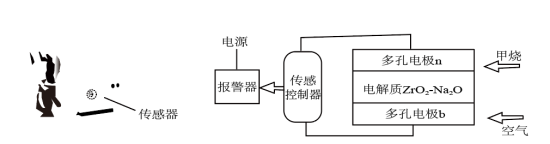
【推荐1】1.天然气报警器的核心是气体传感器,当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警,工作原理如图所示,其中 可以在固体电解质
可以在固体电解质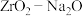 中移动。当报警器触发工作时,下列说法正确的是
中移动。当报警器触发工作时,下列说法正确的是
 可以在固体电解质
可以在固体电解质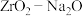 中移动。当报警器触发工作时,下列说法正确的是
中移动。当报警器触发工作时,下列说法正确的是
A.多孔电极 发生氧化反应 发生氧化反应 |
B. 在电解质中向电极 在电解质中向电极 移动 移动 |
C.多孔电极 极的电极反应式为 极的电极反应式为 |
D.当标准状况下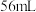 的甲烷在多孔电极 的甲烷在多孔电极 完全反应时,流入传感控制器电路的电子有 完全反应时,流入传感控制器电路的电子有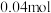 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家研发了一种水系可逆Zn-CO2电池,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充电、放电时,复合膜层间的H2O解离成H+和OH-,工作原理如图所示。下列说法错误的是( )


| A.a膜是阳离子膜,b膜是阴离子膜 |
| B.放电时负极的电极反应式为Zn+4OH--2e-=Zn(OH)42- |
| C.充电时CO2在多孔Pd纳米片表面转化为甲酸 |
| D.外电路中每通过1mol电子,复合膜层间有1mol H2O解离 |
您最近一年使用:0次

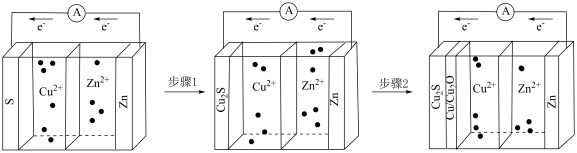
 溶液,步骤2中的电池反应为:
溶液,步骤2中的电池反应为: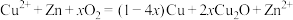 (单独构建该步电池时效率较低)。下列说法不正确的是
(单独构建该步电池时效率较低)。下列说法不正确的是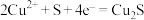
 对步骤2的正极反应可能起催化作用,提高了电池工作效率
对步骤2的正极反应可能起催化作用,提高了电池工作效率

