已知X、Y、Z、V、T为原子序数依次增大的前四周期元素,其中X、W同主族,Z、T同主族,Z是Y、W的相邻元素,W元素的最高价与最低价的代数和为4。下列叙述错误的是
| A.Y元素主要以盐和氧化物的形式存在于自然界 |
| B.最高价含氧酸的酸性:W>Z>T |
| C.X元素分别与Z、W、T元素能形成至少两种二元共价化合物 |
| D.简单氢化物的沸点与稳定性X均高于W的原因相同 |
更新时间:2024-05-19 20:03:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
| A.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B.青铜是我国使用最早的合金,钢是用量最大、用途最广泛的合金 |
| C.铁容器可以盛放浓盐酸、浓硝酸、浓硫酸 |
| D.漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列对单质硅的有关叙述正确的是
| A.晶体硅和金刚石的物理性质相似 |
| B.晶体硅常温下不与任何物质发生反应 |
| C.晶体硅是一种良好的半导体材料,但是它的提炼工艺复杂,价格昂贵 |
| D.硅的化学性质不活泼,在自然界中既有游离态又有化合态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】化学上存在许多的递变关系,下列递变关系完全正确的是
| A.原子半径:Na>Mg>Al>Cl;离子半径:Na+>Mg2+>Al3+>Cl- |
| B.稳定性:HF>HCl>HBr>HI;熔沸点:HF>HCl>HBr>HI |
| C.熔沸点:Li>Na>K>Rb;密度:Li<Na<K<Rb |
| D.酸性:HClO4>H2SO4>H2CO3;非金属性Cl>S>C |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期主族元素X、Y、Z、Q在元素周期表中的相对位置如图所示,已知X、Y、Q三种元素最外层电子数之和为17。则下列说法正确的是
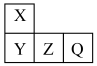
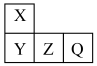
| A.Q的单质是一种黄绿色有毒气体 | B.Q元素只有负价,没有最高正价 |
C.原子半径: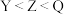 | D.X元素的最高价氧化物对应的水化物为中强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、M的原子序数依次增大,Z的基态原子的2p轨道半充满,M的最高正价与最低负价的绝对值之差为4,由这4种元素组成的一种分子的结构如图所示。下列说法正确的是
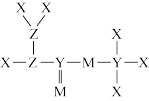

A.电负性: |
B.简单气态氢化物的热稳定性: |
C.第一电离能: |
| D.X与Z、M形成的化合物中,一定不含离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】LiY2ZXW2能够在锂离子电池负极形成稳定、低阻抗的SEI膜,帮助锂离子电池在高温环境中获得良好性能。[Y2Z4XW2]-的结构如图,图中原子最外层都达到8电子稳定结构,X、Y、Z、W位于同一短周期,元素X的最外层电子数是其内层电子数的1.5倍,W是同周期中原子半径最小的元素。下列说法正确的是
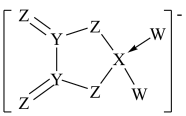
| A.该结构中,X、Y、Z之间形成的化学键均为共价键 |
| B.Y和Z形成的化合物都能和碱发生反应 |
| C.X、Y的最高价氧化物对应的水化物均是强酸 |
| D.Z和W分别与氢元素形成的10电子化合物的沸点:后者高于前者 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】结构决定性质,下列关于化学事实及其解释不正确的是
A.卤化氢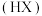 的沸点随着原子序数增大而增大,原因是分子间作用力增大 的沸点随着原子序数增大而增大,原因是分子间作用力增大 |
B. 分子可以稳定存在,原因是共价键键能大 分子可以稳定存在,原因是共价键键能大 |
C. 的酸性比 的酸性比 强,原因是 强,原因是 的电负性比 的电负性比 大,导致 大,导致 的羧基中的羟基极性更大 的羧基中的羟基极性更大 |
D.乙烯容易发生加成反应,原因是碳原子间形成的 键键能小容易断裂 键键能小容易断裂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2023年诺贝尔化学奖授予Moungi G.Bawendi、Louis E.Brus和Alexey I.Ekimov,以表彰他们在发现和合成量子点方面所作出的贡献,碳量子点又称碳纳米点,其表面富含羧基(—COOH)、羟基(—OH)等官能团。下列说法错误的是
| A.碳量子点具有酸性 | B.碳量子点水溶性好与分子间氢键有关 |
| C.碳量子点与金刚石互为同素异形体 | D.碳量子点中存在sp2杂化的碳原子 |
您最近一年使用:0次


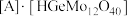 ,其中
,其中 含
含 、
、 、
、 、
、 、
、 五种原子序数依次增大的短周期主族元素,且在每个周期均有分布。基态
五种原子序数依次增大的短周期主族元素,且在每个周期均有分布。基态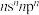 ,
, 和
和 都属于过渡元素
都属于过渡元素



