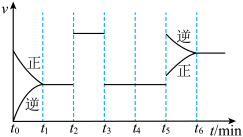
下列说法正确的是
| A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率 |
| B.对于反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
| C.将铜片放入稀硫酸中,无明显现象;若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生 |
| D.100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
13-14高一下·四川成都·期末 查看更多[8]
(已下线)2013-2014学年四川成都外国语学校高一下期末化学试卷2014-2015学年湖北省荆门市高一下学期期末质量检测化学试卷云南省会泽县茚旺高级中学2018-2019学年高二上学期12月月考化学试题【全国百强校】江西省九江第一中学2018-2019学年高二上学期期末考试化学试题(已下线)【南昌新东方】江西省九江市第一中学2018-2019学年高二上学期期末考试化学试题吉林省通化县综合高级中学2020-2021学年高一下学期期末考试化学试题江西省全南中学2022-2023学年高一下学期教学质量验收化学试题(已下线)合格考汇编12化学反应与能量
更新时间:2016-12-09 06:38:38
|
相似题推荐
【推荐1】N2(g)+3H2(g)⇌2NH3(g),∆H=-akJ·mol-1反应过程中的能量变化如图所示(图中 E1表示无催化剂时正反应活化能的数值,E2表示无催化剂时逆反应活化能的数值)。下列说法错误的是


| A.升高温度可提高 N2、H2、NH3的活化分子百分数 |
| B.a = E2-E1 |
| C.恒温恒压条件下通氦气的瞬间,单位体积内 N2的活化分子数减小 |
| D.将 1molN2(g) 和 3molH2(g) 置于密闭容器中充分反应放出 akJ 的热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法中正确的是
| A.凡是放热反应都是自发的,吸热反应都是非自发的 |
| B.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的∆S<0 |
| C.使用催化剂可降低反应的∆H和反应的活化能,从而提高化学反应速率 |
| D.升高温度,可使单位体积内活化分子数增多,反应速率加快 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列措施对增大反应速率明显有效的是( )
| A.Na与水反应时增大水的用量 |
| B.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| C.在K2SO4与BaCl2两溶液反应时,加入少量氯化钠固体 |
| D.将铝片改为铝粉,做铝与氧气反应的实验 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列日常生活做法中与控制反应速率无关的是
| A.用煤粉代替煤块 | B.向食盐中添加碘酸钾 |
| C.向炉膛内鼓入空气 | D.用冰箱冷藏食物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率但不影响生成H2的总量,可向盐酸中加入适量的( )
| A.CaCO3(s) | B.Na2SO4溶液 | C.KNO3溶液 | D.CuSO4(s) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】用锌片与稀硫酸反应制取氢气时,下列措施使氢气生成速率变化最小的是
| A.加入少量硫酸铜晶体 | B.将稀硫酸改为浓硫酸 |
| C.用锌粉代替锌片 | D.加入少量 晶体 晶体 |
您最近一年使用:0次

 2HI(g),ΔH<0,根据如图,下列说法错误的是(
2HI(g),ΔH<0,根据如图,下列说法错误的是(