下列说法正确的是
| A.在铁片上镀铜时,若阴极增重3.2g,则电镀液中通过的电子的物质的量为0.1mol |
| B.钢铁电化学腐蚀的两种类型主要区别在于水膜的PH不同,引起的负极反应不同 |
| C.参加反应的物质的性质是决定化学反应速率的重要因素 |
| D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极区产生的Cl2进入阳极区 |
14-15高二上·浙江温州·期中 查看更多[3]
(已下线)2014-2015学年浙江省温州市十校联合体高二上学期期中联考化学试卷2015届福建省三明市一中高三上学期第二次月考化学试卷黑龙江省哈尔滨市阿城区龙涤中学校2019-2020学年高二上学期期中考试化学试题
更新时间:2016-12-09 06:46:44
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是( )
| A.工业上电解熔融的Al2O3冶炼铝用铁做阳极 |
| B.用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1molNaOH |
| C.用Pt做电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1∶2 |
| D.用碳棒做电极电解CuSO4溶液一段时间后,加入Cu(OH)2固体可以使CuSO4溶液恢复原来浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A.电解饱和食盐水时,阳极的电极反应为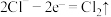 |
B.酸性氢氧燃料电池的正极电极反应为 |
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为 |
D.用铁作电极电解硫酸钠溶液: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】为节约资源,许多重要的化工产品可以进行联合生产。如氯碱工业、金属钛的冶炼工业、甲醇的合成工业可以进行联合生产。联合生产时的物质转化如下图所示:
部分反应的热化学方程式为:
2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
CO(g)+2H2(g)=CH3OH(g) ΔH=-90.7kJ·mol-1
TiO2(s)+2C(s)+2Cl2(g)=TiCl4(l)+2CO(g) ΔH=-70.0kJ·mol-1
下列关于联合生产的有关说法正确的是
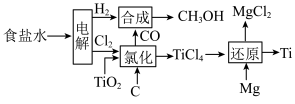
部分反应的热化学方程式为:
2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
CO(g)+2H2(g)=CH3OH(g) ΔH=-90.7kJ·mol-1
TiO2(s)+2C(s)+2Cl2(g)=TiCl4(l)+2CO(g) ΔH=-70.0kJ·mol-1
下列关于联合生产的有关说法正确的是
| A.通过电解MgCl2溶液可以实现镁的再生 |
| B.电解饱和食盐水时,阳极附近溶液pH升高 |
| C.还原反应时,每生成48gTi,反应共转移2mol电子 |
| D.反应TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)在任何条件下均不能自发进行 |
您最近一年使用:0次
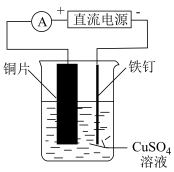
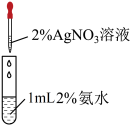
【推荐1】下述装置或操作能实现相应实验目的的是
| 装置或操作 |
|
|
| 实验目的 | 铁钉表面镀铜 | 配制银氨溶液 |
| 选项 | A | B |
| 装置或操作 |
|
|
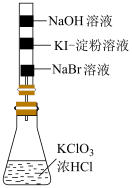
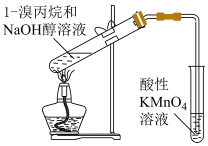
| 实验目的 | 验证氧化性:Cl2>Br2>I2 | 检验1-溴丙烷的消去反应产物丙烯 |
| 选项 | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】关于下列装置说法正确的是


| A.装置①中,盐桥中的 K+移向CuSO4溶液 |
| B.装置②在电解过程中,a极上得到22.4 L气体(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
| C.可以用装置③在铜上镀银,c极为银 |
| D.装置④中一段时间后会有Fe(OH)2生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】钢铁在潮湿空气中发生电化腐蚀时,正极发生的主要反应是( )
| A.Fe-2e-=Fe2+ | B.2H++2e-=H2 | C.4OH --4e-=2H2O+O2 | D.2H2O+O2+4e-=4OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中,正确的是
| A.铅蓄电池放电时铅电极发生还原反应 |
| B.钢铁吸氧腐蚀的正极反应:O2+2e-+2H2O=4OH- |
| C.给铁钉镀铜可采用Cu2+作电镀液 |
| D.生铁浸泡在食盐水中发生析氢腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用惰性电极电解法制备硼酸[H3BO3或B(OH)3]的工作原理如图所示。下列有关说法不正确的是


| A.电流方向:电源正极→b电极→电解液→a电极→电源负极 |
| B.膜A为阳膜,膜B为阴膜 |
| C.a极区加入氢氧化钠是为了增强溶液的导电性 |
| D.当电路中通过3 mol电子时,可得到1 mol H3BO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】H3BO3(一元弱酸)可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图,下列叙述错误的是
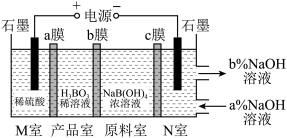

| A.M室发生的电极反应式为:2H2O-4e-=O2↑+4H+ |
| B.b膜为阴膜,产品室发生反应的化学原理为强酸制弱酸 |
| C.理论上每生成1 mol产品,阴极室可生成标准状况下5.6 L气体 |
| D.N室中:a%<b% |
您最近一年使用:0次

 溶液
溶液 与
与 的酸性强弱
的酸性强弱 溶液与
溶液与 溶液的pH
溶液的pH 与
与 对
对 分解的催化效果
分解的催化效果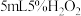 溶液的试管中滴入2滴
溶液的试管中滴入2滴 的
的 溶液与
溶液与 溶液
溶液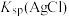 与
与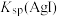 的大小
的大小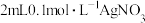 溶液的试管中滴入2滴
溶液的试管中滴入2滴 溶液,振荡试管,再向其中滴入4滴
溶液,振荡试管,再向其中滴入4滴 溶液
溶液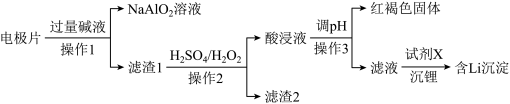
 和
和 ,实验原理示意图如下。
,实验原理示意图如下。
 则有2mol H+转移
则有2mol H+转移


