实验室制备硝基苯的反应原理和实验装置如下:
有关数据列如下表
取100mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)装置B的名称是_______________ 。装置C的作用是_________________________ 。
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:________________ 。
(3)为了使反应在50℃~60℃下进行,常用的方法是______________________ 。
(4)在洗涤操作中,第二次水洗的作用是__________________________ 。
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是_____________________________________________ 。
(6)本实验所得到的硝基苯产率是____________________________________ 。
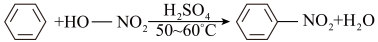 ΔH<0
ΔH<0
有关数据列如下表
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
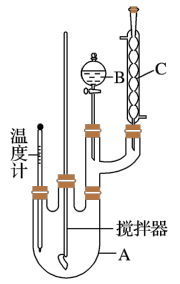
取100mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)装置B的名称是
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:
(3)为了使反应在50℃~60℃下进行,常用的方法是
(4)在洗涤操作中,第二次水洗的作用是
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是
(6)本实验所得到的硝基苯产率是
更新时间:2016-12-09 07:47:18
|
相似题推荐
解答题-实验探究题
|
困难
(0.15)
解题方法
【推荐1】实验室制备1,2—二溴乙烷的反应原理如下:
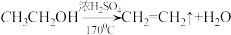 ②
②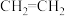 +
+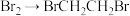
可能存在的的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用16.0g的溴和足量的乙醇制备1,2—二溴乙烷,实验结束后得到9.4g产品。实验装置如下图所示:
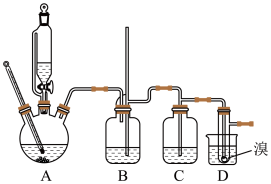
有关数据列表如下:
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是______ (填正确选项前的字母);
a、引发反应 b、加快反应速度
c、防止乙醇挥发 d、减少副产物乙醚生成
(2)在装置C中应加入______ ,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
(3)判断该制备反应已经结束的最简单的方法是________ 。
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____________ 层(填“上”或“下”);
(5)在装置B中较长玻璃导管的作用是_______ ;
(6)反应过程中应用冷水冷却装置D,其主要目的是________ ,但又不能过度冷却(如用冰水),其原因是_____ ;
(7)本实验中,1,2—二溴乙烷的产率为___________ 。
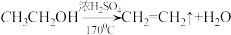 ②
②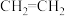 +
+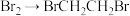
可能存在的的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用16.0g的溴和足量的乙醇制备1,2—二溴乙烷,实验结束后得到9.4g产品。实验装置如下图所示:

有关数据列表如下:
| 乙醇 | 1,2—二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度 / g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点 / 0C | 78.5 | 132 | 34.6 |
| 熔点 / 0C | -130 | 9 | -116 |
| 溶解性 | 易溶水 | 难溶水 | 微溶于水 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是
a、引发反应 b、加快反应速度
c、防止乙醇挥发 d、减少副产物乙醚生成
(2)在装置C中应加入
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
(3)判断该制备反应已经结束的最简单的方法是
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
(5)在装置B中较长玻璃导管的作用是
(6)反应过程中应用冷水冷却装置D,其主要目的是
(7)本实验中,1,2—二溴乙烷的产率为
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
解题方法
【推荐2】如图:1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79 ℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有溴水。
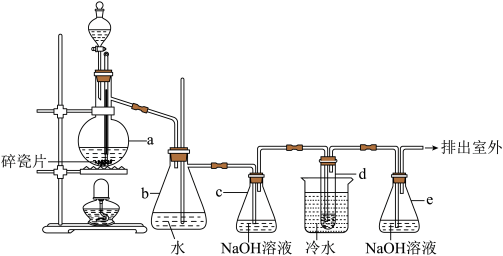
填写下列空白:
(1)写出a中的主要反应的化学方程式:__________________
(2)写出d中的化学反应方程式:____________________________________ ,并指出反应类型:
(3)容器c中NaOH溶液的作用是除去乙烯中混有的SO2,请说明如何鉴定某乙烯气体中混有SO2:_____________________________________ 。
(4)有同学提出分离1,2-二溴乙烷和溴的混合物,将混合物倒入稀的NaOH溶液,然后分离,此时所需两种主要的玻璃仪器是:______________ 。
(5)乙烯是一种重要的化工原料,如果将其与2-甲基-1,3-丁二烯以物质的量之比1:1在一定条件下混聚,请写出此混聚的化学方程式:_________________________ 。

填写下列空白:
(1)写出a中的主要反应的化学方程式:
(2)写出d中的化学反应方程式:
(3)容器c中NaOH溶液的作用是除去乙烯中混有的SO2,请说明如何鉴定某乙烯气体中混有SO2:
(4)有同学提出分离1,2-二溴乙烷和溴的混合物,将混合物倒入稀的NaOH溶液,然后分离,此时所需两种主要的玻璃仪器是:
(5)乙烯是一种重要的化工原料,如果将其与2-甲基-1,3-丁二烯以物质的量之比1:1在一定条件下混聚,请写出此混聚的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
解题方法
【推荐3】1,2-二氯乙烷( )是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置如下:
)是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置如下:

已知:①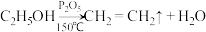
②

回答下列问题:
(1)仪器C的名称是________ ,装置甲中橡皮管的作用是________ 。
(2)装置甲中发生反应的离子方程式为________ 。
(3)制取1,2-二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用):________ 。
a→________→________→________→________→h-i←b←c←f←g←j
(4)装置丁中水的作用是________ 。
(5)相比酒精灯加热,己中采用甘油浴加热的优点是________ 。
(6)相比浓硫酸,用 脱水制乙烯的优点是
脱水制乙烯的优点是________ 。
(7)产品纯度的测定:量取5.5mL逐出 和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应:
和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应: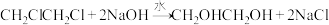 所得溶液先用稀硝酸中和至酸性,然后加入
所得溶液先用稀硝酸中和至酸性,然后加入 的
的 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的质量分数为
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的质量分数为________ 。
 )是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置如下:
)是重要的有机化工原料,不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下逐渐分解。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置如下:
已知:①
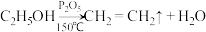
②


回答下列问题:
(1)仪器C的名称是
(2)装置甲中发生反应的离子方程式为
(3)制取1,2-二氯乙烷的装置接口顺序为(箭头为气流方向,部分装置可重复使用):
a→________→________→________→________→h-i←b←c←f←g←j
(4)装置丁中水的作用是
(5)相比酒精灯加热,己中采用甘油浴加热的优点是
(6)相比浓硫酸,用
 脱水制乙烯的优点是
脱水制乙烯的优点是(7)产品纯度的测定:量取5.5mL逐出
 和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应:
和乙烯后的产品,产品密度为1.2g/mL,加足量稀NaOH溶液,加热充分反应: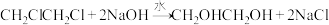 所得溶液先用稀硝酸中和至酸性,然后加入
所得溶液先用稀硝酸中和至酸性,然后加入 的
的 标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的质量分数为
标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,则产品中1,2-二氯乙烷的质量分数为
您最近一年使用:0次




